目的:创伤性脑损伤(TBI)的颅内压是动态变化的,并且受损伤类型、治疗、遗传等因素的影响。现有研究使用的是时间不变的汇总颅内压测量法,因此可能会缺失有关时间趋势的关键信息。我们确定了重型TBI患者的纵向颅内压轨迹,并评估其是否能预测预后。进一步构建模型以探索ABCC8基因多态性(一种已知的脑水肿调节因子) 在不同的轨迹组之间是否存在差异。
设计:前瞻性、观察性、队列研究。
单位:单中心学术医疗中心。
患者:重型颅脑损伤患者404例。
干预:无。
测量和主要结果:我们基于群体轨迹模型,通过结合危险因素调整(年龄、性别、Glasgow昏迷评分6分、开颅手术、原发性出血类型)来识别颅脑损伤后第0-5天的每小时颅内压轨迹。我们比较了轨迹组间6个月的预后(Glasgow预后评分、残疾评定量表、死亡率)和脑水肿相关的ABCC8标签单核苷酸多态性 (rs2237982,rs7105832)。构建回归模型以明确轨迹组能否预测预后。一种分6个轨迹的模型与数据拟合程度最高,确定了在初始颅内压、演变和大于20 mmHg的压力峰值的数量/比例方面不同的队列。在年龄、出血类型和开颅手术率方面存在模式差异。ABCC8基因多态性在不同组间存在差异。GOS(p=0.006)、残疾评定量表(p=0.001)、死亡率(p<0.0001)和rs2237982(p=0.035)在不同组间也存在差异。有趣的发现是低颅内压轨迹和持续的高颅内压都预测到不良预后。不同组间的颅内压变异性存在差异(p<0.001),这可能反映了颅内弹性/顺应性的保留或受损。
结论:我们采用了一种新方法来研究TBI的纵向/动态颅内压模式。在风险调整模型中,确定了六个轨迹分组并预测预后。如果得到验证,轨迹建模与其他表型分析工具(如生物标记物和神经成像)相结合,可能可以开发一种新的、精细的颅内压表型分析方法。 (Crit Care Med 2018; XX:00–00)
颅内高压是重型TBI预后不良的关键预测因子,其管理仍然是TBI指南的基石。然而,这种关系是复杂的。颅内压(ICP)是多种因素的动态产物,包括个体的大脑弹性/顺应性、脑水肿发生/消退的机制、血管调节失调/血容量、冲击特性和损伤复杂性。它进一步受到不可改变的因素的影响,如人口统计学和遗传学因素。目前包括大型试验在内的研究使用单一/汇总ICP测量措施对患者进行分类并确定治疗效果。然而单一/汇总ICP作为一个时间不变的平均值可能会掩盖时间趋势。单一ICP阈值也可能不足以区分日益异质性的脑外伤人群:近年来,老年患者出现脑萎缩/脑脊液空间增加、共病、较低的生理储备和神经可塑性降低,这可能会产生根本不同的ICP模式、最佳阈值和预后影响。在精确医学时代,ICP轨迹的个体差异可能有助于准确分型TBI。对ICP轨迹进行分类可能是新方法中有价值的“第一步”。它为未来的研究奠定了基础,以潜在地识别处于不利轨迹风险中的患者,最终为早期或预防性干预提供机会。因此,我们在这项探索性研究中有三个目标:1) 描述重型TBI患者队列中ICP演变的时间模式,2) 评估这些模式是否影响了预后,3) 轨迹分析是否增加了传统阈值之外的洞察力。
群体轨迹模型(GBTM)是一种已建立的分析方法,可以识别在一段时间内遵循某一度量的相似进程的个体群集。它越来越多地用于医学研究。我们使用GBTM定义纵向ICP轨迹,并在重型TBI中识别潜在的不同模式。我们测试了生成的ICP轨迹组作为预后预测因子的效用。为了验证这一模型,我们探索了组间差异的潜在遗传因素。由于ABCC8编码磺酰脲类受体-1(Sur1),这可能是TBI脑水肿的调节因子,我们评估了ABCC8基因多态性与已报道的脑水肿相关性是否在不同的ICP轨迹组中有所不同。
方法
研究设计
本研究是一项前瞻性队列研究,纳入了2000年至2014年来自单一学术医疗中心的446名重型TBI患者(GCS评分≤8,按照标准治疗,使用脑室外引流术(EVD)和颅内压监护仪进行临床表现和颅内压的监测)。排除了出现脑死亡症状、怀孕和无ICP记录的患者,最终产生了一个404名患者的队列。患者按照标准机构方案进行治疗(详见补充材料)。如果中止治疗,则不能获得进一步的ICP测量,并且按照标准临床程序停止监测。知情同意是从医疗卫生机构获得的。匹兹堡大学IRB批准了这项研究。
临床数据收集
人口统计学、临床信息(年龄、性别、GCS评分)、原发性出血模式和每小时ICP由对ABCC8基因型不知情的研究助理收集。原发性损伤/出血类型(硬膜下、蛛网膜下腔、脑实质内挫伤、硬膜外、脑室内和弥漫性轴索损伤(DAI)是根据最初CT扫描的最终放射学报告确定的,并由有经验的研究助理进行审查确认。对于具有一种以上原发性损伤模式的患者,在没有规定的情况下记录了两种最显著的模式。疑似DAI的点状CT出血均经MRI证实。从钳夹式EVD记录(n=353)或实质内监测仪(n=51)获得监护仪放置后1-120小时内的每小时ICP测量值(根据我们的机构方案的标准持续时间)。对于EVDS,压力传感器放置在耳屏水平。预后的评定包括6个月 GOS评分(不利:GOS<4;有利:GOS≥ 4) 、6个月残疾评定量表评分(DRS)(连续)和6个月全因死亡率。预后是由有经验的研究技术人员在有执照的神经心理学家的监督下,使用GOS和DRS的标准表格通过电话确定的。
DNA收集,标签单核苷酸多态性基因分型和选择
DNA的提取如先前报道所述。采用HapMap(Build-36)和tagger算法配对的方法,检测到23个ABCC8标签单核苷酸多态性(SNPs),r2≥0.8,等位基因频率>0.20。使用iPlexGold进行基因分型。基因型分析采用Typer-4.0分析法。经过质量控制后有410个样本可用(详见补充方法)。两个Tag-SNPs,rs2237982和rs7105832可能与传统的脑水肿标记物相关并被用来评估与ICP轨迹的相关性。
GBTM与统计分析
我们使用具有截断正态分布(0-40 mmHg)的GBTM来建立最初120小时内的ICP轨迹。我们使用由贝叶斯信息准则(BIC)来选择最佳组数,并通过逐步回归来迭代消除不重要的多项式项,以获得最简单的最终模型,其中每个轨迹组在α=0.05时具有显著性(详见补充表1)。我们的模型包括对年龄、性别、初始GCS评分、急诊开颅手术和原发性出血类型的时间不变风险因素调整。我们重复这一过程仅限于未接受开颅手术的患者,还包括特定CT特征作为风险因素的后续模型,特定CT特征包括脑疝、基底池消失、脑室消失、脑沟消失、中线移位程度。
组间比较采用方差分析F检验和Fisher确切检验法。校正了两两比较(Bonferroni法)。对于多变量风险调整GBTM确定的最终轨迹组,我们使用Logistic和线性回归模型来确定组(编码为分类变量)是否能预测预后。Hosmer-Lemesshow测试确定拟合优度。以最大轨迹组作为参照组。作为比较,传统的多变量线性和Logistic回归模型根据平均ICP来预测6个月时的预后。使用Stata 14.0进行统计分析。
结果
ICP轨迹组
最终模型确定了六个不同的轨迹组(图1)。组成员的平均后验概率≥0.90,表明分组良好。表1总结了临床和人口学特征。年龄、急诊开颅手术和原发损伤类型在各组之间存在差异,但性别或初始GCS评分不存在差异。传统记录值(平均ICP、中位数和ICP峰值的比例)在不同组之间也不同(详见表1和补充表2)。与单一测量值相比,GBTM分类具有更细微的模式差异和预后意义(随后公布)。
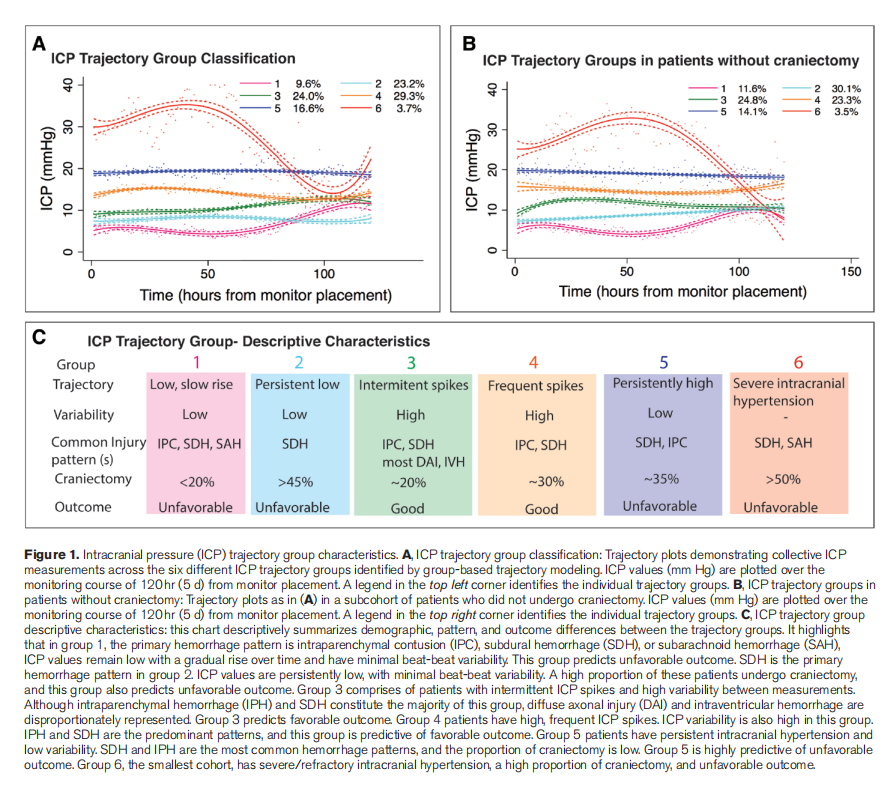
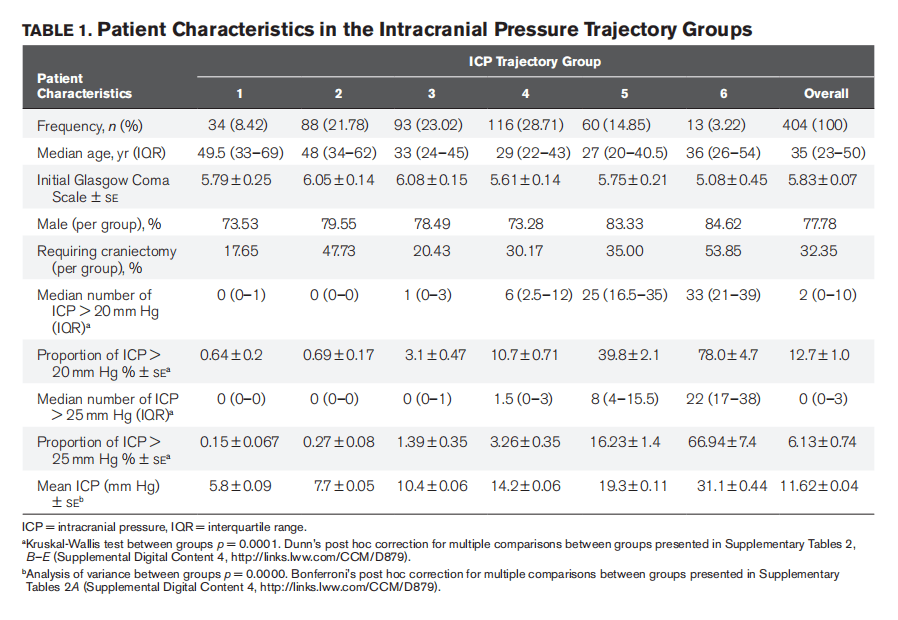
ICP特征:各组的纵向ICP轨迹逐渐升高(图1A)。“组1”(n=34)的ICP较低,并随时间逐渐升高。“组2”(n=88)的ICP比组1高,但仍持续较低。“组3”(n=93)有两位数的ICP,罕见的峰值>20 mmHg,“组4”(n=116)是最大的组,间歇性ICP峰值>20 mm Hg。在整个监测期间,组4的ICP均高于组3,且出现更频繁的尖峰(表1,图1;补充图1)。“组5”(n=60)持续升高ICP,频率在20至30 mmHg(平均19.19±0.11 mmHg)之间。“组6”(n=13)是一组早期严重颅内压持续升高的小队列,在最初的48小时内持续升高。经整理的单个ICP测量结果如补充图1所示。图1C总结了每个ICP轨迹组内的一般特征。
临床特征:第1组(49.5)和第2组(48)的中位年龄高于其他组(表1)。还评估了各组之间的放射学和开颅手术差异。
损伤模式:所有轨迹组中最常见的三种原发性损伤模式是硬膜下损伤、挫伤和蛛网膜下腔出血(详见补充图2)。257例患者在初始CT上有一种以上的损伤类型。在所有ICP轨迹组中,额叶和弥漫性损伤最常见(详见补充图2B)。虽然在第6组中硬膜下血肿的比例比其他组略高,但并不显著(p=0.084)。各组的病变体积相似,尽管第5组的硬膜外血肿看起来更大,但并不显著(p=0.35)(详见补充图2C)。亚组中的样本量太小,无法对每种病变类型进行有意义的轨迹建模或比较。第3组DAI和IVH患者的比例不对称:超过50%的DAI和70%以上的IVH患者在该组。补充图2A表明,组1和组3中DAI的组内比例似乎高于其他组(无统计学意义),尽管这些组预后较好的几率不同(详见结果部分)。
影像学水肿:显示任何一种急性CT水肿征象(定义为中线移位、基底池消失、脑沟消失、脑室消失、脑室脱出)的患者的比例在不同组之间存在差异(p=0.001)(详见补充图3A)–第6组水肿患者的比例最高,第1组最低,第2-5组相似。补充图3B显示了每个轨迹组内急性水肿的CT个体征象的分布。中线移位的程度(p=0.09)和脑疝证据(p=0.087)在两组之间无差异;但是,基底池消失有统计学差异 (p=0.002),其中第6组比例最高(详见补充图3B)。风险调整模型,包括CT水肿的任何征象或一系列潜在的危险征象(中线移位程度、基底池受压、脑疝)没有改变ICP轨迹模式(详见补充图3C,D)。
开颅手术:所有组的大多数开颅手术都是在症状出现后24小时内完成的(详见补充图4)。第1组中,17.65%的患者行开颅手术。第2组(47.73%)和第6组(53.85%)行开颅手术的患者比例较高。
有趣的是,6组模型即使在没有行开颅手术的亚组中,也会产生几乎相同的ICP轨迹组(图1B,补充表 3),令人惊讶的是,在该队列的第6组中,60-75小时后ICP迅速下降不是由于手术干预,而是基于这些早期严重颅高压患者的病理生理途径的ICP的自然演变。此外,尽管在约75%的队列中,开颅手术是急性的(<24小时),但在第6组接受开颅手术的患者中,100%的患者是急性的(补充图4A)。ICP轨迹组5是唯一一组在前72小时内开颅术次数分布相似的组–该组在开颅手术前后都有持续的颅内高压。晚期开颅手术也与晚期ICP升高的临床意义一致。GBTM将开颅手术从二元风险因素调整变量替换为连续变量(以评估其如何影响轨迹模式),其证实了该模型的鲁棒性/稳定性(补充图4B)。
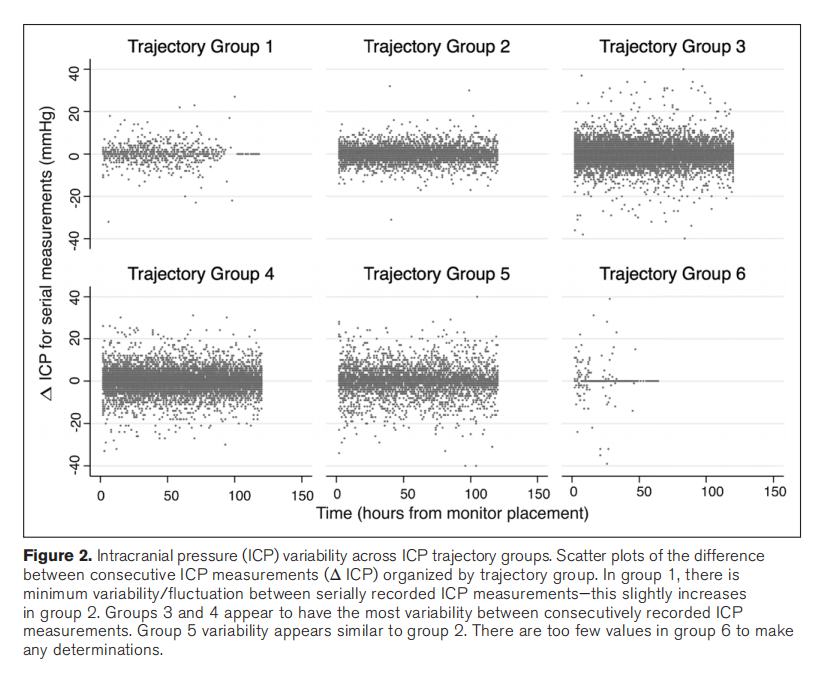
其他特点:不同轨迹组退出治疗的情况不同(p=0.02),组2中退出比例最高;经Bonferroni矫正后,组间比较无显著意义(补充图5A)。不同轨迹组的损伤严重程度评分没有差异(补充图5B)。不同组间连续测量之间的时间ICP变异性/波动不同(p<0.001)(图2),第3组和第4组的差异高于其他组(p<0.001)。
不同ICP轨迹组的6个月TBI预后不同
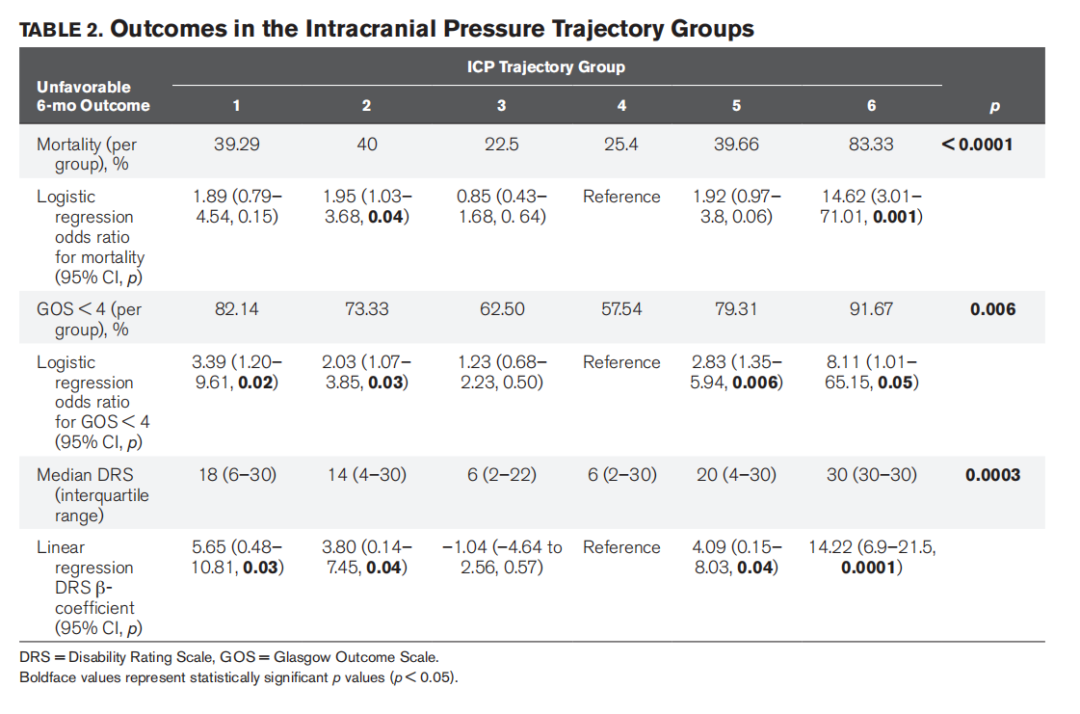
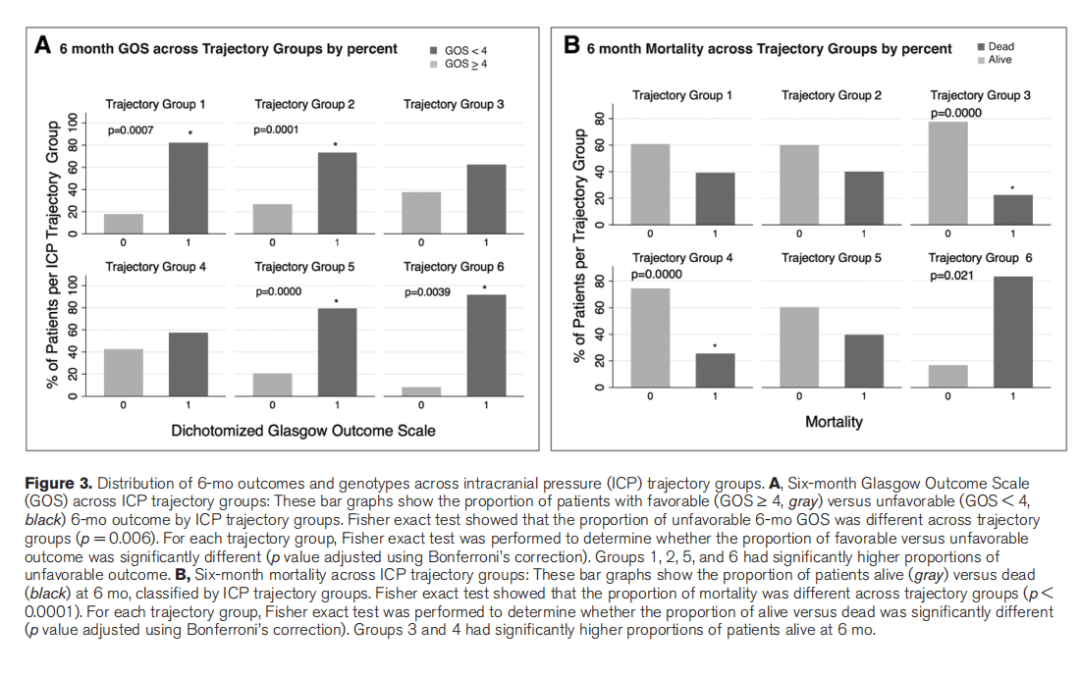
较差的6个月GOS(p=0.006)、DR(p=0.0003)和死亡率(p<0.0001)在不同的轨迹组中不同(表2和图3)。ICP轨迹组内比较显示,第1组(中位年龄49.5岁,缓慢上升的ICP),第2组(中位年龄48岁,开颅手术比例高,持续低ICP),第5组(中位年龄27岁,持续升高的ICP)和第6组(重度/难治性颅高压)的较差GOS评分比例较高(图3A)(均P<0.001)。第3组和第4组(间歇性ICP峰值,较高的变异性)的存活率较高(图3B)(均P<0.0001)。
ICP轨迹组成员预测了所有评估指标的6个月结局(表2,图3;和补充图6)。尽管组1、组2、组5和组6在ICP绝对值方面处于相反极端,但组1、组2、组5和组6有更高的DR和更高的较差GOS比例 (图1和表2)。令人惊讶的是,即使在没有开颅手术的患者中,这些结局仍然存在,并且在风险调整模型中,包括CT危险水肿X线征象(中线移位程度,基底池消失,脑疝)。组1和组5继续预测≤50岁患者的发病率。
我们的队列是可靠的,因为这些患者的传统模型验证了先前报道的不良预后因素,如年龄、初始GCS评分、平均ICP以及大于20和25 mmHg的ICP测量比例(补充表4C-F)。我们的队列进一步证实,这一预测结果不适用于幸存者(ICP平均值,p=0.77,ICP>20 mmHg的比例,p=0.22)(补充表4 C-E)。GBTM分类提示,基于点测量值的模型可能无法检测到重要差异(补充结果ii):即使在幸存者中,轨迹组仍可以预测不良预后,,并且平均ICP/和最小频率尖峰大于20或25 mmHg的组的不良预后几率增加。
ABCC8-Tag SNP rs2237982基因型在ICP轨迹组中不同
rs2237982和rs7105832此前已被认为与传统的脑外伤水肿指标有关,包括CT水肿。不同ICP轨迹组的rs2237982(p=0.035)而非rs7105832(p=0.135)的基因型频率不同(补充表5,补充图6 C-D)。不同ICP轨迹组的rs2237982杂合子不同(p=0.013),第1组杂合子比例过高(67.7%)(补充图6D)。补充结果-ii提供了额外的事后差异。
讨论
理解和管理ICP仍然是TBI治疗的基础,因此对其分型至关重要。我们采用了一种新的、动态ICP测量方法来研究TBI中的ICP模式。这种分类系统解决了目前TBI人口统计学问题,增加了时不变的点测量值的细微差别,并且可以为最终开发基于ICP的临床治疗、患者选择和重型TBI的预测提供新的见解。
ICP轨迹组作为一种新的分类策略
在风险调整模型中,根据不同的ICP模式和临床特征来区分本研究中识别的6个不同的ICP轨迹组。ICP轨迹组是多项测量中6个月预后的独立预测因素,并质疑传统定义/病理生理学。出乎意料的是,6组模型在未行开颅手术的亚组患者的轨迹模式和预后预测方面产生了几乎相同的结果,并且大多数患者的组成员保持不变,除了ICP轨迹组3的患者和较小程度的组4的患者–所有人在未行开颅手术的队列中都过渡到组3(补充表3)。这可能表明了组间固有的未测量差异的一个组成部分,如果得到验证,则需要表征。固有差异与治疗策略对ICP轨迹组成员的影响程度尚不清楚,组成员的可操作程度也是未知的。这些因素会影响不同中心队列中是否会出现相似或不同的ICP轨迹。本研究为在今后的工作中探索这些重要问题奠定了基础。
目前的证据表明,颅内高压(ICP≥20-25 mmHg)和ICP峰值比例与幸存者的死亡率有关,但与致残率无关。我们队列中的传统模型证实了这一发现。然而,基于轨迹的分类结果发现了两组令人惊讶的患者,尽管ICP较低,但预后不佳(组1和组2)。这种联系的原因尚不清楚,本文尚未解释清楚;然而,这些组可能存在未测量指标上的差异,如萎缩、大脑顺应性、神经可塑性、神经血管耦合等方面。虽然这种关联可能部分归因于这些组中较高的中位年龄,但在第1组中,即使在≤50岁的患者中,与不良结局和死亡率的关联也是真实存在的。因此,轨迹组之间的差异可能反映了细胞功能障碍和生理上其他重要的不可测量的变异性。此外,与平均ICP不同,ICP轨迹组1和组5预测了幸存者的不良预后。因此,我们认为,对所有患者使用点测量值和相同阈值的规则可能不足以区分TBI后复杂和动态的生理学变化:将患者分为ICP轨迹组是认识到纵向时间趋势和患者组之间更细微差异的潜在重要性的第一步,从而确定未来研究的潜在患者组。
目前对模式与点测量的价值进行了探索。难治疗的ICP比绝对值更能预测预后。ICP>20 mmHg可能影响预后。我们的轨迹组分类支持这些概念。第5组和第6组有持续性的颅内高压,明显增加了不良预后的几率。然而,这些模式并不能解释组1和组2(低ICP)与不良预后之间的关系。我们假设,ICP的“可变性”可能是一个重要的预测性因素,表明诸如更健康/更灵敏的弹性或完整的神经血管偶联等现象–这些可能代表了一个需要进一步探索的早期表型。先前的研究已经证明,生理变量的反应性/完整的自我调节表现与TBI预后之间存在关联–这是否只与体内平衡完整性有关,还是受到干预/系统因素的影响尚不清楚。因此,与EEG变异性/反应性或反映脑血管反应性的压力反应指数的预测价值相似,健康的脑组织在ICP测量中可能有更大的变异性(组3和组4)。另一种可能的解释是,顺应性差的/不健康的大脑预示着不良的预后。我们的发现也可能在某种程度上反映了对治疗的反应,但尚未完全确定。
高分辨率的动态ICP分类系统如果得到验证,与其他表型变量一起最终有助于指导患者选择试验,最大限度地减少治疗效果稀释,预先指定的亚组分析/适应性设计试验,促进生物标记物的发现以预测轨迹,并指导基于个体表型的临床治疗阈值的差异。这需要与其他完整的(和相关的)生理变量相结合,包括脑灌注压、压力反应性指数/自我调节状态和脑组织氧合。在未来的研究中,使用纵向轨迹分析来探索这些额外的变量可能是有价值的。虽然我们没有探索ICP轨迹组的先验预测,但我们的结果为此类研究提供了框架。
年龄和ICP轨迹组
TBI的情况在最近几十年已经发生了变化。临床指南所依据的患者与当前流行病学最明显的区别之一是向老年患者的转变。这与不同的损伤机制、年龄相关的合并症、损伤前抗血小板/抗凝药物的使用、生理储备/病理生理反应(包括依从性、ICP)、临床病程和转归有关。这些差异可能导致不同的ICP模式、最佳阈值和预后影响。第1组和第2组的中位年龄比其他组高,是不良预后的独立预测因素。即使在50岁以下的患者中,第1组仍有良好的预测能力;而第2组则不能。在这两种情况下,都极少发生颅内高压。这些结果提出了一些具有争议性的问题,包括ICP监测在特定年龄组/损伤特征的患者中的实用性,或者是否需要替代治疗阈值。对于≥55岁的患者,建议降低ICP阈值。ICP的适度增加可能反映了老年患者由于年龄相关性脑萎缩和/或依从性降低而造成的更严重损伤。也有人提出减少对老年患者的ICP监测,然而,需要平衡对这一人群的不合理的消极态度,他们在积极治疗后可能会有预后较好。
遗传学与ICP轨迹
遗传因素在TBI预后中的作用越来越受到重视。这些关于脑水肿的数据是有限的,但不断发展,并且具有表面效度。由ABCC8编码的Sur1介导的水内流是脑水肿的一种独特途径。在卒中II期试验中,格列本脲的抑制作用有望减轻水肿,ABCC8变异与脑水肿和脑外伤预后相关。因此,测试ABCC8基因多态性(rs7105832,rs2237982)是否与传统的脑水肿指标(平均/峰值ICP,CT水肿)在ICP轨迹组之间存在差异似乎是合乎逻辑的。在我们的分析中,rs2237982基因型在各组间存在差异。ABCC8/Sur1通路是遗传多样性在该过程中所起作用的一个例子。我们选择它是因为ABCC8基因多态性很可能是影响脑水肿/神经保护的通路中更大的遗传变异性的例子。基于ICP轨迹组的分类最终可能更精确地反映TBI队列中的分子、遗传和病理生理学的差异。
局限性
这项研究为探索早期轨迹预测方法奠定了基础;定义预测群体成员所需的ICP轨迹观察的最短持续时间超出了本分析的范围。目前的临床局限性,就患者分类的直接转化为床边效用而言,是未来工作的一个重要考虑因素。更高分辨率的数据(通过波形分析或自动每分钟测量)可能提供额外的潜在有用的表型。我们的发现尚未确定早期患者分类的方法、干预的目标,也没有分析不同的干预措施如何导致患者改变轨迹组。序列自相关滞后在每一组中评估也可能是有趣的,因为这些可能是潜在生物过程的典型时间尺度的指标。然而,如果不首先识别/轨迹表征模式来分析预后,这些问题就无法得到回答。我们的研究结果为未来的表型研究和生物标记物的开发奠定了基础,以探索生物学底物,这些生物底物可以1)更早地识别患者的病程轨迹,2)洞察轨迹组之间的病理生理/分子/遗传的差异,3)评估早期/预防性治疗,并可能为临床试验的患者选择提供信息。
这是一项容易出现选择/机构偏倚的单中心研究。然而,它有治疗一致性的优势。在其他中心复制该研究将是有益的:一致的结果可能表明固有差异,而模式的改变可能意味着管理的影响。手动ICP记录可能不如自动数据敏感。虽然我们机构的大多数急诊开颅手术是针对肿块性病变而非难治性颅高压,但我们的数据没有区分这一点,也没有包括预防性开颅手术的比例或开颅术大小的信息。治疗强度的测量无法区分组(特别是4组和5组)在管理方面的差异 (例如,高渗盐水的使用,开颅手术的范围)。这是主要的局限性,因为这可能会改变ICP水平/模式,以及这些轨迹对预后的影响。尽管ICP轨迹组受到治疗的影响,但对无偏轨迹进行前瞻性分析属于非伦理行为。然而,与未行开颅术患者相比,所有患者有着几乎相同的轨迹组分类。可能具有重要临床意义的晚期ICP升高被遗漏。我们的数据还可能存在难控制的时间偏倚的影响;然而,自2006年以来,同样的方案一直在实施,与之前的版本相比,唯一显著的变化是脑组织氧合监测仪的设置(不太可能显著影响ICP的轨迹)。
虽然GBTM对于纵向预测策略很有价值,但它使用多项式平滑算法,这可能是非生理性的。为了给模型提供限值,ICP>40 mmHg被视为当量ICP,超过该阈值可能会增加死亡风险。我们的模型根据损伤严重程度和原发损伤模式进行风险调整,然而,有限的样本量限制了损伤模式/位置亚组内进行有意义的统计比较。在未来的研究中,对这些变量进行更详细研究可能会揭示出不同于ICP轨迹的对结果的额外影响。在每个亚组中有足够的患者参与的大型研究对于识别ICP轨迹组和损伤模式或部位之间的相互作用及其对预后的相对影响非常重要。可能还有其他(目前未知的)因素同时影响预后和ICP轨迹,如神经血管解耦联、大脑顺应性、脑组织氧合/脑代谢需求。例如,早期的一项儿科研究得出了一个有趣的低ICP和低脑组织氧合的患者群体;分析ICP轨迹组和脑组织氧合之间的纵向相互作用可以进一步深入了解患者亚群。因此,尽管ICP轨迹组提供了有价值的高分辨率信息,但本研究分析的ICP仅是“TBI可变性的复杂拼图中的一块”–我们的结果为今后分析提供了初步的基础,以便与TBI中的其他重要生理变量(如:脑灌注压数据、自我调节状态、波形分析、脑组织氧合、损伤模式和位置或脑电图数据)来探讨这一点。ICP轨迹与其他变量的结合对于TBI表型预测最大精确值可能是必不可少的。
结论
我们报告了一种新的基于ICP轨迹的分类方法,以初步了解TBI中该指标的动态纵向模式。确定的6个ICP轨迹组有助于提高对ICP和TBI预后与点测量值之间关系的洞察力。在我们的风险调整模型中,ICP轨迹组意外地预测了6个月的死亡率和致残率,低ICP轨迹组也预测到了不良预后。颅内压变异性可反映颅内顺应性/弹性状态,并且在预后较好和较差的轨迹组之间存在差异。这种ICP方法为未来评估轨迹组的早期识别、病理生理差异、生物标记物的开发和干预效果的研究奠定了基础。如果经过验证和改进,ICP轨迹模型结合其他变量(包括神经成像、生物标记物、自我调节状态、多模态数据和电生理数据),可能有助于临床试验设计、精确医疗驱动的治疗和TBI的预测。
https://pubmed.ncbi.nlm.nih.gov/30119071/
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。









 微信扫一扫
微信扫一扫