摘要
子痫前期和子痫是与胎盘血管发育异常有关的妊娠高血压疾病。胎盘发育异常引起的系统性血管生成失衡、内皮功能障碍和促炎状态导致肾、肝、肺和神经功能异常。与妊娠引起的高血压(PIH)有关的神经感觉症状,其中最具破坏性的是颅内出血和癫痫发作,是全球孕产妇和围产期发病率和死亡率主要原因之一,但危险分层策略和针对性的治疗方法仍难以捉摸。目前对具有严重特征的子痫前期的治疗仅限于分娩、抗高血压治疗和硫酸镁预防癫痫发作。硫酸镁可降低严重子痫前期患者的癫痫发生率,但会使患者容易无力、子宫收缩乏力、肺水肿和呼吸抑制。因此,理想情况下,该药物应仅适用于神经系统并发症风险会增加的子痫前期患者。尽管尚无客观方法可预测子痫,但我们假设对视神经鞘管直径、视盘高度和大脑中动脉经颅多普勒阻力指数的测量可能有助于识别亚临床脑水肿,可能使我们识别那些癫痫风险最高的患者。
这个对当前文献的总结为开发更复杂和无创的方法提供了一个初始框架,以识别、监测和治疗那些因子痫前期而引起的神经系统并发症风险最高的产妇。
关键词:子痫前期 子痫 孕产妇死亡率 妊娠高血压疾病 神经病理生理学
引言
高血压疾病每年影响全世界2.13亿孕妇中的5%至10%,并且是孕产妇发病率和死亡率的主要原因,因为全世界16%孕产妇死亡是与此家族相关疾病的并发症的直接结果。子痫前期和子痫每年造成全球约50,000例死亡(非洲25,000例,亚洲22,000例,拉丁美洲和加勒比2800例以及工业化国家150例产妇死亡)。这些死亡中有70%以上是神经系统原因,归因于脑或肺水肿、颅内出血和子痫。
了解脑自动调节、内皮功能和血管生成平衡对于子痫前期和子痫的管理至关重要。尽管高血压是一个高危特征,但正常高血压患者可能会出现神经系统异常,如可逆性后部脑病综合征(PRES)。此外,血压与重度癫痫发作(子痫)之间几乎没有相关性。为什么有些子痫前期妇女容易发生神经系统并发症,而其他人却不易,这仍然难以确定,而在系统性症状(即高血压、神经系统症状)开始之前确定脑水肿亚临床升高的客观方法目前尚不存在。因此,我们有义务通过预防硫酸镁来治疗任何具有严重特征的子痫前期母亲。
子痫前期的大脑自身调节失调、肌源反应性不良和血脑障碍完整性障碍集中于脑水肿的共同途径上,这在很大程度上解释了该人群中PRES、抽搐发作和中风的临床表现。这在很大程度上解释了该人群的PRES,癫痫发作和中风的临床表现。我们假设,如果脑水肿是所有具有子痫前期神经感觉症状患者的共同发现,通过常用技术(超声)及早发现颅内压升高可以使我们在症状发作之前识别出高危患者。
根据ACOG高血压特别工作组的定义,子痫前期定义为新发高血压(SBP> 140 mmHg或DBP> 90 mmHg)伴妊娠20周后蛋白尿(24小时内尿蛋白> 300 mg或尿蛋白:肌酐> 0.3)。在没有蛋白尿的情况下,如果高血压伴有以下任何情况,则可诊断为子痫前期:血小板减少症(血小板计数<100,000cell/uL),肝功能受损(≥正常ALT的两倍),肾功能不全(在没有其他肾病的情况下,血清肌酐>1.1mg/dl或血清肌酐加倍),肺水肿,或新发性的脑紊乱或视觉障碍。
SBP> 160 mmHg或DBP> 110 mmHg且伴以下任何一项的患者:血小板减少,肝功能受损,持续性头痛或神经系统症状,持续性上腹或右上腹疼痛,24小时内少尿少于500 mL或肺水肿,可诊断为重度子痫前期。患有重度子痫前期的患者几乎普遍接受了硫酸镁预防,这种预防一直持续到产后。
子痫的定义是在有或没有伴发高血压的产妇中出现新发作的癫痫大发作,并可能在分娩前、分娩中或分娩后发生。
妊娠高血压的特征是在妊娠20周后血压开始升高,但没有蛋白尿。在怀孕期间,慢性高血压被定义为在受孕前或在妊娠20周前被发现的高血压
提出机制
子痫发作的发展以及与子痫前期有关的轻度神经感觉症状具有共同的病因,即脑水肿。脑血管失调、高血压脑病,可逆性后部脑病综合征(PRES)和实质内出血均会导致脑水肿。脑水肿会导致神经元易怒、神经功能受损、颅内压(ICP)升高,在严重的情况下会因脑灌注受阻而导致疝或神经元死亡。这种潜在的常见途径的临床症状从轻到重不等,包括持续性头痛、反射亢进、视力障碍、精神状态改变、中风和癫痫发作。这些症状的发作是血管生成失衡、促炎状态、脑自动调节功能失败以及微循环和血脑屏障(BBB)破坏之间复杂相互作用的结果。
脑水肿可被分为血管源性或细胞毒性,这取决于BBB是否被破坏。血管源性脑水肿被认为是妊娠高血压疾病中神经感觉症状的主要驱动因素。孕妇静水压力升高,加上内皮通透性增加和脑自动调节障碍,均会导致血管源性水肿。细胞毒性水肿可能在子痫中起作用,但在有神经系统症状的子痫前期或子痫患者的影像学研究中,神经元死亡并不普遍存在。
在这里,我们的目的是解释怀孕如何使女性适应这些病理变化,并提出一种更有选择性的方法来识别那些出现神经感觉症状或子痫风险最高的人。我们希望本讨论能介绍当前技术以发展我们的诊断、预后和治疗选择,使我们能够探索出更多方法以更好地选择哪些患者受到侵入性或高风险干预措施如引产、剖宫产、硫酸镁治疗。
3.脑自动调节
需要严格调节脑血流量(CBF)才能满足活动神经元的能量需求,维持神经元功能并保持细胞完整性。脑自动调节是在一定的平均动脉压(MAPs)或脑灌注压(CPP)范围内维持CBF的生理过程。高于和低于此限制,将失去自动调节功能,并且CBF线性遵循MAP。
4.脑自动调节的决定因素
脑血流主要受血管平滑肌的肌源性反应调节,该反应包括两个部分:张力和反应性。在健康的患者中,MAP的变化会引起血管平滑肌张力增加或血管口径缩小。反馈回路可防止过度的血管舒张或血管收缩,并且脑动脉的反应性不均一。事实上,来自内皮细胞和血管周围神经的局部代谢物和血管活性因子会影响肌源性张力和血管阻力。
脑自动调节由“静态自动调节”(对MAP或CPP缓慢变化的响应)和“动态自动调节”(对MAP或CPP迅速变化的响应)组成。在正常情况下,自动调节功能可在50-150mmHg的MAP范围内将脑血流量保持在50mL/100g脑组织/分钟(图1)(从而将脑灌注压力(CPP)维持在50—70 mmHg之间)。慢性高血压使自动调节曲线右移,但在较高的MAP时保留了自动调节和脑灌注压力。子痫前期患者表现出动态自动调节功能受损,因此难以适应该疾病特征性的血压突然升高。
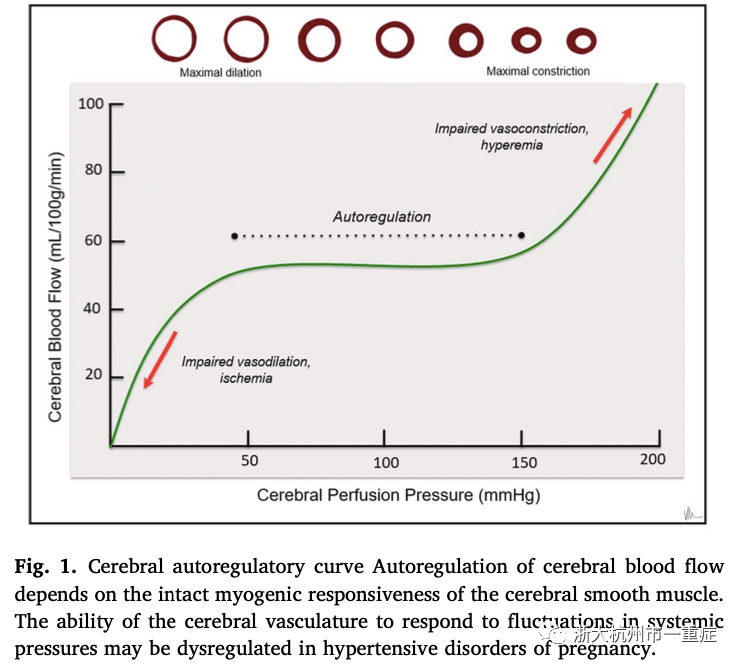
5. 子痫前期/子痫的脑血流失调
如上所述,脑血管中的肌源性反应旨在血压升高的情况下引起血管收缩。2011年,Ryan等人证明了妊娠大鼠的胎盘局部缺血会损害离体的大脑中动脉(MCA)的成肌活性。在这些从胎盘缺血大鼠中分离出的体外MCA中,他们发现动脉的直径随着腔压力的增加而增加。在体的随访激光多普勒血流仪对胎盘缺血大鼠脑血流的研究表明,脑血流可随着血压的持续升高而被动增加(异常自动调节指数,ARI)。在另一项关于脑血管自动调节的研究中,van Veen等人通过妊娠高血压、慢性高血压、子痫前期和子痫对110名高血压孕妇进行分层。在这项研究中,他们发现与正常血压的女性或仅患有妊娠高血压的女性相比,子痫前期和慢性高血压女性的自我调节指数显著降低。尽管各组之间的ARI有所不同,但所有组的ARI仍在正常范围内,因此该发现的临床意义仍不清楚。
妊娠中大脑自动调节功能受损和血脑屏障破坏的主要后果是血管源性水肿。脑血管阻力(CVR)的变化与管腔半径的四次方成正比(r4)。因此,产妇大脑血管口径的微小变化会导致CBF的较大变化。实际上,以前的研究提示妊娠可以预防或逆转高血压性脑血管重塑。这个概念可以解释为什么与未怀孕的患者相比,怀孕期间在较低的全身血压下会发生充血和脑水肿。最终,当脑血流失调时,血管内压力的增加更容易克服动脉和小动脉的肌源性血管收缩,从而削弱其提供阻力的能力。结果是内皮损伤和水肿,增加了神经元易惹、受伤和死亡的风险。
6.血脑屏障通透性
为了保持正常的大脑功能,神经环境必须保持在一个狭窄的稳压范围内,依赖于血液和大脑之间分子和离子运输的紧密调节。血脑屏障(BBB)提供了这种高度专业化的内皮细胞半透层,可通过限制水和各种溶质的通过来调节循环血液与大脑之间的化学、离子和代谢平衡。
维持这种微调的系统涉及三种主要的细胞类型。首先,微血管内衬有内皮细胞,内皮细胞具有30–40nm厚的基底膜,由胶原蛋白和各种细胞外基质蛋白组成。这些内皮细胞周围有周细胞和星形胶质足突,这两种都是必不可少的细胞类型,它们形成了将血管与脑组织分开的额外连续层(图2)。内皮细胞通过跨膜蛋白建立的高电阻紧密连接而连接,并表现出低的胞饮作用,从而形成了扩散屏障。星形胶质细胞足紧紧包裹着血管壁,对于诱导和维持紧密连接屏障起着至关重要的作用,但不认为具有独立的屏障功能。周细胞是在星形胶质细胞附近发现的收缩细胞,在BBB的诱导和形成中起重要作用。人们认为周细胞可以在毛细血管水平上调节微血管的血流,视网膜微脉管系统中这种现象的视频也已经发表。在衰老的动物模型中,这种细胞类型的功能障碍或缺失与血脑屏障完整性的丧失和局部脑血流的减少有关。
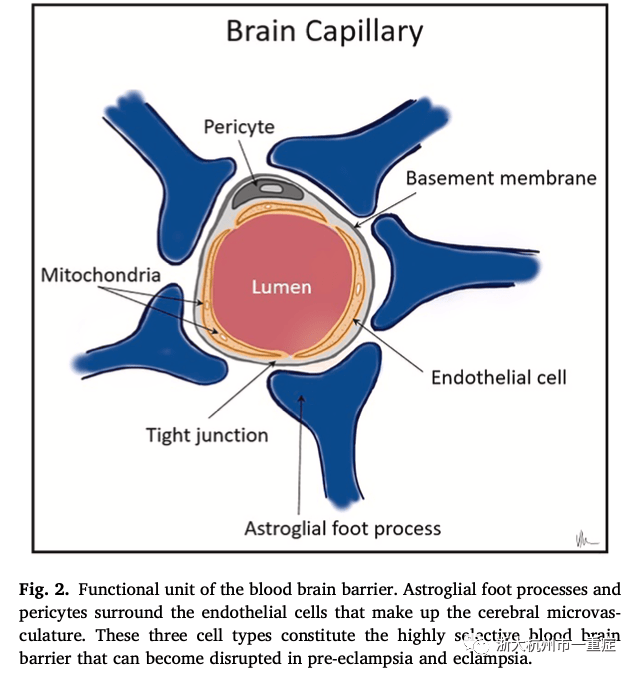
分子通过三种主要机制穿越血脑屏障:1)细胞外转运(小的亲水性物质),2)被动转运(CO2,O2)或易化转运(小的亲水性分子),以及3)主动转运(葡萄糖和对大脑代谢至关重要的氨基酸等大型大分子通过BBB主动转运)。
子痫前期状态与血脑屏障破坏有关。临床上,BBB的功能障碍导致组织液中离子、神经递质和代谢产物的失衡,从而导致异常神经元活动。另外,这种渗透性的增加与血管源性水肿的发展有关。使用大鼠的妊娠模型,Amburgey等人在子痫前期和正常分娩中研究了脑血管被动暴露于血浆后,血脑屏障渗透性、成肌活性以及内皮血管扩张剂的影响。在这项小型研究中,大鼠静脉和动脉腔内暴露于正常分娩和子痫前期的20%血浆。这项研究确定,暴露于子痫前期血浆后,血脑屏障通透性被扩大了。
6.1 促炎状态
子痫前期和子痫中子宫-胎盘缺血的主要病理后果之一是各种体液因子的释放,包括炎症细胞因子、内皮素、组织型纤溶酶原激活物、神经激蛋白β和补体蛋白。这些因子通过影响多个系统来影响产妇的体内平衡,但在这里,我们将重点关注这些因子与血脑屏障、脑自动调节以及水肿和子痫发作进展之间的关系。
神经激肽B(NKB)是一种化学调节剂,在非妊娠和血压正常的孕妇中含量较低,但子痫前期患者中的含量过高。NKB引起平滑肌收缩、血管和免疫学改变导致妊娠期某些血液动力学改变。NKB还可通过激活兴奋性谷氨酰胺受体来增强癫痫状态样的放电。它是已知的基于癫痫动物模型的促惊厥药,其作用机理涉及通过释放内皮素-1直接或间接激活谷氨酸受体。
一氧化氮(NO)的也可在子痫中产生,一氧化氮(NO)是一种平滑肌松弛剂,其水平在正常妊娠中会增加。在患病状态下,NO的过量产生会导致神经血管过度扩张,而氧自由基的产生则会对神经元组织造成伤害。
6.2 促炎细胞因子
在子痫前期中,血浆中促炎细胞因子例如TNF-α、IL-6和IL-10的水平升高。这些细胞因子激活内皮并改变BBB通透性。促炎细胞因子也被认为可增强兴奋性神经递质谷氨酸的作用。
6.3补体蛋白
补体系统是先天免疫系统的主要分支,涉及激活肝脏产生的蛋白,从而触发吞噬作用、炎症和膜攻击。激活后,补体蛋白(分裂片段)通过经典途径或替代途径运行(图3)。健康、正常的产妇比非妊娠产妇具有更高的补体蛋白水平。虽然关于补体系统和子痫前期的研究得出了矛盾的结果,据推测,由于缺血或胎盘中的氧化应激,子痫前期患者会发生补体激活增大(特别是C3a和随后的终末途径激活)。
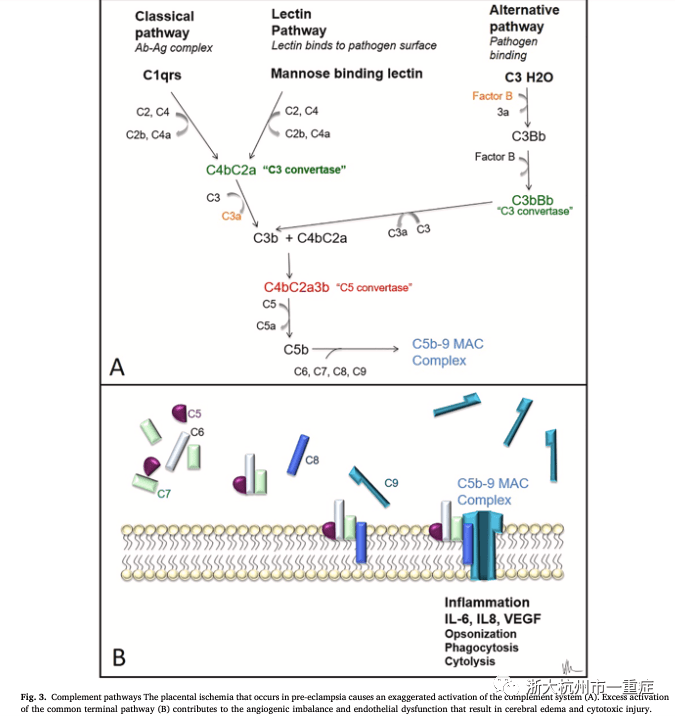
2015年Yallampalli等人的研究,在731名孕周15至26周之间进行羊膜穿刺术的妊娠妇女中,有2.4%患有早发型子痫前期。他们发现早发型子痫前期妇女羊水中C3a水平明显高于正常妊娠对照组的妇女。此外,子痫前期患者中补体因子B的水平升高。子痫前期中胎盘局部缺血引起的补体过度激活会触发胎盘损伤、抗血管生成因子产生和母体血管损伤的循环。子痫前期患者中补体激活的上调被认为可导致血管生成失衡、内皮损伤和胎盘功能不全恶化。
7.补体激活与血脑屏障
BBB通常可防止神经元暴露于过量的免疫调节因子(例如补体蛋白)。然而,为了响应应激信号,神经血管内皮细胞可能会成为补体启动剂的选择性靶点。补体介导的内皮损伤促进BBB渗漏,随后活性补体片段、细胞因子以及免疫细胞大量涌入受伤的脑组织。通过这种机制,子痫前期中的补体激活可能独立影响BBB的完整性,随后使补体激活产物进入大脑,这可能导致继发性脑水肿。补体蛋白一旦进入大脑,便能够改变神经元、小神经胶质细胞和少突胶质细胞的功能,如神经退行性疾病(如阿尔茨海默氏病、视神经脊髓炎和中风)的小鼠动物研究所证明的。尽管还需要进一步的研究,但初步研究表明,在动物中,阻断C3a受体的活化可显著改善子痫前期关键特征和相关的血管生成失衡以及缺血后损伤。
8.可逆性后部脑病综合征
可逆性后部脑病综合征(PRES)是一种临床和放射性综合征,与产科(子痫前期/子痫)和非产科患者的许多系统性疾病相关。PRES表现为头痛、视力障碍、癫痫发作和/或精神状态改变。人们认为,在内皮和BBB功能障碍的情况下,血压升高超过脑血管自动调节的上限并导致脑血管的强制血管舒张时,就会形成PRES。由于动脉和小动脉的大脑肌原性血管收缩受损,子痫前期患者在正常高压或正常压力下可能发生高灌注,从而使他们失去抵抗能力。
子痫前期/子痫伴PRES的典型急性神经影像学特征是继发于高灌注的后颅窝广泛性血管源性水肿,以及局灶性区域的细胞毒性水肿,最常见的是顶叶和枕叶。
9.神经影像学
正如不同患者的临床表现可能不同,PRES的影像学特征可以多变。但是,有一些关键的影像学特征与PRES的急性表现以及该综合征的长期后遗症有关。在成像方面,PRES的特征是白质和灰质异常,主要影响后部区域。主要发现通常是水肿——关于水肿是细胞毒性还是血管源性存在争议。交感神经神经源性反应负责补偿肌源性调节反应的任何恶化。交感神经系统在后循环中的作用不如其余脑血管系统重要,这解释了为什么后部容易受累。
弥散加权成像对大脑中水分子分布的变化敏感,其原理是高细胞组织或肿胀组织具有较低的扩散系数。水扩散越容易,初始T2信号就越少。结果,DWI可以区分血管源性水肿和细胞毒性水肿。
9.1磁共振成像(图4)
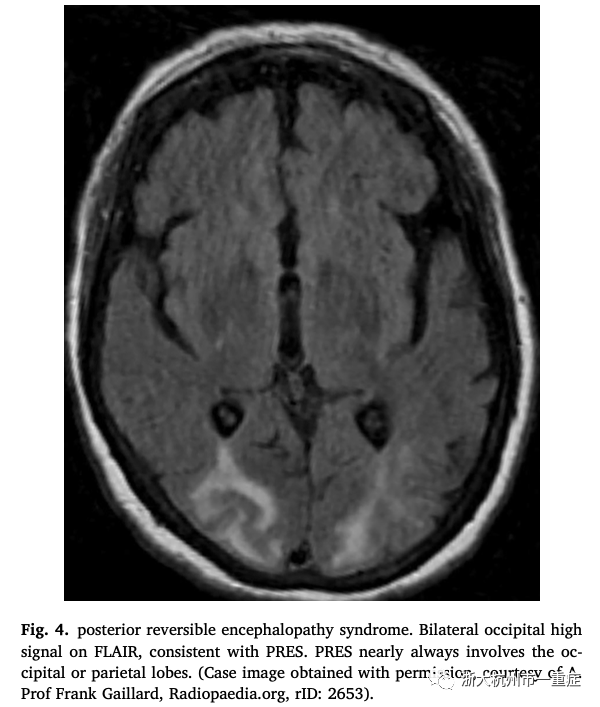
9.1.1 血管源性水肿
在MRI上,血管源性水肿在T2和FLAIR序列上表现为高信号。在T1上显示为等或低信号。没有证据表明血管源性水肿弥散受限。
9.1.2细胞毒性水肿
由于细胞因高灌注或低氧血症而受损,因此变得无法维持其ATP Na / K泵。这样,钠会在细胞内积聚,从而带走水。钠的这种流入导致细胞内肿胀,并且导致细胞外容积的减少。细胞外容积的这种减少限制了MRI上的弥散,并被视为DWI上的高信号和ADC上的低信号(表观扩散系数)。
9.2 CT检查
在CT上,PRES通常与水肿一致的弥漫性低密度区域相关。近100%的病例中可见顶叶或枕叶受累。
10.组织病理学
在产科文献中,已有子痫前期和子痫病史的患者描述了颞叶内侧硬化症。1973年对子痫患者的尸检分析还发现了点状脑皮层出血,尤其是枕叶出血。弥漫性脑水肿和大出血的发生率较低。脑静脉血栓形成在产后出现子痫的妇女中很常见。一项更现代的尸检研究(2017年)评估了Mozambique300例子痫造成的孕产妇死亡病例,发现了以下类型脑损伤及其发生率:血管周围水肿(68%)、出血(37%)、血铁血黄素(32%)、实质坏死(16%))和小血管血栓形成(11%)。
11.在临床实践中的应用
当前,通过评估非子痫前期的临床体征和症状,包括发生持续性头痛、视力障碍和上腹痛或右上腹痛,来确定发生子痫发作风险最高的患者。建议对所有诊断为具有严重特征的子痫前期患者进行高剂量的硫酸镁治疗(治疗范围4-7mEq/L),以预防围产期癫痫发作,同时应制定引产或剖宫产的计划。硫酸镁可将严重子痫前期患者的癫痫发作率从3.4%降低至0.3%,是该人群中最有效的抗癫痫药,但易使患者出现神经肌肉无力、低血压、子宫收缩乏力、产后出血、肺水肿和呼吸抑制。使用非特异性症状标准会导致因硫酸镁过度使用而引起的广泛并发症,以及与早期分娩有关的并发症。
我们相信,有强有力的分子学、解剖学和生理学证据表明,脑水肿是子痫前期和子痫的神经系统并发症的核心。如果我们接受这一前提,那么就可以使用颅内压的临床和亚临床升高(脑水肿的替代词)来识别高危女性,并最终以更个性化的方式进行干预。
11.1我们能否选择性地识别和治疗子痫和子痫前期风险最高的患者?
当前,用于识别ICP波动的方法成本高昂,具有侵入性或不可靠。这些方式包括神经影像学、脑室内导管和患者主诉的临床症状。
我们假设有发展神经系统症状风险的分娩会在头痛、视觉障碍和癫痫发作之前出现亚急性脑水肿。脑水肿反映在颅内压的波动中,尽管测量ICP的金标准是通过外部脑室引流(EVD)直接测量,但是这种设备的放置是侵入性的,其在子痫前期孕妇中的风险并未确定。在非孕妇患者中,CT扫描常被用作快速、非侵入性的手段来识别高ICP的病例,但是在子痫前期患者中,其成本、时间和辐射暴露也不合理。幸运的是,与CT相比,通过眼部超声检查测量视神经鞘管直径(ONSD)是安全、便宜、快速、易于传授的,且为颅内高压的检测提供了良好的诊断测试准确性。ONSD测量已被反复验证为评估非妊娠原发性颅内高压、外伤性脑损伤和颅内出血患者颅内压变化的工具,并且正在进行研究以验证妊娠的正常参考值。
识别高危患者的另一种非侵入性方法是使用产妇经颅大脑中动脉血流速度作为脑血管阻力的替代指标。这种评估脑血流动力学的方法在妊娠中具有公认的标准值,并且有合理的证据表明它可以在妊娠中期用于预测妊娠晚期子痫前期的发展。
11.2视神经鞘管直径
视神经与其鞘之间的空间与蛛网膜下腔连续,并充满脑脊液。在没有眶周病理的情况下,该空间中的压力等于ICP。视神经鞘被眼眶周围的脂肪包围,一项尸体研究发现其在视网膜后方3mm处最易扩张。尽管技术有所不同,但此时的扩张程度或视神经鞘管直径是通过眼眶超声测量的。最近的研究已确定了可以在与ONSD相同的超声视图中测量的另一个临床相关参数,称为视盘高度(ODH)。ODH可以代替乳头状水肿,但需要进一步研究它与子痫前期患者的神经系统症状相关。
尽管ONSD的参考值在妊娠中仍有待验证,但可以确定的是,尽管足月胎儿有腹胀,正常妊娠期间CSF压力仍保持不变。大量研究表明,子痫前期的妇女比单纯妊娠的妇女的ONSD升高具有统计学意义。目前公认的≥5.8mm的ONSD截断值与ICP升高> 20 mmHg的危险性有95%的关联,并已得到大量比较非妊娠神经重症患者侵入性监测和ONSD研究的证实。
11.3经颅多普勒超声
经颅多普勒超声检查用于评估大脑血管中的脑血流速度,最常见的是脑中动脉。MCA的测量是通过将2 MHz脉冲多普勒超声放置在经颅声学窗口上以可视化同侧MCA来获得的。ICP升高会阻碍脑部血流,从而降低血流速度,允许人们可以通过监测MCA速度的变化来识别ICP的亚临床升高。使用TCD的局限性包括需要大量训练,观察者之间和内部的差异以及在骨窗不足的患者中难以获得图像。
总结
围产期任何急性神经系统事件的发生都会对母亲和胎儿造成灾难性的后果。目前,所有有严重特征的子痫前期患者都使用硫酸镁治疗、积极的血压管理及在许多情况下及时终止妊娠。硫酸镁预防癫痫发作与母体的重大副作用有关,但是由于子痫发作的概率大大减少,因此可以接受这些并发症。
目前没有证据表明颅内压升高预示子痫,但是脑水肿对子痫前期和子痫的神经系统症状的发展至关重要。我们假设视神经鞘管直径、视盘高度和MCA经颅多普勒阻力指数所提示的ICP升高可以预测神经系统症状,因为它们可以识别脑水肿和血管异常。需要进一步的研究
评估这些方式是否可以用于诊断。其他潜在的干预目标包括生物制剂(即抗C3a抗体)对补体和炎症途径的调节。对这种疾病过程的病理生理学的更好理解是开发可靠研究工具和新治疗方法的关键。
本文荟萃自 杭州市一重症,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫