在前面几期“细胞死亡大盘点”系列推文中,小E分别给大家介绍了细胞凋亡、细胞自噬、细胞坏死、坏死性凋亡和细胞焦亡的相关内容,今天让我们一起来了解铁死亡的相关内容。
01
铁死亡的定义
铁死亡(Ferroptosis)是于2012年首次提出的一种由铁依赖的氧化损伤引起的调节性细胞死亡方式,铁死亡与肿瘤、代谢疾病,神经系统疾病、肾脏损伤等多种疾病的病理生理过程密切相关,是目前国自然基金研究的热点和焦点。
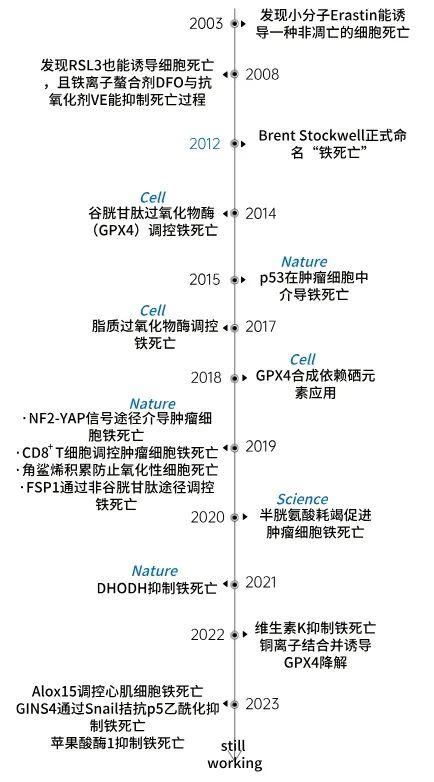
图1. 铁死亡的研究历程
02
铁死亡的发生
细胞内的亚铁含量增加,与H2O2发生芬顿反应,生成羟基自由基,羟基自由基氧化膜上的多不饱和脂肪酸,导致脂质过氧化,当细胞内的抗氧化系统被抑制时,无法清除过多的脂质过氧化和胞内活性氧,引起细胞膜损伤,最终诱导细胞发生铁死亡。
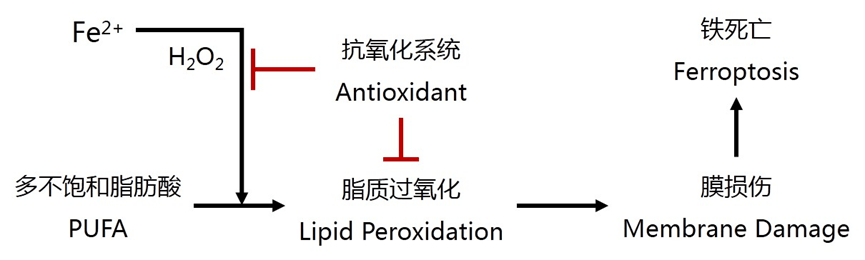
图2. 铁死亡的原理
03
铁死亡的调控
已有研究表明,铁死亡可以被多种代谢调控,涉及脂质、铁和氨基酸,谷胱甘肽等多种的代谢,可分为依赖于GPX4的代谢途径及独立于GPX4的调控途径。GPX4是还原毒性过氧化物的关键酶,通过其酶活性可防止脂质过氧化物的毒性,并保持膜脂双层的稳态,在铁死亡过程中扮演着关键的角色,GPX4活性受到阻碍时,脂质过氧化物累积并最终导致细胞死亡。
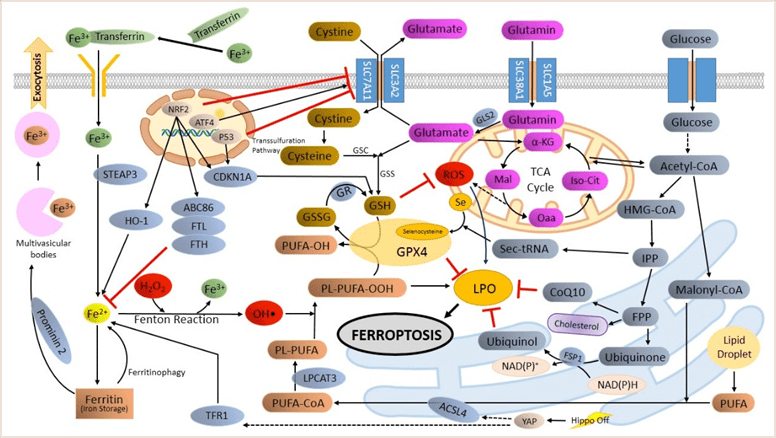
图3. 铁死亡简要通路图
04
铁死亡的特征
铁死亡是一种形态、生化、遗传上完全不同于凋亡、坏死和自噬的细胞死亡方式,铁死亡不能被细胞凋亡、细胞焦亡、细胞自噬的抑制剂抑制,却可以被铁螯合剂、抗氧化剂等抑制,因此铁死亡表现的主要特征是脂质活性氧增多及细胞内亚铁离子累积。
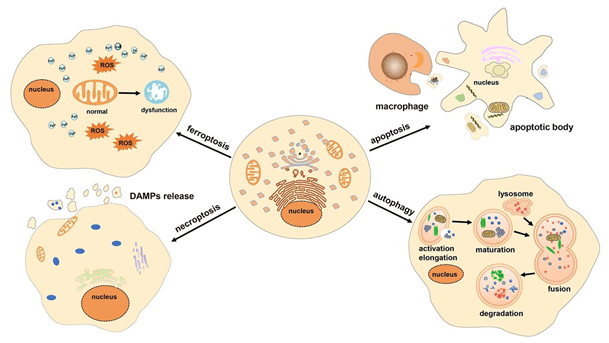
图4. 不同细胞死亡的独特形式及其形态学特征
在形态上,细胞发生铁死亡的主要特征体现在线粒体的形态变化上。过量铁负载引发的质膜过氧化会改变质膜的流动性和完整性,使线粒体外膜破裂,体积缩小,嵴减少或消失,导致线粒体功能缺失。
在代谢层面,铁死亡的过程除了细胞中铁和亚铁离子的积累和活性氧物质(ROS)的增加外,通常还伴随着谷胱甘肽代谢水平的降低及其他变化。
05
铁死亡的检测方式
铁死亡的判断与检测,可以通过四个方面进行检测:相关基因检测,相关蛋白检测,细胞形态检测,代谢检测。这些检测指标包括各个调控途径的关键基因及铁死亡的特征指标。
⋆
细胞形态检测:主要通过电镜检测线粒体的形态变化和细胞膜的完整性。
⋆
相关基因的检测:如GSH稳态调节基因、CHAC1的上调,NFE2L2基因的激活等。
⋆
相关蛋白的检测:如CHAC1蛋白的上升,GPX4蛋白的降低等;
⋆
相关代谢的检测:如细胞活性的变化,铁/亚铁离子的细胞内变化,ROS、过氧化氢等氧化物质的增加,脂质过氧化产物(如MDA、LPO等)的增加。
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫 


![[JAMA述评] 迈向个体化治疗:评估随机临床试验中疗效的异质性](https://www.icu.cn/wp-content/uploads/2023/05/2023-05-09_112937-480x300.gif)