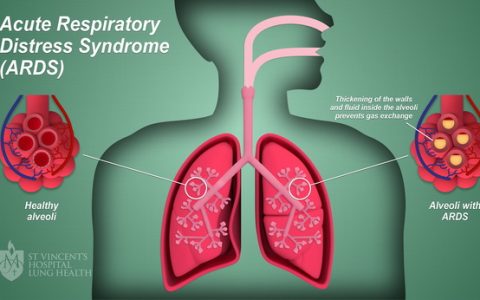
内毒素血症是一种由血液中或病灶内细菌释放大量内毒素至血液所引发的病理生理状态,可能引发多器官功能衰竭、不可逆休克甚至死亡。据全球统计数据显示,每年约有500万至700万患者罹患内毒素性脓毒性休克(endotoxic septic shock,ESS),其中超过半数患者死亡[1]。
随着医学研究的不断深入,人们对于其发病机制的认知日益加深,诊断技术和治疗手段也在不断完善。近年来,体外血液吸附作为一种非药物治疗方法在脓毒症治疗中逐渐受到关注。基础和临床研究均证实,对于脓毒症尤其是脓毒性休克等严重病症,体外吸附已成为一种积极有效的临床治疗选择。
内毒素性感染性休克的病理生理机制及临床表现
内毒素来自细菌毒素家族,是革兰氏阴性菌细胞壁外壁层上的特有结构,主要化学成分为脂多糖(LPS)。LPS是机体识别和调控内毒素的重要启动因子[1]:
LPS与脂多糖结合蛋白(LBP)结合,被运送到免疫细胞的膜表面,与蛋白质CD14相结合。CD14将LPS转运至Toll样受体4(TLR4)及髓样分化蛋白2(MD2)形成蛋白复合体。从而激活细胞内MyD88和TRIF依赖性通路,导致促炎细胞因子和I型干扰素(IFN)的产生和释放(图1中)。
炎症蛋白水解酶caspase4和5可识别细胞内内毒素,结合LPS后发生寡聚而活化,激活nlrp3炎症小体,直接导致线粒体功能障碍(图1左)。
LSP可激活补体系统产生过敏毒素(C3a和C5a),C3a可导致肥大细胞释放组胺,C5a可直接诱导nfkb通路介导的炎症(图1右)。
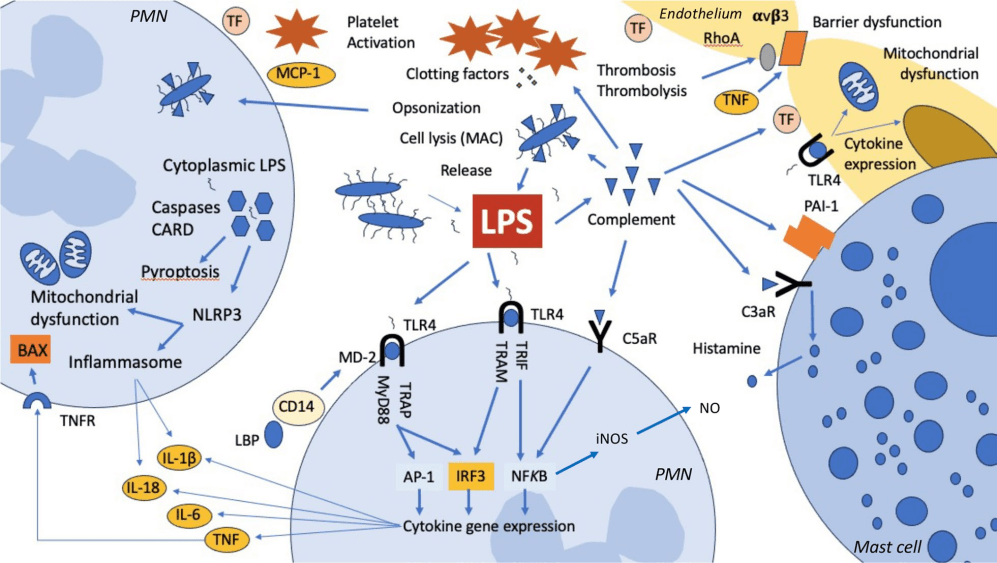
图1内毒素性脓毒性休克的病理生理机制(Kellum JA, et al. Crit Care. 2023 Oct 19;27(1):400.)
不同内毒素水平下,患者临床表现具有差异性。根据内毒素活性测定(EAA),临床通常将其分为三级:低水平(<0.30)、中等水平(0.30-0.60)和高水平(>0.60)。如图2所示,即使是较低的内毒素水平,也可能对机体的多个器官系统产生影响。处于中等内毒素水平时,可能诱发代谢综合征、动脉粥样硬化、关节炎等疾病。随着内毒素水平进一步升高,多器官功能衰竭的风险超过50%,其典型表现为肝功能障碍、急性肾损伤以及各种形式的内皮功能障碍(从弥散性血管内凝血到血栓性微血管病)等。若EAA值超过0.9,患者在恶性炎症状态下的死亡率可能超过80%[1]。
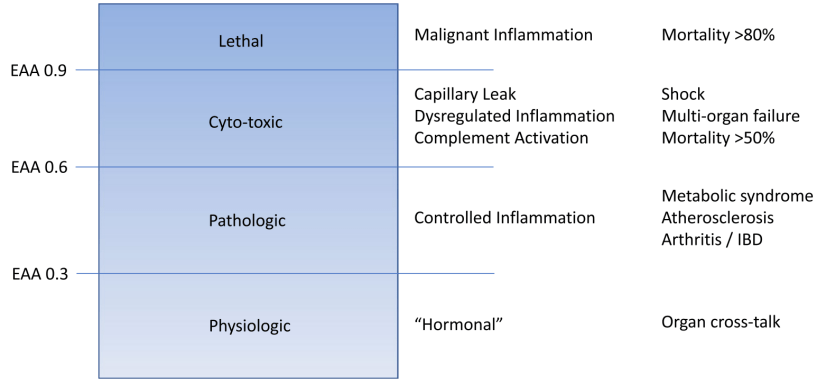
图2内毒素负荷与临床表现的关系
内毒素性脓毒性休克的诊断与临床表型
在脓毒症和脓毒性休克患者中,仅有高内毒素水平患者可从抗内毒素治疗中获益。因此,临床必须明确内毒素或其他刺激分子是否为脓毒性休克的主要驱动因素,以便实现精准治疗[1]。
由于ESS相关器官损伤缺乏特异性,临床仅凭临床表现难以区分ESS与低内毒素水平的脓毒性休克。建议结合内毒素活性测定(endotoxin activity assay,EAA)检测血液中的内毒素。当高内毒素活性(如EAA > 0.6)合并器官衰竭(如SOFA > 7),定义为ESS。但需注意的是,ESS患者内毒素负荷相同的情况下,其临床表现可能存在差异。如高内毒素活性患者可能无严重临床表现,也可出现急性器官衰竭,甚至死亡,这可能与脓毒症休克的表型差异有关[1]。
为进一步探究脓毒症表型差异,Seymour等人使用机器学习方法,通过不同的生物学和临床数据衍生并验证了关于脓毒症的四种临床表型(α、β、γ、δ)[2]:
α表型是最为常见的类型,占比33%。此类患者表现出较低的异常指标和器官功能障碍,同时病死率也相对较低。在治疗过程中,他们所需的升压药物剂量也最小。
β表型患者以老年人群为主,占比27%。他们往往伴随多种合并症,并且存在肾功能障碍的问题。对于这部分患者,临床治疗中需要特别关注肾功能的变化,如出现急性肾损伤(AKI)需及时采取相应的治疗措施。
γ表型患者的特点在于较高的炎症水平和呼吸功能障碍,占比同样为27%。这类患者的炎症指标明显升高,且存在呼吸功能受限的情况。因此,在治疗过程中,应重点关注抗感染治疗和呼吸支持措施。
δ表型占比最少,仅为13%,但其病死率却是最高的。这部分患者容易发生肝功能障碍及休克等严重并发症。因此,对于δ表型患者,应严密监测肝功能变化,并及时采取抗休克治疗措施。
总之,这四种表型在28d和365d的病死率上呈现出显著差异,并且炎症标志物的水平也存在明显不同。提示未来需要更多的大样本研究和临床实践,根据患者的具体表型特点,制定个性化的治疗方案,以提高治疗效果和患者生存率。
内毒素性脓毒性休克的血液吸附疗法
体外血液吸附技术是指在体外循环中,通过范德华力、静电和(或)疏水键等相互作用,实现对炎症因子、细胞因子以及内毒素的特异性或非特异性吸附。相较于传统的血液透析和血液滤过,血液吸附技术在清除大、中分子及脂溶性物质方面展现出更高的效能[3]。
理论上,通过吸附治疗迅速移除血液中的脓毒症相关溶质分子,可能有效地中断炎症级联反应,恢复促炎与抗炎细胞因子之间的生理平衡,从而遏制疾病的进展。迄今为止,已经研发出多种基于不同作用机制的体外血液吸附装置,主要包括多黏菌素B 吸附柱(PMX)和吸附型oXiris血液净化过滤器[3]。PMX吸附柱通过灌流吸附内毒素[3],而新一代吸附型oXiris血液净化过滤器集支持肾脏功能、清除炎症因子、吸附内毒素和局部抗凝4种功能于一体[4]。2018年EUPHRATES试验[5]表明,内毒素水平升高(EAA>0.6)的脓毒症患者应用PMX血液灌流并未见显著终点获益。那么,功能更为全面的吸附型滤器oXiris,是否能成为更有效的脓毒症治疗方法呢[3]?
2019年,一项随机对照试验(RCT)[6]评估oXiris滤器在脓毒症合并急性肾损伤(AKI)患者24h治疗期间对内毒素和细胞因子水平的调控作用,并与标准过滤器进行对比分析。研究结果显示,oXiris组患者的内毒素水平相较于标准过滤器组显著降低(图3)。此外,在接受治疗的初始24小时内,oXiris组患者的血乳酸水平出现明显下降,而去甲肾上腺素(NE)的用量也在治疗后的4小时内有所减少。这些发现为oXiris过滤器在脓毒症合并AKI治疗中的应用提供了有力支持,提示oXiris滤器清除内毒素和细胞因子的同时可以改善血流动力学状态。
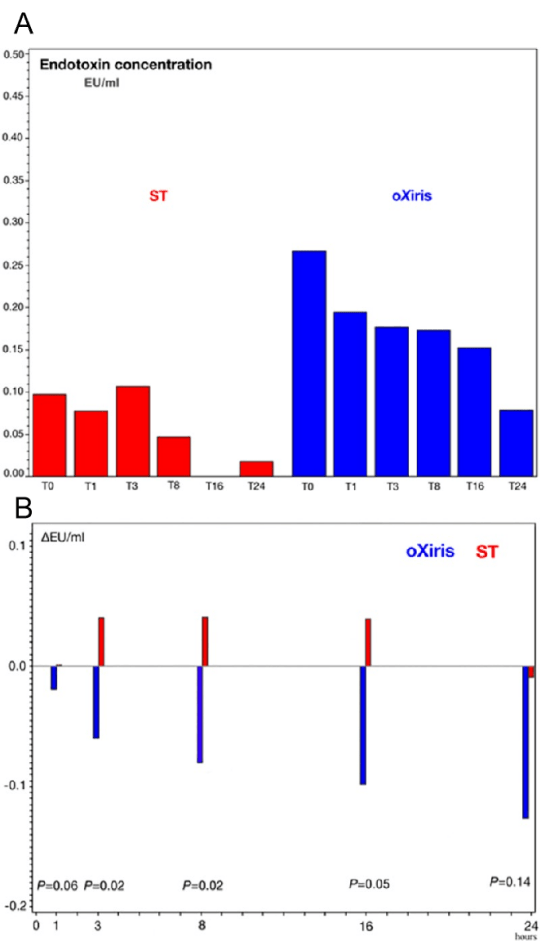
图3 24h治疗期间内毒素浓度变化
注:图A为每个时间点的中位内毒素浓度,图B为内毒素水平的绝对平均变化
2023年,一项纳入695例接受CRRT的脓毒症患者的荟萃分析表明[7],相较于其他滤器(AN69-ST、M100、M150),采用oXiris滤器进行治疗能够有效降低患者在接受治疗后的7天、14天及28天的死亡率。此外,该治疗方法还能显著改善患者的SOFA评分,明显减少NE的使用量,降低乳酸水平和白细胞介素-6(IL-6)的水平。同时,患者ICU治疗天数也显著缩短(图4)。
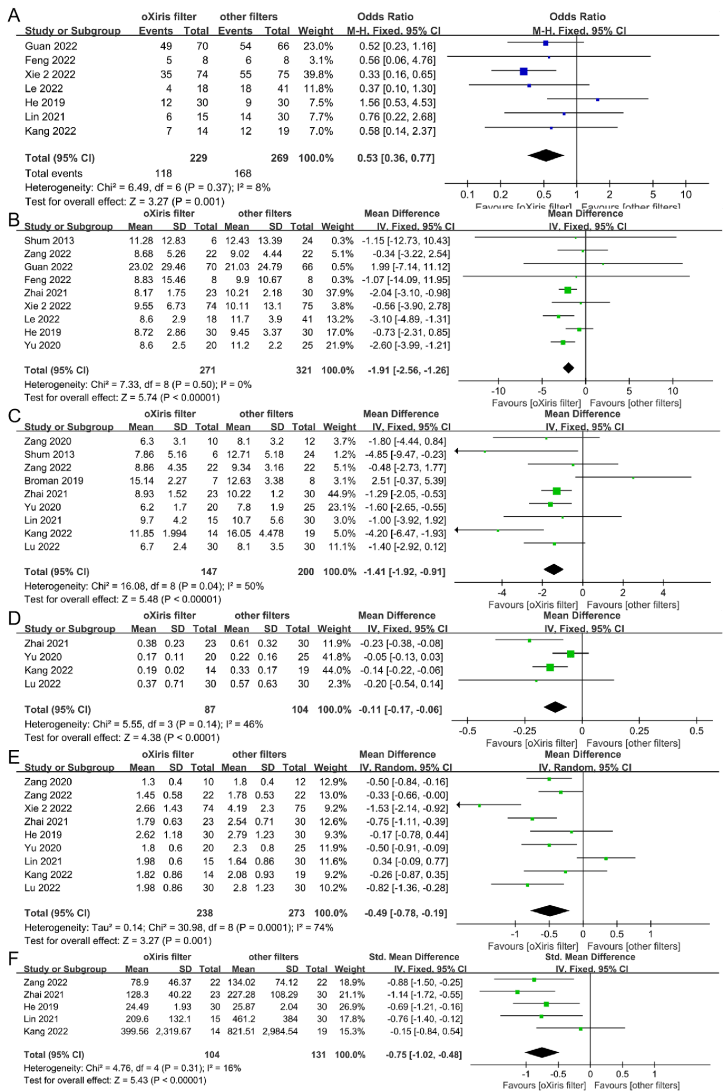
图4 研究结果
注:图A:28天死亡率;图B:ICU治疗时间;图C:SOFA评分;图D:去甲肾上腺素(NE)用量;图E:乳酸水平;图F:白细胞介素-6(IL-6)水平
小结
ESS作为脓毒症的一种亚型,治疗重点集中于抗生素应用、感染源控制及支持性疗法。此外,体外血液吸附等新型血液净化技术,在特异性针对脓毒症内毒素的清除以及血流动力学参数的改善方面,已展现出一定的积极效果。然而,这些技术的具体作用机制、适应症以及确切的临床益处,仍需我们进行更为深入和系统的研究与验证。
参考文献
[1] Kellum JA, Ronco C. The role of endotoxin in septic shock. Crit Care. 2023 Oct 19;27(1):400.
[2] Seymour CW, Kennedy JN, Wang S, et al.Derivation, Validation, and Potential Treatment Implications of Novel Clinical Phenotypes for Sepsis. JAMA. 2019 May 28;321(20):2003-2017.
[3]丁朔,黄曼.体外血液吸附治疗脓毒症的研究进展[J].中华急诊医学杂志,2023,32(4):574-576.
[4] Hellman T, Uusalo P, Järvisalo MJ. Renal Replacement Techniques in Septic Shock. Int J Mol Sci. 2021 Sep 23;22(19):10238.
[5] Dellinger RP, Bagshaw SM, Antonelli M, et al. Effect of Targeted Polymyxin B Hemoperfusion on 28-Day Mortality in Patients With Septic Shock and Elevated Endotoxin Level: The EUPHRATES Randomized Clinical Trial. JAMA. 2018 Oct 9;320(14):1455-1463.
[6] Broman ME, Hansson F, Vincent JL, et al. Endotoxin and cytokine reducing properties of the oXiris membrane in patients with septic shock: A randomized crossover double-blind study[J]. PLoS One, 2019, 14(8):e0220444.
[7] Wang G, He Y, Guo Q, et al. Continuous renal replacement therapy with the adsorptive oxiris filter may be associated with the lower 28-day mortality in sepsis: A systematic review and meta-analysis [J]. Crit Care, 2023,27(1):275.
本文荟萃自公众号:百特重症医学频道,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫