急性肾损伤 (acute kidney injury, AKI) 是围手术期一种常见并发症,无疑对患者是雪上加霜,严重影响患者预后甚至危及生命。本文将带领大家了解一下围手术期AKI的现状,包括定义及诊断、发病率及危害、发病机制及危险因素、现今应对策略等4个方面的最新进展。
1、围手术期AKI定义及诊断
围手术期AKI主要是指在围手术期发生的AKI,是一种以急性肾小球滤过率丢失为主要特点的临床综合征。目前AKI的诊断和临床分期主要基于血清肌酐升高和尿量减少,常用的AKI诊断标准有危险,损伤,衰竭,功能丧失,终末期肾病 (Risk, Injury, Failure, Loss of kidney function, End-stage renal failure, RIFLE) (2004)、急性肾损伤网络工作组(Acute Kidney Injury Network, AKIN) (2007)、改善全球肾脏预后组织 (Kidney Disease: Improving Global Outcomes, KDIGO) (2012) (图1),目前KIDIGO诊断标准在临床应用比较广泛 [1]。
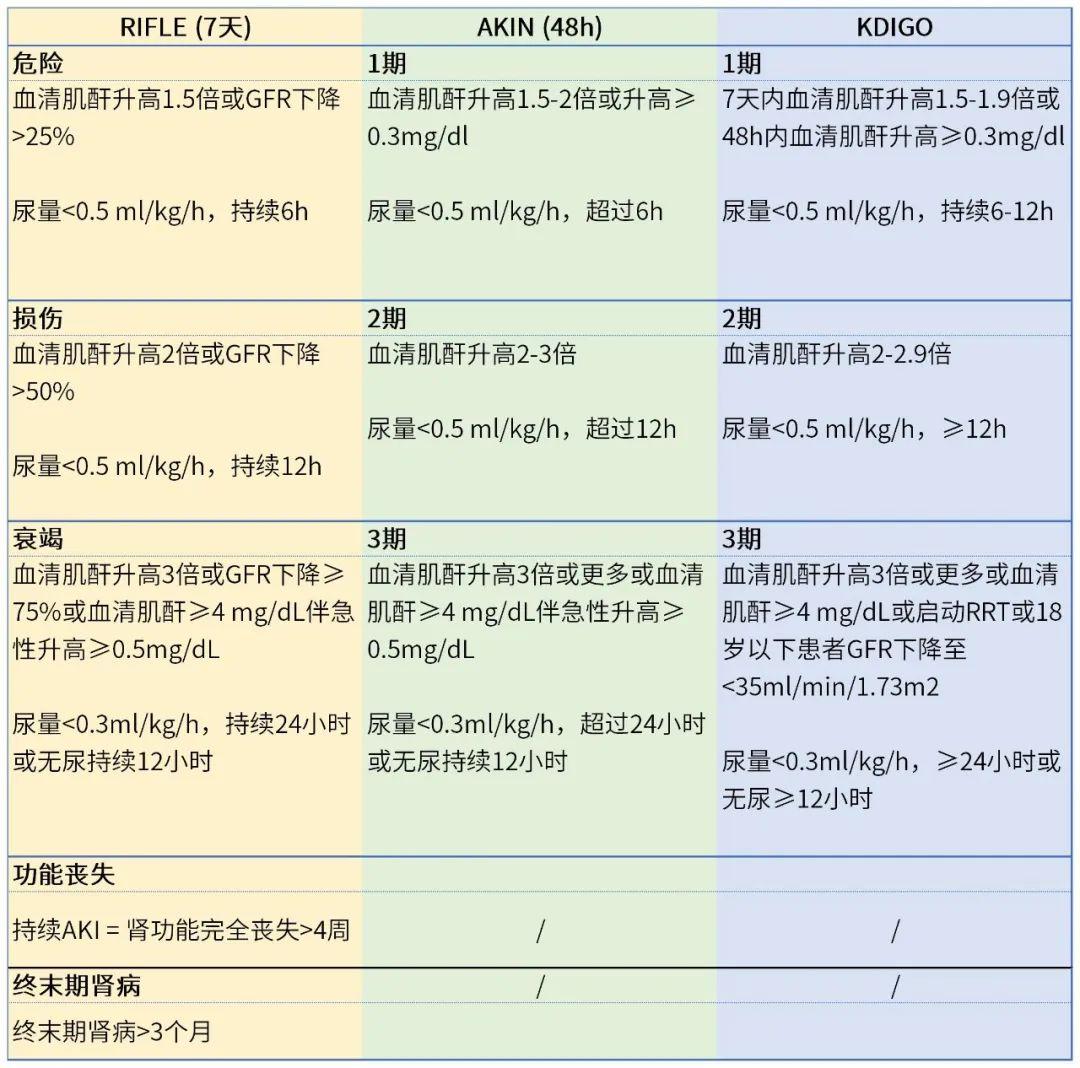
图1:AKI诊断及分期标准[1]
2、围手术期AKI发病率及危害
AKI并非一种少见的围手术期并发症,术后期间AKI尤为突出,高风险人群发病率在20%~40%[1]。体外循环下心脏手术发生AKI的风险最高,其次为普外科、胸外科、骨科、血管外科和泌尿外科[2]。相关研究数据表明,围手术期AKI总发病率约为6%。而在心脏手术患者中,其发病率高达25%~30%[1]。一项纳入32万心脏术后患者AKI情况的研究显示,AKI发生率为22.3%,需要肾脏替代治疗 (renal replacement therapy, RRT) 的比例为2.3%[3]。
围手术期AKI与患者的预后密切相关,越来越多的证据表明AKI直接导致心、肺、脑、肝、免疫和其他器官系统的远程器官损伤[1],患者的住院天数、医疗支出及病死率增加。一项关于术后AKI流行病学的国际前瞻性、观察性、多中心研究 (N=10568) 数据显示,与术后未发生AKI的患者相比,术后AKI患者的ICU死亡率 (6.3% vs 0.7%) 和住院死亡率 (8.6% vs 1.4%) 更高,且中位ICU住院时间 (3 vs 2天) 和中位住院时间 (14 vs 10天) 更长[4]。一项单中心研究中回顾性分析39369例手术患者,发现即使轻度AKI也会带来显著的死亡风险,并增加住院时间[5]。
近期发表的一项关于我国患者术后AKI的发病率、危险因素和预后情况的回顾性研究,共纳入520707例手术患者 (数据涵盖10个省份的16家三甲医院),总计25830例 (5%) 患者发生了AKI,AKI 1期、2期和3期的占比分别为77.3%、15.4%和7.3%,其中AKI发生风险最高的是心脏手术 (34.6%)。AKI 3期患者中,仅859例 (52.8%) 患者的肾功能恢复正常。1025例 (4.0%) 术后AKI患者在住院期间死亡,且随着AKI分期的增加,患者院内死亡风险显著增加 (图2)[6]。此外,与未发生AKI的术后患者相比,发生AKI的患者其住院时间更长(12 vs 19天)、费用更高(38,000元 vs 82,000元),更容易接受ICU治疗(13.1% vs 45.0%),更容易接受RRT(0.4% vs 7.7%)[6]。
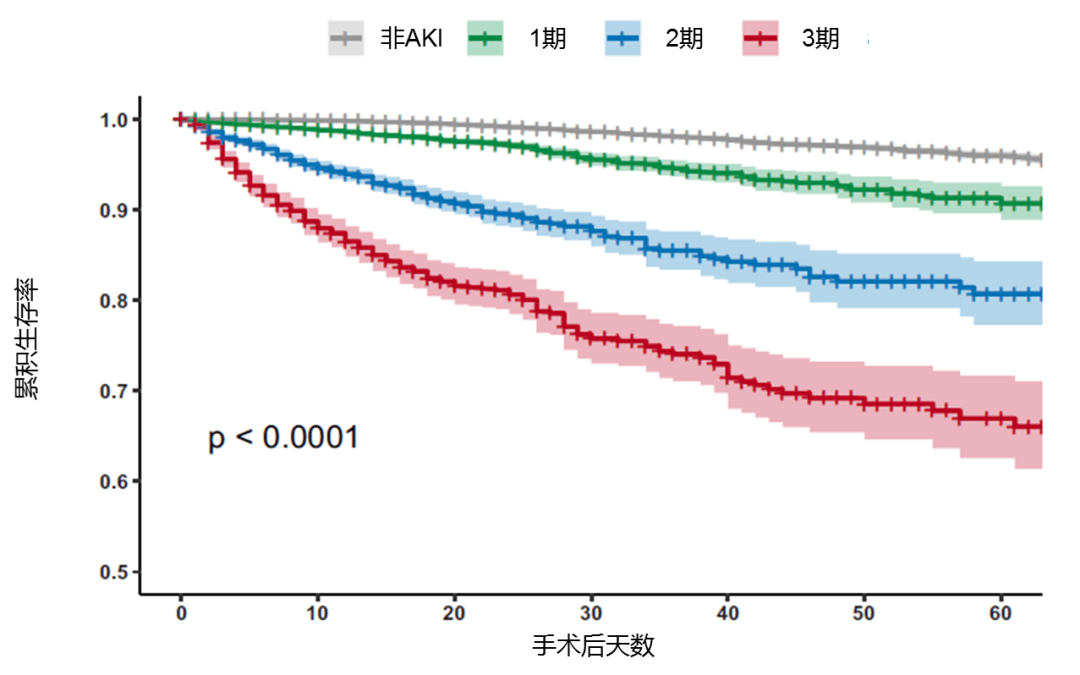
图2:AKI不同分期患者的院内累积生存率[6]
3、围手术期AKI发生机制及危险因素
围手术期AKI的病因往往是复杂的,多因素的。其发生机制通常涉及缺血-再灌注损伤,内源性或外源性肾毒素,物理原因如梗阻、炎症因子、血管收缩和氧化应激等。术前有CKD (Chronic Kidney Disease, 慢性肾脏病) 病史是发生AKI的主要危险因素,其风险高达10倍[2]。在大多数情况下,术前、术中和术后危险因素的综合作用导致了AKI的发生,涉及患者相关因素和手术相关因素 (图3) [2,7]。
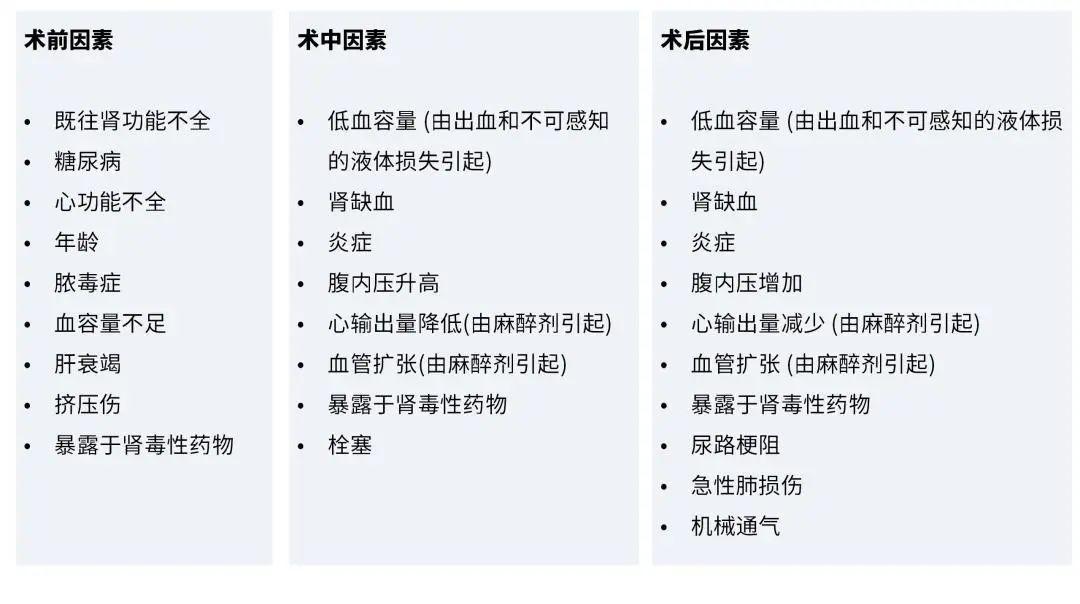
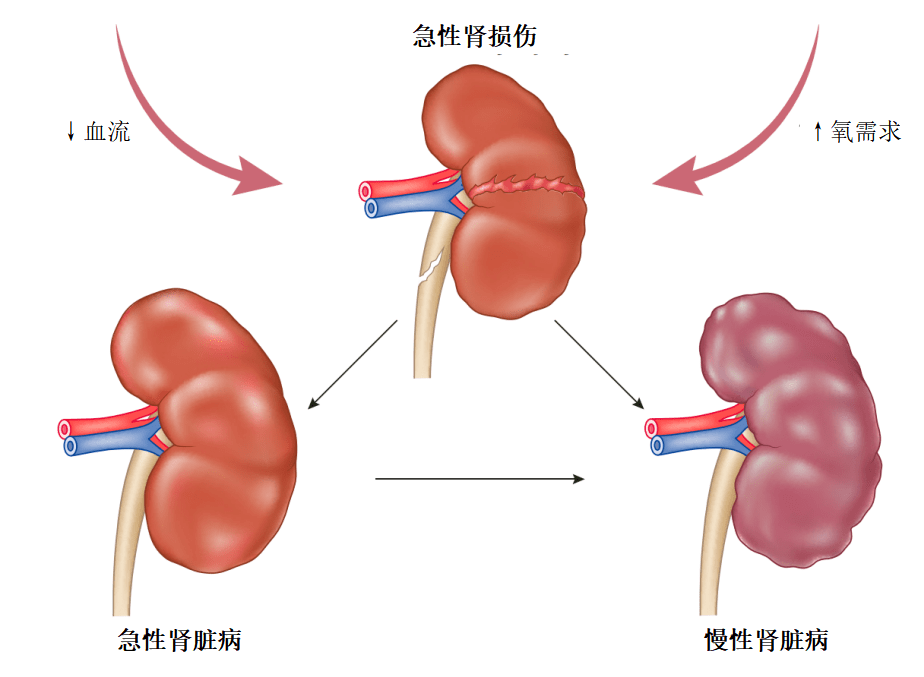
图3:围手术期AKI病理生理学[7]
4、围手术期AKI预防与治疗
KDIGO“集束化治疗”:预防围手术期AKI
AKI是近期和远期不良结局的预测因子,临床管理的核心还是在于围手术期AKI的预防。KDIGO指南鼓励在高危患者中使用预防策略并提出一系列预防AKI的措施,主要包括[8]:
-
早期发现AKI,可以使用肾损伤标志物 (NGAL、KIM-1等) 结合传统评估肾功能的肌酐进行诊断,更好地发现亚临床的AKI
-
围术期血流动力学监测与调控
-
监测血肌酐和尿量
-
保证容量和灌注压
-
停用或者避免肾毒性的药物
-
维持血糖平稳
-
尽量避免使用造影剂
必要时采取治疗:RRT是目前治疗严重AKI的唯一选择
即便做了预防,围手术期AKI的发生有时也是不可避免的。必要时需启动RRT,KDIGO指南推荐[8]:当出现危及生命的容量、电解质及酸碱平衡紊乱时,紧急开始RRT。在决定开始RRT时,需要考虑整体的临床情况、可以通过RRT纠正的问题以及实验室检查结果的变化趋势,而不仅仅关注肌酐及尿素氮的变化。
关于RRT的模式选择 (连续性 vs. 间歇性) 仍存在争议。由于连续性肾脏替代治疗 (Continuous Renal Replacement Therapy, CRRT) 可使血液溶质浓度及容量变化对机体的影响降到最低,具有血流动力学稳定,持续稳定的维持水、电解质和酸碱平衡,清除炎症介质等优点。此外,有研究表明,与CRRT相比,间歇性血透不利于肾功能恢复,增加长期透析依赖的风险[9]。KDIGO指南推荐[8]:对于血流动力学不稳定的AKI患者,建议使用CRRT,而不是间歇性RRT。
我国心脏外科手术期CRRT专家共识指出[10]:心脏手术相关急性肾损伤(cardiac surgery associated⁃acute kidney injury,CSA⁃AKI)是心脏手术后常见的严重并发症,CRRT在肾功能未恢复之前可避免严重并发症的发生,如代谢性酸中毒、高钾血症,容量超负荷等。对于心脏外科术后患者而言,血流动力学变化十分迅速,需要进行CRRT介入的时机要早于KDIGO 3级。
心脏外科CSA⁃AKI 启动CRRT应用指征:
-
容量超负荷,尿量<0.5ml/kg/h连续6h伴或不伴利尿剂抵抗时,考虑开始CRRT治疗
-
患者严重代谢性酸中毒,持续pH值<7.2,剩余碱<-8mmoL/L时,可考虑开始CRRT治疗
-
患者血清肌酐值处于KDIGO 2级 (血清肌酐值较基线水平增加2-2.9倍) 时,可考虑开始CRRT治疗
-
血钾>6.0mmol/L且对胰岛素和利尿治疗不敏感时,应考虑给予CRRT治疗
-
横纹肌溶解造成的高肌红蛋白血症合并筋膜间隙综合征,及时给予CRRT治疗可减少多器官功能障碍综合征的发生,尤其是急性肾功能不全
-
低心排出量综合征导致肾功能不全利尿剂抵抗时行CRRT治疗
-
心脏外科术后急性肾损伤患者肾脏替代治疗时机的选择,应充分评估患者内环境状态,综合分析血清电解质 (高钾血症及严重的高钠血症)、酸碱平衡、渗透压、液体容量及心脏功能和代谢产物水平等,做到个体化治疗。不必满足所有条件才启动CRRT治疗,而是分析患者迫切需要解决的问题,选择恰当时机开始CRRT治疗
心脏外科CSA⁃AKI CRRT应用要点:
-
对目标静脉进行穿刺置管时,推荐超声引导下完成操作
-
股静脉可为心外科术后CRRT通路的首选静脉,右侧颈内静脉为次选静脉
-
连续性静脉-静脉血液透析滤过 (continuousvenovenous hemodiafiltration, CVVHDF) 模式对于血流动力学欠稳定的CSA⁃AKI患者更具有治疗价值
-
枸橼酸局部抗凝是无枸橼酸抗凝禁忌证患者进行CRRT治疗的首选抗凝方案
-
对于存在枸橼酸局部抗凝禁忌证者,可采用肝素、阿加曲班等进行全身抗凝,应用之前要充分评估患者出血风险
-
25~35ml/ (kg·h) 的剂量对于CSA-AKI患者较为合适
-
临床需短时间达到滤过效果,推荐采用后稀释法;为延长滤器寿命,推荐采用前稀释法
-
患者循环稳定、血管活性药量不大、电解质酸碱平衡稳定、无严重感染的证据,筋膜间隙综合征得到控制时肌红蛋白下降至正常范围,每日尿量>500ml,可终止CRRT
围手术期AKI属于高发、高危的并发症,尤其心脏手术术后患者发生AKI的风险最高。其与患者不良的短期和长期预后息息相关,目前围手术期AKI的预防仍是应对策略的关键,当发生严重AKI时,RRT是医生的唯一武器,助力化险为夷。对于血流动力学不稳定的AKI患者,国内外权威指南推荐启动CRRT以支持患者转危为安。
参考文献
-
Gumbert SD, et al. Anesthesiology. 2020 Jan;132(1):180-204.
-
Gomelsky A, et al. Best Pract Res Clin Anaesthesiol. 2020 Jun;34(2):167-182
-
Hu JC, et al. J Cardiothorac Vasc Anesth. 2016 Jan;30(1):82-9.
-
Zarbock A, et al. Intensive Care Med. 2023 Dec;49(12):1441-1455.
-
Kork F, et al. Anesthesiology 2015; 123:1301–11.
-
Cheng Y, et al. Nephrol Dial Transplant. 2024 Jan 23:gfad260.
-
Boyer N, et al. Clin J Am Soc Nephrol. 2022 Oct;17(10):1535-1545.
-
Khwaja A. Nephron Clin Pract. 2012;120(4):c179-84.
-
Wald R, et al. Intensive Care Med. 2023 Nov;49(11):1305-1316.
-
中国心脏重症连续性肾脏替代治疗专家共识工作组. 中华医学杂志. 2019; 99 (5): 321-328.
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫