吸入是将口咽或胃内容物吸入喉部、气管支气管和下呼吸道。吸入性肺部炎症是因吸入无菌胃内容物而引起的化学损伤;而吸入性肺部感染是指吸入由致病细菌定植的口咽分泌物而引起的感染过程。这2种吸入性肺炎存在重叠,都可引起肺损伤[1-2],严重者导致低氧血症或ARDS[3]。临床上以吸入胃内容物引起的吸入性肺炎较多见,也可见于误吸煤油、汽油、挥发性气体、干洗剂、溺水等。吸入性肺炎在社区获得性肺炎(community-acquired pneumonia,CAP)中的占比约为5%~15%,而在医院获得性肺炎中所占比例不清楚[1]。老年人反应差,易发生吸入性肺炎,约占老年CAP的71%[4]。
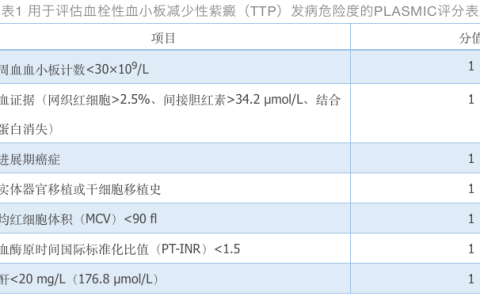
仅从临床表现上难以区分吸入性肺炎诱发途径是空气途径还是口腔途径,使用纤维支气管镜检查看到食物颗粒或胃内容物有助于确诊。目前各国肺炎临床指南中,CAP、医院获得性肺炎及健康护理相关肺炎略有涉及吸入性肺炎的内容,然而缺乏深入阐述吸入性肺炎的诊断和治疗。鉴于吸入性肺炎的诊治与其独特的发病机制、危险因素、感染时微生物特征、疾病管理等密切相关。为此,成人吸入性肺炎诊断和治疗专家组查阅国内外相关文献资料,参照美国感染病学/美国胸科学会相关指南,制定证据等级和推荐等级(表1),同时结合我国具体国情,就吸入性肺炎进行专题研讨并达成临床建议,为临床医师诊断和治疗吸入性肺炎提供指导和参考。
流行病学
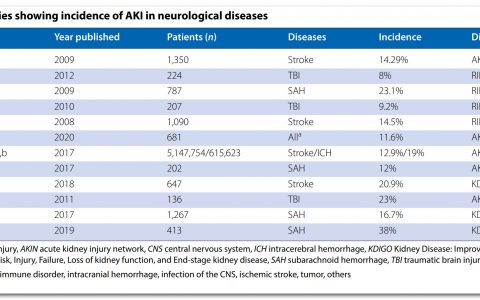
我国目前尚无关于吸入性肺炎发病率和病死率的大样本、多中心研究数据。2014年和2016年国内2项单中心研究显示,年龄≥60岁和年龄≥55岁老年住院患者中,吸入性肺炎的发病率分别为13.4%和14.0%[5]。日本单中心大样本研究显示,2010-2015年吸入性肺炎的发病率为67.2/万人,病死率为13.6%[6]。韩国单中心回顾性研究显示,吸入性肺炎患者的1年、3年、5年病死率分别为49.0%、67.1%、76.9%[7]。即使数据通过校正,吸入性肺炎的病死率仍比其他形式的肺炎高[8]。
随着患者年龄增加,吸入性肺炎的发病率增加显著。美国2002-2012年吸入性肺炎住院患者为406 798例,其中年龄<65岁的吸入性肺炎患者占20.7%,≥65岁患者占79.3%[9]。西班牙2003—2013年≥75岁人群中吸入性肺炎的发病率从19.0/万人升高至34.7/万人,其中75~84、85~94及>94岁人群吸入性肺炎发病率分别为16.0/万人、56.9/万人和108.0/万人[10]。此外,我国脑卒中患者7 d内下呼吸道感染的发病率约为7%~38%,导致卒中患者死亡风险增加3倍[11]。
危险因素
正常人由于会厌和声门保护性反射及吞咽的协同作用,食物和异物不易进入下呼吸道,少量液体能通过咳嗽排出。误吸后立即出现刺激性呛咳、气急甚至哮喘,称为显性误吸;若当时(>1 min)无咳嗽、气急、呼吸困难等症状体征,称为隐性误吸,易被忽视、漏诊[12]。
意识障碍、吞咽困难、咳嗽反射受损、胃食管反流或留置鼻胃管/鼻肠管等是误吸常见的危险因素。当神经系统病变或意识障碍时,如假性延髓性麻痹、脑血管疾病、癫痫发作、帕金森病、痴呆、药物毒品滥用(如镇静剂、麻醉药、某些抗抑郁药和酒精等)导致吞咽困难或声门关闭不协调、咳嗽反射受到抑制,异物或食物易被吸入气道。呼吸衰竭、ARDS、重症肌无力等引起的咳嗽反射受损导致呼吸道内异物或分泌物排出困难,合并呼吸道感染时可使疾病加重,表现为PaO2下降和/或PaCO2升高。胃食管反流病变,如食管失弛缓症、反流性食管炎、食管上段肿瘤、食管憩室、胃溃疡等导致食物不能全部入胃并反流进入气管;肿瘤或外伤引起的食管-气管瘘导致食物经食管直接进入气管内。医源性因素,如留置鼻胃管/鼻肠管、气管插管或气管切开等刺激咽部引起呕吐或影响喉功能抑制正常咽部运动可将呕吐物吸入气道[13-23]。另外,口腔疾病,如龋齿、牙周炎、牙龈炎,来自口腔、咽部含有细菌的分泌物在喉头反射迟钝、消化道蠕动减慢、食管肌肉松弛时易被吸入气道[24-25]。隐匿性吸入性肺炎的发生通常由于口腔内的病原体在睡眠中随唾液、痰液、食物残渣一起吸入气道[26]。具有多重吸入风险的患者,其不良后果的发生率和病死率增加[2](ⅡB)。
睡眠中吸入少量口咽部分泌物是正常的[27-28]。研究表明高达45%的健康成年人睡眠时伴有(误)吸入[29]。然而,发生上气道的正常防护功能减退或损害时,如声门闭合异常、吞咽功能失调和咳嗽反射减弱有可能导致吸入量和发生频率增加。吸入含特定微生物的口咽部或上消化道内容物至气道或肺实质是吸入性肺炎的必要条件[28],误吸无菌性胃内容物后易引起急性化学性肺损伤,其病程早期为无菌性炎症,随后可合并有细菌感染[2]。
病原学特点
与之前”肺无菌”的认知相悖,微生物组学研究揭示了肺部微生物的多样性,细菌可吸入并定植在肺脏[30-32]。在健康人群,微生物在口腔的不同部位定居,如牙龈、牙菌斑和舌头。肺微生物群的稳定性通过外来菌群的移居和清除维持[33]。外来菌群移入主要通过口咽部的微吸入,清除则通过纤毛运动和咳嗽[34]。疾病可导致肺微生物群失稳态,尤其在清除功能受损时,如患者意识障碍或咳嗽反射抑制,肺脏的微生物移居-清除失衡,细胞表面纤维连接蛋白破坏并暴露气道上皮细胞下层的革兰阴性杆菌受体致使感染风险增加[35](ⅡB)。
既往也有学者认为,误吸时咽部定植菌可被带入肺内,引起厌氧菌感染为主的继发性细菌感染,形成肺脓肿[24-25]。然近年来研究显示,吸入性肺炎厌氧菌感染的概率不高[36]。社区获得性病例中主要分离到肺炎链球菌、金黄色葡萄球菌、流感嗜血杆菌和肠杆菌,而医院获得性病例中主要分离到革兰阴性杆菌,如铜绿假单胞菌,未见到厌氧菌。在呼吸机相关肺炎病例中只有1例为厌氧菌感染[37]。目前对吸入性肺炎病原菌变化的原因尚未知,可能与发病人群和采样时间不同有一定关系[1,38](ⅡC)。
病理生理
吸入胃内容物后,胃酸刺激支气管引起强烈的支气管痉挛、支气管上皮细胞的急性炎症反应和支气管周围的炎症细胞浸润;进入肺泡的胃液向周围肺组织扩散,肺泡上皮细胞损伤并累及毛细血管,血管通透性增加、肺泡-毛细血管屏障破坏,逐渐形成间质性肺水肿、肺泡水肿。胃酸吸入引起的上皮和内皮破坏激活炎性细胞,如肺泡巨噬细胞和中性粒细胞等,释放大量炎症介质,包括IL-8、肿瘤坏死因子α、巨噬细胞炎症蛋白2和中性粒细胞趋化因子1等,并与受损细胞膜相互作用产生大量自由基、过氧化物、蛋白酶等。中性粒细胞和补体在肺损伤的发展中起着关键作用[3]。在胃酸合并胃内容物吸入性肺损伤的动物研究显示,IL-10和单核细胞趋化蛋白1水平在肺泡灌洗液中是升高的,且与肺损伤严重程度有关。然而,迄今尚无吸入性肺炎患者肺泡灌洗液或血清学相关数据[3]。
肺水肿导致肺顺应性降低、肺容量减少、肺泡Ⅱ型上皮细胞损伤、表面活性物质生成减少、小气道陷闭、肺泡萎陷、肺不张。肺泡通气不足导致通气/血流比例失调、动静脉分流增加,出现低氧血症。血管内液体大量渗出或反射性血管扩张,当血容量减少35%以上,易发生低血容量性低血压。随后,肺泡水肿和出血逐渐吸收,纤维母细胞增生,肺纤维化[3]。吸入碳氢化合物的病理生理过程与胃酸吸入相仿,因其表面张力低,吸入后可在肺内迅速扩散,使肺泡表面物质失活,更易产生肺不张、肺水肿、严重的低氧血症。吸入物含固体颗粒时,可阻塞气道,引起肺不张,导致阻塞性肺炎[39]。
临床特征
吸入性肺炎患者临床表现各异,既可以表现为无症状,又可以表现为严重的ARDS。此类患者常合并误吸的高危因素。吸入呕吐物后可突发喉反射性痉挛和支气管刺激发生喘鸣、剧咳。吸入大量低pH胃酸或大量胃内容物时,引起严重的肺组织损伤,表现为突发呼吸困难、心动过速。呼吸困难通常早于影像学表现,随着缺氧和临床症状加重,影像学表现可更显著。查体可闻及两肺哮鸣音和湿啰音,有低氧血症,严重时可伴有二氧化碳潴留和代谢性酸中毒[1,26]。吸入性肺炎进展为ARDS的概率约为16.5%,若合并休克、创伤或胰腺炎则发生ARDS的风险增加[40]。食管-支气管瘘引起的吸入性肺炎患者每天进食后有痉挛性咳嗽伴气喘。意识障碍患者吸入后常无明显症状,但在1~2 h后可突发呼吸困难,发绀,咳出浆液性泡沫样痰,可带血。吸入性肺炎通常为急性发病,症状在误吸后数小时到数天内发生。合并厌氧菌感染时,因厌氧菌毒力偏弱,症状常呈现亚急性。
高龄老年吸入性肺炎患者可表现为高钠血症和肾小球滤过率降低,更多的进展为重症肺炎,其病死率要高于非吸入性肺炎[41]。吸入性肺炎的病死率高于其他类型的CAP可能与医院的诊断编码不恰当有关[8]。
吸入性肺炎患者血常规中白细胞计数常常增高且伴核左移。降钙素原、α-淀粉酶等生物标志物在吸入性肺炎诊断中的作用尚未证实[42-43](ⅡB)。动脉血气分析常提示低氧血症。影像学的肺内病变分布与吸入时体位有关[44],早期表现可能为阴性,典型表现为两肺散在不规则片状边缘模糊阴影。胸部CT提示肺部阴影常见于上叶后段、下叶背段或后基底段为主,呈坠积样,以右肺多见[4,44-46](ⅡB);发生肺水肿时,两肺出现片状、云絮状阴影融合,从肺门向外扩散;进展为ARDS时可见双肺毛玻璃样改变。纤维支气管镜检查可在气管或支气管中见到食物颗粒或胃内容物,具有诊断价值[43](ⅡA)。
诊断
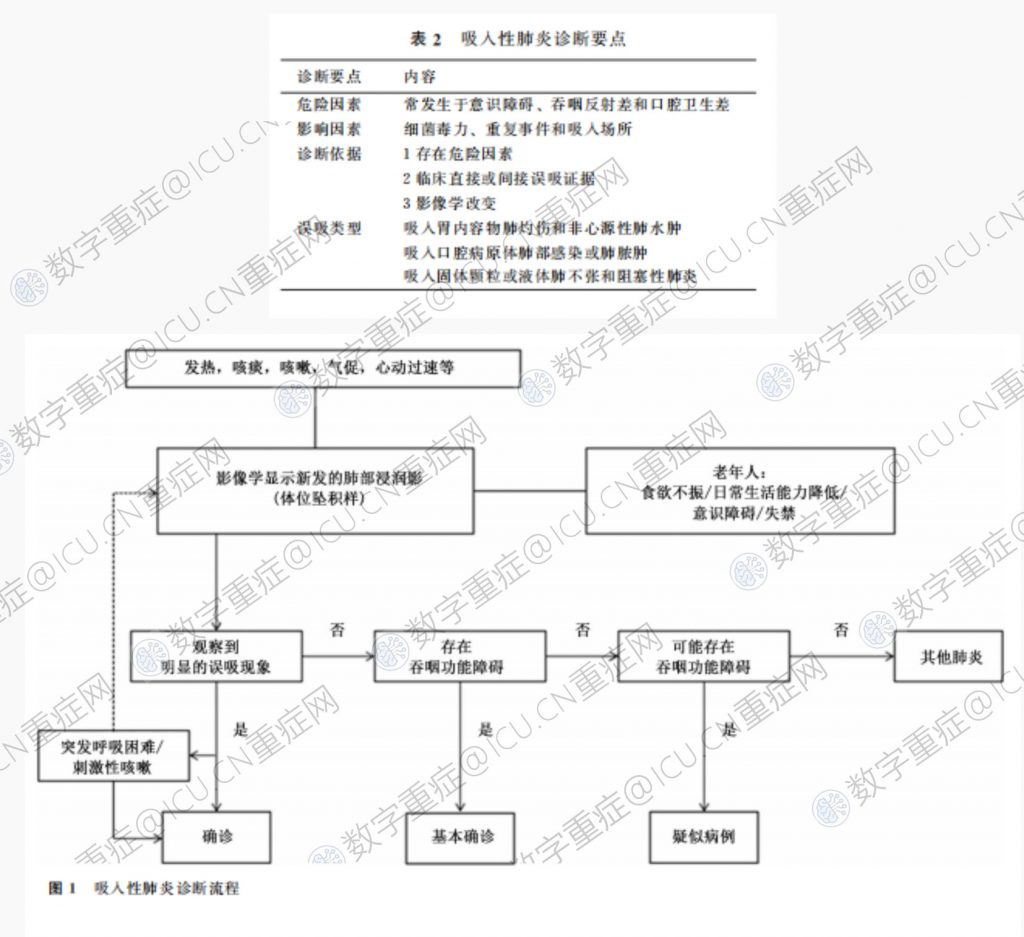
吸入性肺炎的诊断要点:常见的危险因素,如意识障碍、吞咽困难、牙周疾病或口腔卫生差等[20,28,47-49]。吸入性肺炎影响因素包括细菌毒力、重复事件及吸入场所[28]。诊断主要取决于危险因素、临床误吸和影像学上重力依赖性肺段渗出影3个主要方面[2](ⅡA),并需结合患者临床表现、实验室检查和吞咽功能检查等进一步证实。支气管肺泡灌洗液定量培养可用于区分细菌和非感染性吸入性肺炎[44](ⅡA)。
有呼吸系统症状,如发热、咳嗽、咳痰、气短、心动过速等或有非特异性症状,包括头痛、恶心、呕吐、厌食和体质量减轻、精神状态改变,尤其需注意老年人。胸部影像学显示肺部炎症改变,如直接观察到明确的误吸现象可确诊吸入性肺炎。当有吸入性肺炎危险因素的患者突然出现呼吸困难、刺激性咳嗽,甚至呼吸衰竭,应高度怀疑吸入性肺炎。有肺部炎症改变,可能有吞咽功能障碍者可疑似此病,若存在吞咽功能障碍者可基本确诊吸入性肺炎(表2、图1)。
鉴别诊断
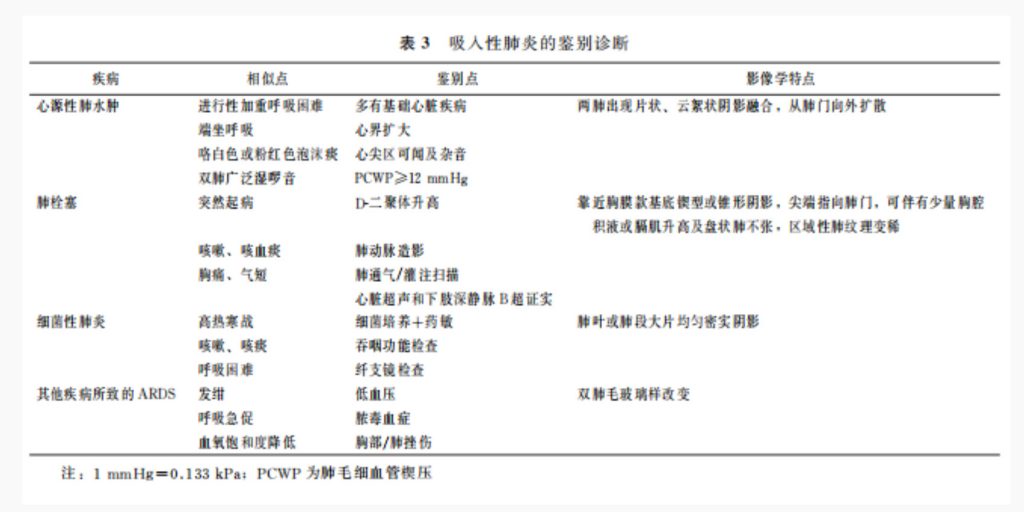
吸入性肺炎与心源性肺水肿、肺栓塞、细菌性肺炎和其他原因引起的ARDS鉴别诊断,见表3。
治疗
吸入性肺炎的治疗原则是通畅呼吸道、纠正缺氧、控制感染、减轻炎症。
8.1 一般治疗
评估患者生命体征,动态监测患者呼吸、循环、水电解质、酸碱平衡及其他重要脏器的功能,及时调整治疗方案。
氧疗是吸入性肺炎患者最常用的辅助治疗。低氧血症患者,推荐鼻导管吸氧,维持血氧饱和度在90%以上。严重低氧患者,可给予高浓度吸氧或面罩吸氧。研究显示,经鼻导管加温湿化的高流量吸氧(40~60 L/min)可用于临床[50-51](ⅡB)。经鼻高流量氧疗可显著改善脑卒中后吸入性肺炎和呼吸衰竭患者的氧合状态,并降低有创通气的发生率[52]。若发生二氧化碳潴留,则根据血氧饱和度,调整吸氧浓度,维持血氧饱和度在88%~92%[53-54](ⅢA)。无创机械通气(双水平正压通气)能降低急性呼吸衰竭患者的气管插管率[55]、改善氧合[56]、降低病死率(ⅡB)。若使用无创机械通气不能改善氧合、不能降低高碳酸血症患者的二氧化碳水平[57]或进展为ARDS,应立即改为气管插管呼吸机辅助呼吸(ⅡA),插管后宜采用小潮气量机械通气(6 ml/kg)[58-59](ⅠA),当机械通气仍不能改善,可考虑使用体外膜肺氧合(ECMO)[60-61](ⅡB)。
8.2 驱因治疗
保持呼吸道通畅,应使患者处于仰卧位、头后仰,托起下颌并将口打开,使用纤维支气管镜或气管插管吸出胃内容物或异物,早期进行支气管肺泡灌洗可加快肺部炎症阴影的吸收消散[62](ⅡB)。可吸出异物患者应及时翻身、拍背,鼓励患者咳嗽并加强引流。同时积极治疗原发病,如对脑卒中合并吞咽障碍患者应早期接受康复训练。
胃酸吸入的初始治疗需要保护气道,解除支气管痉挛和气道水肿,减少肺损伤。根据严重程度,进行体液吸引、支气管镜、插管、机械通气等。若考虑为吸入性肺部炎症,不必即刻使用抗生素,但48 h后不缓解或有脓肿脓胸或有应用抑酸剂的应使用抗生素。若考虑为吸入性肺部感染,如果全身炎症反应轻微可按CAP治疗,推荐使用头孢曲松、喹诺酮类;全身炎症反应明显或院内获得性感染,考虑革兰阴性菌(如:铜绿假单胞菌)或耐甲氧西林金黄色葡萄球菌(MRSA),不需要即刻覆盖厌氧菌,推荐使用氨苄西林舒巴坦、派拉西林他唑巴坦、万古霉素等(很多青霉素酶抑制剂能覆盖厌氧菌)(ⅡB)。在驱因的同时,对轻中度患者,建议使用抗生素,根据临床和影像学表现,48 h内重新评估患者病情。在重症患者中,(如休克或需要气管插管)即使最初胸片显示正常,可经验使用抗生素,并根据2~3 d临床病情变化,决定是否需要继续使用抗生素[2](ⅡC)。
8.3 抗感染治疗
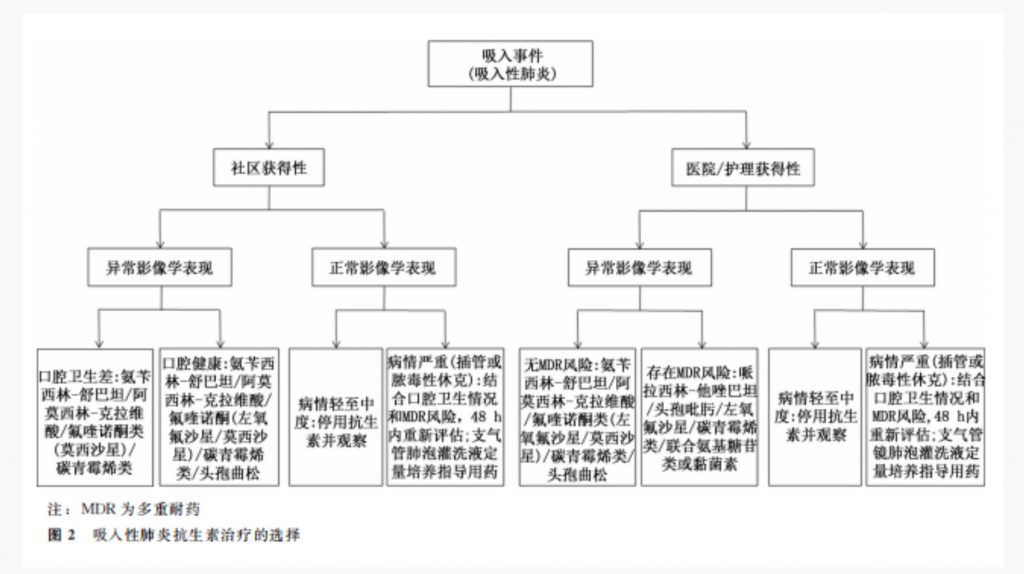
抗菌药物的选择应结合误吸事件场所推测误吸内容物中可能的病原菌,吸入性肺炎常以革兰阴性菌(大肠杆菌、肺炎克雷伯菌和铜绿假单胞菌)及金黄色葡萄球菌感染为主,治疗应覆盖这些病原菌,并根据患者病情严重程度经验性选择阿莫西林-克拉维酸、氨苄西林-舒巴坦、氟喹诺酮、碳青霉烯等具有抗厌氧菌活性的药物,或联合应用甲硝唑、克林霉素,待痰或分泌物培养药敏结果选择合适的抗生素[28,57-69](图2)。国内有专家认为,吸入性肺炎的常见病原体以敏感的肺炎克雷伯菌为主的肠杆菌科细菌和口咽部厌氧菌,非发酵菌如鲍曼不动杆菌、铜绿假单胞菌等则少见,金黄色葡萄球菌也不常见[70]。虽然重症患者口咽部往往有多重耐药菌定植,可经分泌物一起吸入远端气道并反复培养检出,但导致肺组织炎症的往往还是敏感的肺炎克雷伯菌和口腔细菌。吸入性肺炎的抗菌治疗,如果误吸量不大,没有广泛渗出实变和脓毒症征象,可选择β-内酰胺酶抑制剂、氟喹诺酮、克林霉素联合氨曲南等;严重吸入性肺炎由于感染灶细菌浓度高而出现抗菌药物接种效应,导致体外敏感体内治疗无效,可首选单用碳青霉烯,不需要联合抗革兰阳性菌或抗真菌药,3~5 d感染指标改善后可降阶梯治疗[70]。
厌氧菌感染时,建议使用氨苄青霉素-舒巴坦、阿莫西林-克拉维酸钾[66,71](ⅡA);有报道对厌氧性肺脓肿使用克林霉素有效[1](ⅡA)。当厌氧菌合并需氧菌感染时,需氧菌因改变局部氧化还原电位可能消除厌氧菌。社区获得性吸入性肺炎,可考虑使用克林霉素、氨苄西林-舒巴坦和莫西沙星[29]。医院获得性吸入性肺炎,若有耐药风险高,则可考虑哌拉西林-他唑巴坦、头孢吡肟、氟喹诺酮(左氧氟沙星)、碳青霉烯(亚胺培南、美罗培南)单独或联合[72](ⅡB)。对多耐药菌的感染,可采用氨基糖苷类或黏菌素。有MRSA危险因素的患者,可考虑使用具有抗MRSA活性的药物,如万古霉素或利奈唑胺[2](ⅡB),见表4。

若气管镜取样培养阴性,而临床疑似感染,建议抗感染治疗[73](ⅡC)。紧急情况下,气管插管昏迷患者可考虑使用抗生素。研究显示,气管插管患者使用抗生素的肺炎发生率低于未使用抗生素的患者,预防使用抗生素治疗吸入性肺炎,患者可获益,然也有相反结论[74]。也有研究显示,在插管后4 h内应用对昏迷患者可预防早发性肺炎,但对晚发性肺炎疗效不佳[75]。
静脉抗感染的患者,若生命体征平稳和临床症状缓解,可改为口服抗感染药物。不伴有空洞或脓胸或肺外感染的病例,抗生素治疗时间通常为1周[2]。考虑为化学性肺损伤的吸入性肺炎,在体温正常、影像学上肺部浸润影消失、临床症状缓解后,可考虑停止使用抗生素。
8.4 液体管理
纠正血容量,可予白蛋白或低分子右旋糖酐。使用利尿剂可避免左心室负荷过重和胶体渗入肺间质。合理限制液体入量减轻肺水肿,允许较低的循环容量来维持有效循环。
8.5 其他
肾上腺皮质激素治疗尚存争论,目前没有随机对照研究显示糖皮质激素在吸入性肺炎常规治疗中的作用。有明显化学性肺炎影像学征象患者早期可予短疗程激素治疗。有研究显示,在吸入12 h内大剂量使用,连续3~4 d,可能有助于肺部炎症吸收[76](ⅡC)。但考虑到激素的不良反应,暂不建议常规使用[2-3]。
预防
防止口咽分泌物、食物和胃内容物误吸是预防吸入性肺炎的关键。对危险因素进行预防如手术麻醉前必须使胃排空,术前至少禁食8 h、禁饮2 h;避免酗酒;停用或减少促进误吸和干扰吞咽的药物[16],如抗精神类、抗组胺类、抗胆碱能类药物的使用;抑酸剂可改变胃内正常菌群、提高胃内pH值,致病菌得以繁殖,增加吸入性肺炎发生率。见表5。

康复包括吞咽训练和早期康复活动可能有助于吞咽困难患者,并预防吸入性肺炎的复发[77]。应尽量经口进食而非肠内营养,选择浓稠软食而非浓汤或稀稠饮食[2](ⅡC)。对意识障碍或长期卧床患者可把床头抬高35~40°并采取适当体位进食,加强护理[78]。对吞咽困难的患者,在进食时应尽量保持低头(下颚向下)、头转向一侧,鼓励吞咽少量食物、多次吞咽和吞咽后咳嗽[14]。已发生误吸的患者,可考虑插鼻胃管。然鼻胃管在预防吸入性肺炎的作用尚不确定[79]。残余容量检查提示幽门后喂养吸入风险并不低于胃喂养[80]。对于进食困难、反复肺炎、营养不良、严重胃食管反流伴吸入性肺炎患者,必要时可考虑胃造瘘营养。长期卧床不起、生活不能自理的患者口腔卫生较差,吸入性肺炎的发病率较高[81]。口腔细菌可潜在导致呼吸道感染。保持口腔卫生、减少口咽细菌定植可降低隐匿性吸入性肺炎的发生。假牙清洗不当、菌斑和食物残留在假牙和牙床可间接引发吸入性肺炎。专业口腔洗护、定期清洁可有效预防吸入性肺炎[82]。
卒中患者,尤其是亚洲患者,使用抗血管紧张素转化酶抑制剂可控制血压,同时降低吸入性肺炎风险[83]。可能的机制为通过提高P物质,促进咳嗽和改善吞咽反射。西洛他唑是一种抗血小板药物,可能对P物质有类似的作用,被证实亦可用于预防卒中后吸入性肺炎[84]。此外,甲氧氯普胺可降低经鼻胃管喂养的亚急性脑卒中患者肺炎的发生率[85];梨状窦吸引能预防急性脑卒中患者吸入性肺炎的发生风险[86]。
学术交流文章,不做为临床依据,特此声明。发布者:Chu,转转请注明出处:https://www.icu.cn/?p=3552

 微信扫一扫
微信扫一扫