基于体表热度不均一性来评估危重患者低灌注的严重程度
摘要
【背景】体表热度分布不均是灌注不足的一种表现,可以通过红外热成像进行量化。我们的目的是研究体表热度不均一性是否能准确评估有低灌注风险的患者的严重程度。
【方法】这是一项前瞻性队列研究,从心脏外科ICU中有较高低灌注风险的重症患者的腿部采集红外温度图像。对每位患者计算了五个体表热度不均一性指标,包括标准差(SD)、峰度、偏度、熵和低温区比例(LTAR)。对死亡和存活的患者的人口学、临床和热度特征进行了比较。死亡风险和毛细血管再充盈时间(CRT)被分别选为主要结果和低灌注的对标指标。受试者工作曲线下的面积(AUROC)被用来评估预测的准确性。
【结果】373名患者被纳入,其中55名(14.7%)在住院期间死亡。在热度不均一性指标中,SD(0.738)和LTAR(0.768)在评估死亡风险方面与CRT(0.757)的AUROC相当。此外,正常血压、低血压和休克患者的LTAR(1至3至7%)和SD(0.81至0.88至0.94℃)呈增加的趋势。这些热度指标与CRT、乳酸和血压有关性。纳入三个热度不均一性指标(SD、峰度和熵)的联合预测的AUROC大幅升高至0.866。
【结论】体表热度不均一性为低灌注高风险的危重病人的提供了非侵入性的准确的严重程度评估。
前言
低灌注是许多危重疾病中常见的、危及生命的病理生理表现,尤其是在各种形式的休克中(1-4)。由于低灌注的严重程度和持续时间与死亡风险的增加有关(5,6),因此有必要在休克复苏和治疗优化中识别和监测它。在目前的临床实践中,低灌注通常通过分析尿量、乳酸、氧代谢指标和毛细血管再充盈时间(CRT)进行评估(7,8)。其中,CRT是评估灌注不足的一个简单工具;然而,它需要手动按压病人的手指和用肉眼计数,这增加了观察者之间的差异性,使连续的自动测量难以实现(7,9)。因此,有必要开发替代方法,以准确和方便地评估低灌注的严重程度。
体表提供了一个评估低灌注严重程度的窗口。以前,Kazune等人探索了一个6分制的皮肤花斑评分,但大多数患者,评分都落在0-2的范围内(10),阻碍了准确的预测。另一个缺点是,皮肤花斑出现的滞后性(11),使得早期预警和持续监测更加困难。患者的皮肤颜色也可能妨碍准确的观察。此外,Bourcier等人报告说,脚趾到室内的温度梯度反映了组织灌注(12)。但在单点(脚趾)获得的热度信息是有限的。相反,在生理上,局部血流决定了体表温度的分布。当外周灌注恶化时,到达体表的血流的量和连续性下降,导致热度分布不均匀(即热度不均一性)。
因此,我们假设体表热度不均一性指标可以准确反映低灌注高风险的患者的严重程度。本研究的目的是验证基于无创红外热成像的体表热度不均一性指标监测是否能准确评估有低灌注风险的患者的严重程度。
方法
【患者】本研究经机构审查委员会批准,在拥有40张床位的复旦大学附属中山医院心脏外科重症监护室(ICU)进行。在研究期间(2020年6月至2021年5月),在收到患者亲属的知情同意书后,前瞻性地招募了患者。接受重大心脏手术的患者,如果有任何低灌注的高风险因素,就考虑纳入研究,包括:(1)至少30分钟的低血压(收缩压[SBP]<90毫米汞柱或依赖升压药),(2)心功能不全(左心室射血分数<40%或需要使用强心药)或(3)有证据显示灌注不足(心动过速、高乳酸血症、少尿、皮肤花斑、CRT延长等)。排除标准为:(1)患者年龄小于18岁;(2)怀孕;(3)严重的动脉异常(狭窄或栓塞)或下肢皮肤病变;(4)其他妨碍获取完整图像的情况(双腿有动静脉导管、手术切口或浓密的毛发);(5)预计在ICU停留时间少于24小时。
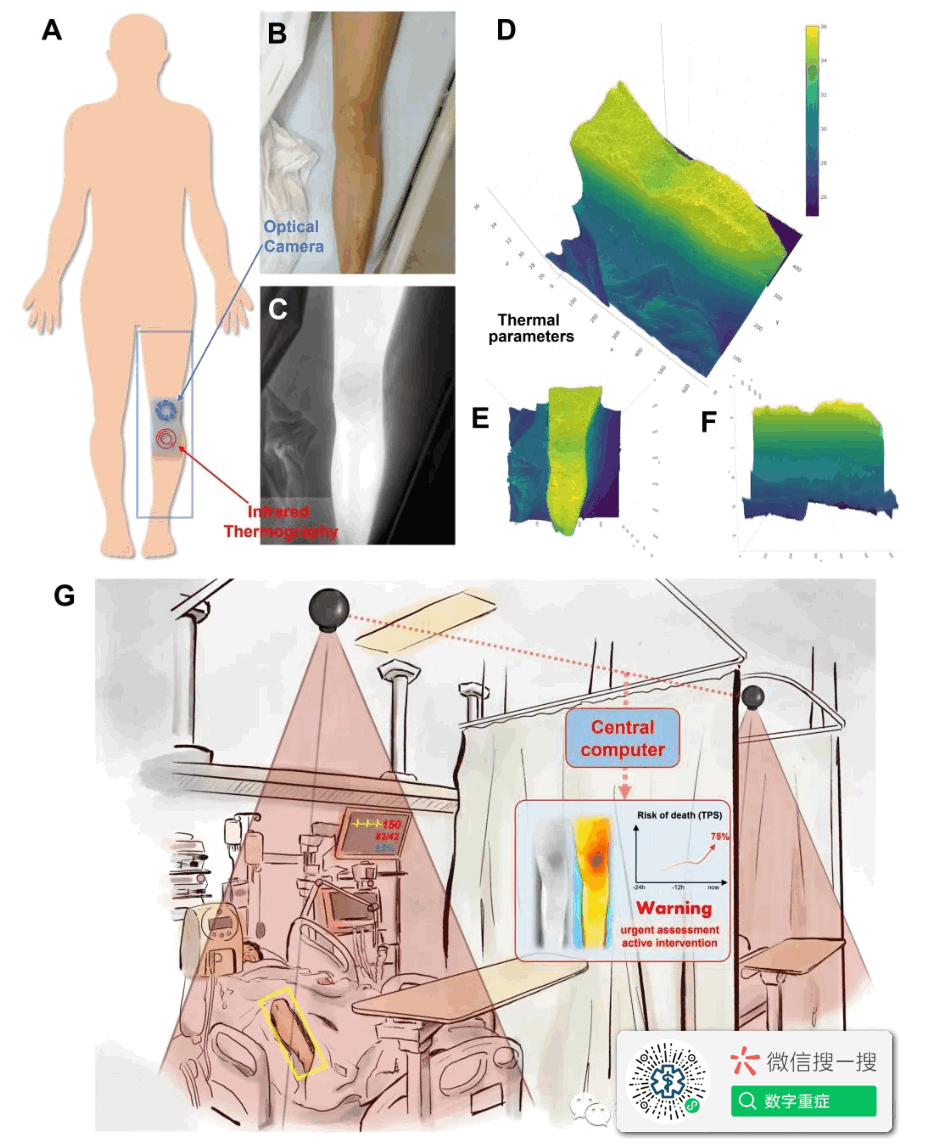
【热度图像采集和预处理】每位受试者都是仰卧位,露出其中一条腿部。选择花斑评分的区域[7],即左腿或右腿会阴部以下、脚踝以上的体表,进行热数据采集(图1.A和C)。图像采集包括两台相机:(1)红外热成像仪(A615,640×480像素,±0.05ºC,Teledyne FLIR LLC,美国加州),被置于患者腿部正上方(图S1),以收集热信息;(2)用普通相机拍摄平行的可见光图像(图S1和图1.B)。腿部的轮廓最初由阈值分割算法描绘,然后由两名研究成员手动调整。根据温度矩阵和计算的热度不均一性指标绘制地形图(等温图,图1.D-F)。
【体表热度不均一性指标的计算】利用感兴趣区域的预处理数据,我们计算了反映热度不均一性的五个指标,包括标准差(SD)、峰度(13)、偏度(13)和熵(14)以及低温区比例(LTAR)。LTAR被定义为体温下降超过最高温度10%的腿部区域的比例(补充材料中分享了推断过程的细节)。例如,如果腿部的最高温度是38℃,那么LTAR就是体温下降超过3.8℃(低于34.2℃)的区域比例。
【临床数据的收集和随访】入院时,患者的人口统计学信息、基本生命和循环指标(SBP、DBP、MAP、HR、CVP、血管活性药物评分[VIS](15))和灌注指标(花斑评分(16)、乳酸、ΔPCO2、ScvO2、2小时乳酸清除率、CRT和尿量[UO])均被记录。还收集了当天的实验室检查(WBC、血小板、血红蛋白、ALT、AST、胆红素、肌酐、BUN、[cTnT、NT-proBNP和PCT)。序贯器官衰竭评估(SOFA)评分(17)也被计算。
【相关定义】所有患者均被随访至出院或死亡。主要结局是院内的死亡风险。次要终点是机械通气时间、ICU住院时间和总住院时间。此外,我们将CRT作为低灌注的对标指标,因为它容易获得且较准确。我们还使用了低灌注状态的三个经典阶段定义:正常血压、低血压和休克,以评估常规和热度不均一性指标的分布。在这种情况下,低灌注被定义为SBP<90mmHg或使用升压药物,而休克被定义为低血压和高乳酸血症(乳酸≥4mmol/L)(20)。
【统计学分析】数据以均值±标准差或中位数与四分位数范围或总数与百分比表示,并酌情用学生t检验或Wilcoxon(或Friedman)秩和检验或Fisher精确检验来比较。绘制ROC曲线,并计算曲线下的面积(AUROC)(18)以评估对死亡风险的预测准确性。为了提高预测的准确性,我们做了基于逻辑回归模型的联合预测。对于联合预测模型,我们绘制并计算了相应的校准曲线和Brier评分(19)。联合预测模型可以计算出量化的死亡风险(范围:0-100%),然后将其定义为热灌注评分(Thermal Perfusion Score,TPS)。然后通过相关性矩阵和带有Loess回归曲线的二维直方图探讨TPS和常规低灌注指标之间的关系。在正常血压、低血压或休克的患者亚群中,还评估了常规低灌注指标、热度不均一性指标和TPS的分布趋势。最后,绘制了TPS的生存曲线,以获得其判别能力。所有的统计检验都是双尾的,P值<0.05表示有统计学意义。统计分析使用R,4.1.1版。
结果
【研究队列的特征】在一年的时间里,有373名有低灌注风险的患者入组,55名患者在中位数为16[IQR 12-105]天的住院期间死亡(图S2)。与那些活到出院的病人相比,院内死亡的病人有更高的HR和VIS,而DBP和MAP则更低(表S1)。死亡患者的血液学(血红蛋白和血小板较低)、肾脏(肌酐和BUN较高)、肝脏(ALT和AST较高)、心脏(cTnT和NT-proBNP较高)和感染(PCT较高)指标也较差(表1)。死亡组的SOFA评分也比生存组高得多(表S1)。此外,正常血压、低血压和休克的患者分别有195人、127人和51人(表S2),他们的住院病死率从8%上升到15%,然后又上升到37%。
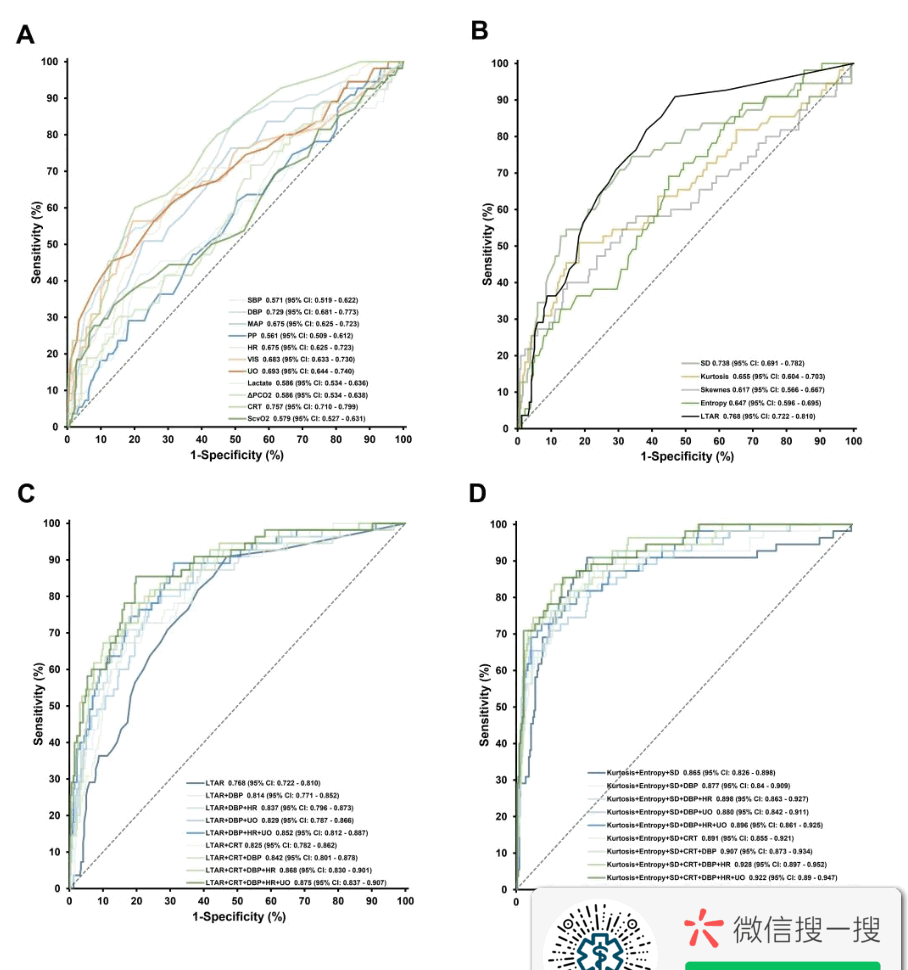
【常规低灌注和循环指标的表现】除了ScvO2和乳酸在2小时内的变化,常规指标在死亡和存活的病人之间表现出明显的差异(表S1)。死亡组患者的UO较少,乳酸和ΔPCO2较高,CRT延长,皮肤花斑较多,然而,上述指标之间的相关性并不强(图S3)。这些常规指标对死亡风险显示出不同程度的预测准确性。CRT和UO的具有最佳和仅次的AUROC,分别为0.757(95%CI:0.710-0.799)和0.693(95%CI:0.644-0.740),与DBP(0.729[95%CI:0.681-0.773])和HR(0.675[95%CI:0.625-0.723])相近(表1和图2A)。
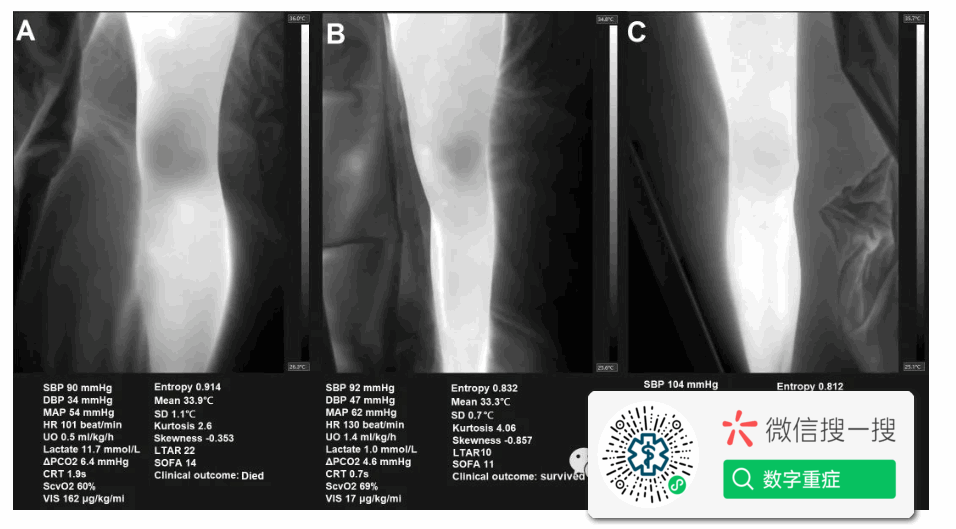
【体表热度不均一性的三个代表性案例】我们总结了三个有代表性的案例来阐明热度不均一性的患者间差异(图3)。第一个案例是一个有低血压、高乳酸血症、大剂量升压药和高SOFA评分的病人(图3A)。从热度图像中,我们还可以看到更高的熵、SD和LTAR。极高的LTAR在肉眼看来是一个主要分布在膝关节周围的低温暗区。第二个病例涉及一名低血压和心动过速的患者,但低灌注指标有所改善,SOFA评分较低(图4B),仍有一个低温区,但比第一例要小得多。第三个案例涉及一名灌注压、心率较正常的患者,乳酸和CRT水平也相对正常(图3C),热度图像显示了极其均匀的温度分布。
【热度不均一性指标的表现】平均体温受基础体温、环境温度和发热性疾病的影响很大,因此在死亡患者和存活患者之间没有表现出差异(34.2±1.5 vs. 34.4±1.1 ℃,P=0.284)。相比之下,死亡患者比存活患者有更为异常SD、峰度、熵、偏度和更高的LTAR。在预测死亡风险方面,LTAR的AUROC最高,为0.768(95% CI: 0.722 – 0.810),其次是SD(0.738 [95% CI: 0.691 – 0. 782]),峰度(0.655[95%CI:0.604 – 0.703]),熵(0.647[95%CI:0.596 – 0.695])和偏度(0.617[95%CI:0.566 – 0.667])(图2B和表1)。与CRT、乳酸和ScvO2等常规指标类似,正常血压、低血压和休克患者的LTAR和SD的中位数值分别从1%到3%到7%,从0.81℃到0.88℃到0.94℃,显示出与循环状态恶化一致的趋势(P=0.003和0.033)(图S7)。
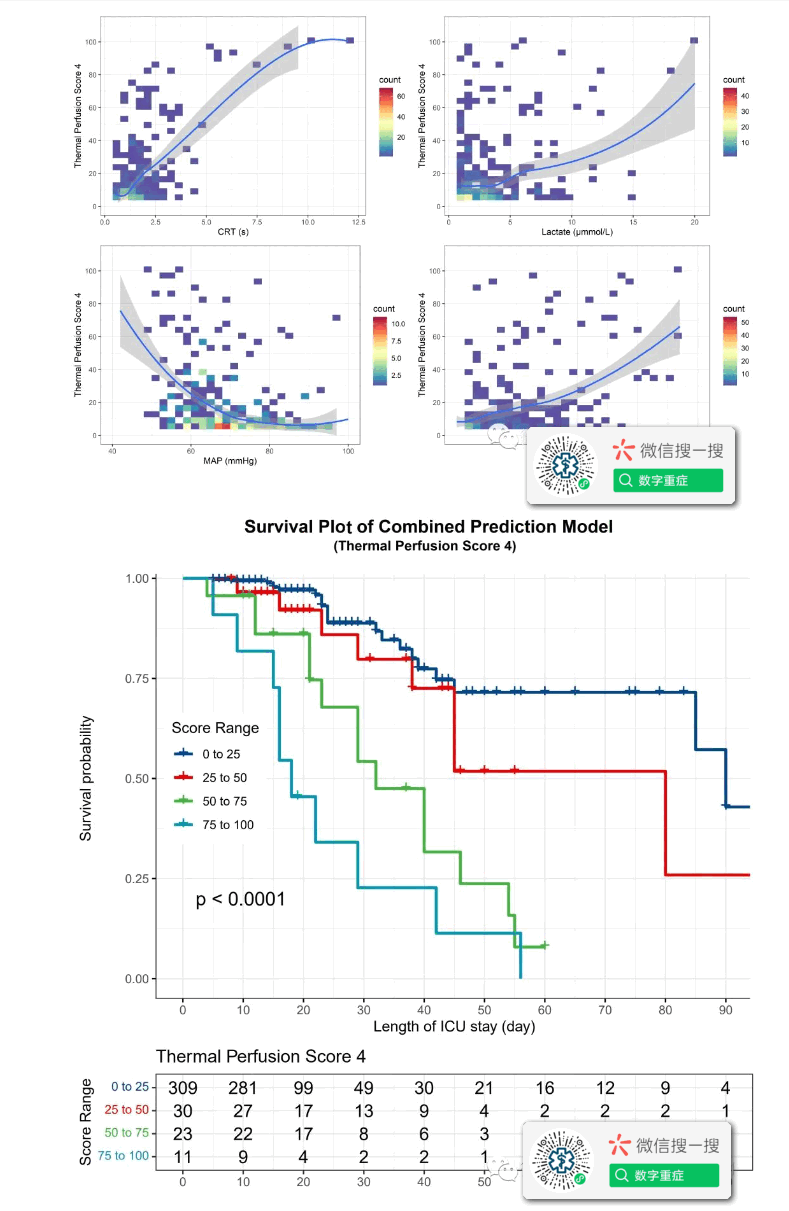
【由不均一性指标组成的热灌注评分】使用三个不均一性指标(峰度+熵+SD)进行综合预测,AUROC增加到一个更高的值0.865(95 % CI:0.826 – 0.898),并明显优于单独的LTAR(P<0.001)。将这三个指标纳入逻辑回归模型,可得到0-100%的死亡概率,可定义为热灌注评分(TPS-5,表S3)。这个分数与MAP呈负相关,但与CRT、乳酸和VIS呈正相关(图S6和S8),表明它可能从不同角度反映灌注不足的严重程度。它在正常血压、低血压和休克患者中也有增加的趋势(图S7)。此外,从生存曲线来看,它具有很强的风险分层能力,但对中高风险患者的区分能力还不太理想(图S9)。
【将常规指标纳入热灌注评分中】尽管准确性较低,但传统指标,如HR、UO、血压和CRT,都很容易获得。将HR、UO、血压或CRT纳入基于峰度+熵+SD或LTAR的TPS,可提高其区分能力(AUROCs:0.837至0.928)(表S3和图2C、D)。在这些TPS中,以第四个TPS(TPS-4)为例,它具有良好的Brier评分和风险分层能力,同时与常规指标保持相关性(图4和5)。在正常血压、低血压和休克患者中,TPS-4的中值也分别从4到8增加到19(P<0.001)(图S7)。未来,可以根据这些热度和常规指标在临床实践中的自动捕捉能力,选择合适的联合预测模型(图S10)。
讨论
据我们所知,这是第一个探索热度不均一性指标在危重病人中的转化价值的研究。我们的研究表明,热度不均一性指标在评估有低灌注风险的患者的严重程度方面具有良好的准确性(不逊于CRT)。
由于缺乏低灌注状态的金标准,创建和验证新的指标一直很困难。根据Bourcier等人的研究方法(12),总结出探索新的低灌注指标的三条标准。一个新的低灌注指标可以被认为是有效的,如果它(1)(至少在理论上)与外周低灌注有特定的生理关系;(2)可以准确反映低灌注患者的死亡风险,特别是CRT;(3)与众多常规低灌注或循环指标相关,并且在休克和非休克患者中存在差异。在本研究中,体表热度不均一性指标满足了上述三个要求,证明了其作为低灌注指标的潜力。
红外热成像技术在医学领域已经应用了很多年。通过检测局部热度的异常,可以确定诸如乳腺癌(21,22)和动脉狭窄(23)等疾病。在猪的模型中,Magnin等人(24)报告,周围到中心的热度梯度与动脉压(Spearman r: – 0.40, p=0.002)和心指数(Spearman r: – 0.36, p=0.02)呈负相关。然而,两点温度差并没有充分利用体表热度分布中包含的信息。此外,Nagori等人(25)使用机器学习方法来读取儿童的热度图像,从而预测发生休克的概率。尽管符合得很好,但机器学习方法就像一个 “黑匣子”,缺乏可解释性(26),这意味着我们不知道它是如何准确利用温度数据的。
在这项研究中,我们使用具有精确定义和数学含义明确的变量来评估热度数据,我们发现热度分布不均一性的参数与病情严重程度密切相关。在休克状态下(可能是隐匿的),体表血流变得不均匀,皮肤花斑会逐渐出现(10)。此外,热度异常出现得更早,而且比皮肤颜色异常更明显(11),使这种热学方式更容易揭示灌注的异常。由于以往的研究表明,膝关节部位是低灌注的前哨部位(11,27),在本研究中,我们直观地发现,患者的病情越严重,腿部低温区域出现的越明显,而且随着病情的恶化,这个区域会逐渐从膝关节向周围延伸。
更重要的是,通过体表热度不均一性和联合预测模型,可以实现可量化的评估和更高的准确性。CRT是评估低灌注的主流指标(28),并在两个大规模的临床试验中被当作治疗目标(29, 30)。在本研究中,我们以CRT为锚点,比较热度指标的准确性。我们发现,LTAR与CRT或ScvO2之间存在关联性。后两者是皮肤血流和全身供氧的指标。因此,LTAR可以被认为是对低灌注的更全面的评估。当把某些常见的指标(HR、DBP、UO和CRT)加入到LTAR中时,联合预测模型的准确性可以提高到一个惊人的水平。
2020年,李飞飞团队提出了关于环境智能的设想(31)。在她的设计中,红外摄像机被常规地部署在床边,以监测病人在夜间区域的活动。我们的研究证实,随着特定算法的引入,红外摄像机(带测温功能)也可用于实时监测有低灌注风险的病人的严重程度,并为ICU环境中的高危病人提供早期预警(图1G)。这种方式的优点是无接触、无创、不需要一次性耗材。危重病人,尤其是接受大手术的病人,术后低灌注的风险更大,但要普遍实施先进的血流动力学监测是具有挑战性的。此外,部署红外摄像机不具有工程或经济上的挑战性。部署红外摄像机的成本已经相当低廉,可以普遍监测低灌注的严重程度和进展情况,显示出巨大的临床转化价值。
本研究只记录了每个病人的单一数值,没有进行红外热成像的连续监测。然而,Bhavani等人发现,温度轨迹也与疾病的严重程度和预后有关(32)。因此,热度指标的趋势,特别是在治疗变化或特定干预措施前后,可以提供额外的信息。这有可能作为未来研究的方向。
我们的研究有几个局限性。它是在一个单一的中心进行的,这可能会限制其普遍性。此外,我们缺乏低灌注的金标准,所以CRT(最广泛认可的灌注参数之一)被用作锚点。另外,作为一项概念验证研究,我们没有使用更先进和复杂的模型进行综合预测。最后,下肢的严重血管疾病,如动脉狭窄,影响了热度不均一性的计算,因此被排除在外。该算法将需要在未来进行改进,以适应这一人群。
结论
反映体表热度不均一性的指标与低灌注高风险的重症患者的严重程度有关,并能提供了比传统工具更精确、无创和定量的评估。未来,通过对热学算法的深入改进、验证和优化,研究人员可能有机会进行进一步的前瞻性研究,以更好地监测和指导低灌注的针对性复苏。
全文链接:https://pubmed.ncbi.nlm.nih.gov/36155398/
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫