摘要
【背景】国际血栓与止血学会(ISTH)于2001年发布了弥散性血管内凝血(DIC)诊断标准。至此之后,DIC被认为是终末期消耗性凝血障碍,而不是治疗的靶点。然而,DIC不仅仅是一种失代偿性凝血障碍,还包括凝血系统激活的早期阶段。因此,ISTH最近发布了脓毒症诱导凝血病(SIC)标准,该标准可以利用生物标志物来诊断代偿期的凝血障碍。
【内容】尽管脓毒症是最常见的基础疾病,但由于各种危重情况,DIC是一种基于实验室指标的诊断。脓毒症相关DIC的病理生理机制是多因素的,除了凝血功能激活和纤维蛋白溶解被抑制外,作为血栓形成的一部分,激活的白细胞、血小板和血管内皮细胞还启动了多种炎症反应。虽然ISTH已经建立了明确的显性DIC诊断标准来诊断晚期DIC,但出于治疗方面的考虑,还需要其他能诊断DIC早期阶段的标准。因此,ISTH在2019年引入了SIC标准,这些指标易于获得,只需要血小板计数、凝血酶原时间-国际标准化比率和序贯器官衰竭评估评分。SIC评分可以用来评估疾病的严重程度和确定潜在的治疗干预的时机。治疗脓毒症相关DIC的主要缺点之一是除了治疗潜在感染之外,缺乏特异性治疗方法。到目前为止的临床试验都以失败告终,因为其中还纳入了没有凝血障碍的患者。然而,除了控制感染外,抗凝治疗将是脓毒症相关DIC的选择之一。因此,肝素、抗凝血酶和重组血栓调节蛋白的地位还需要在未来的临床研究中得到证实。
【结论】有必要寻找一种新的治疗脓毒性相关DIC的策略,以改善患者预后。因此,我们建议使用SIC评分系统筛查和监测DIC。
关键词:脓毒症,弥散性血管内凝血,凝血病,内皮细胞,抗凝血酶,血栓调节蛋白
引 言
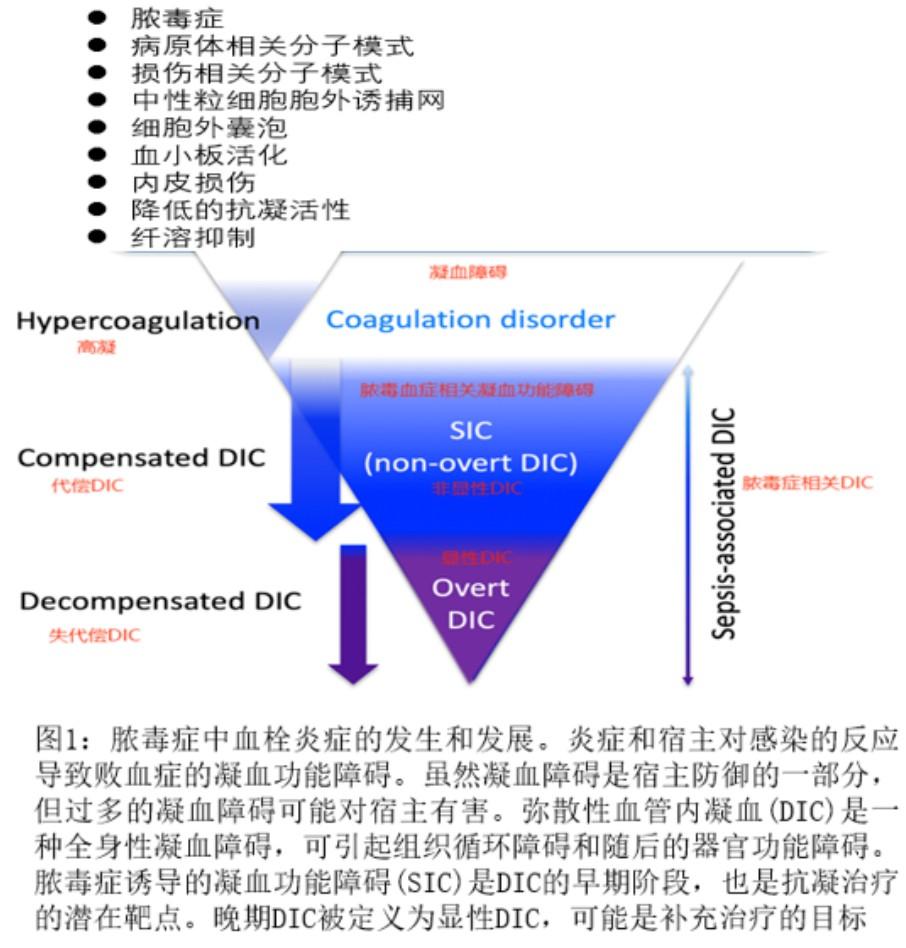
止血是抵抗各种病理生理损伤的一种基本的宿主防御机制,临床上表现为急性损伤和危重病相关的大血栓和微血栓。虽然止血反应在某些情况下是有利的,但过量的凝血酶原会导致组织灌注不良,进而器官功能障碍。弥散性血管内凝血(DIC)的诊断标准是根据实验室的(DIC)诊断标准临床诊断而定。根据潜在的致病因素不同,DIC的病理生理学、表型和治疗具有很大的不同。然而,脓毒症是DIC最常见和最危及生命的病因,通常表现为血栓性DIC。这种类型的DIC常合并器官功能障碍,出血事件发生率较低。凝血状态可根据基础疾病的进展而动态变化。脓毒症相关DIC是一种动态的过程,从凝血功能紊乱开始,可逐渐发展成脓毒症诱发的凝血功能障碍(SIC),最终进展为失代偿性凝血功能障碍(显性DIC)(图1)。代偿性DIC需要抗凝治疗,而失代偿期可能需要补充治疗之外的其他治疗方法。脓毒症相关DIC治疗的最新进展包括根据现成的临床信息制定早期诊断标准,以及潜在有效的抗凝剂的应用。这篇综述将总结在脓毒症相关DIC的诊断、治疗和未来研究方面的进展。
胞外囊泡(Extracellular vesicle,EV)是一种脂质双分子膜包裹的膜性囊泡,由细胞释放到细胞外微环境的膜性囊泡,携带母细胞来源分子,参与机体的生理和病理活动过程,在细胞间通讯中起到关键的信使作用。
脓毒症相关弥散性血管内凝血的病理生理
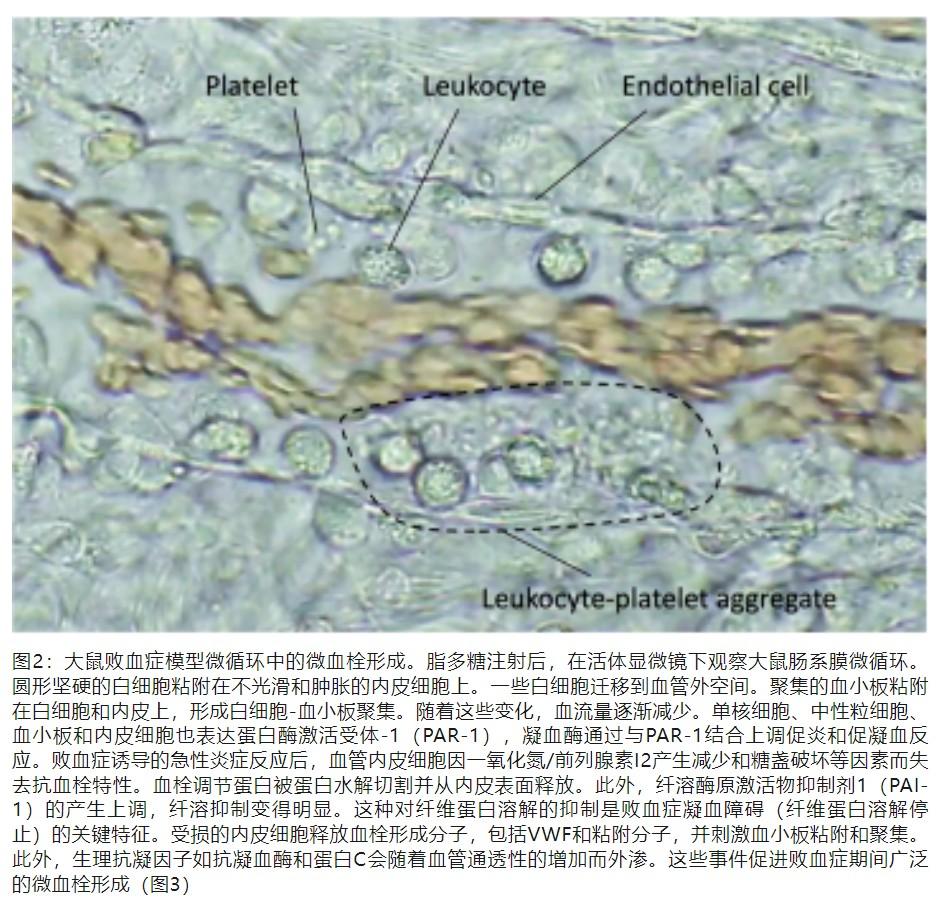
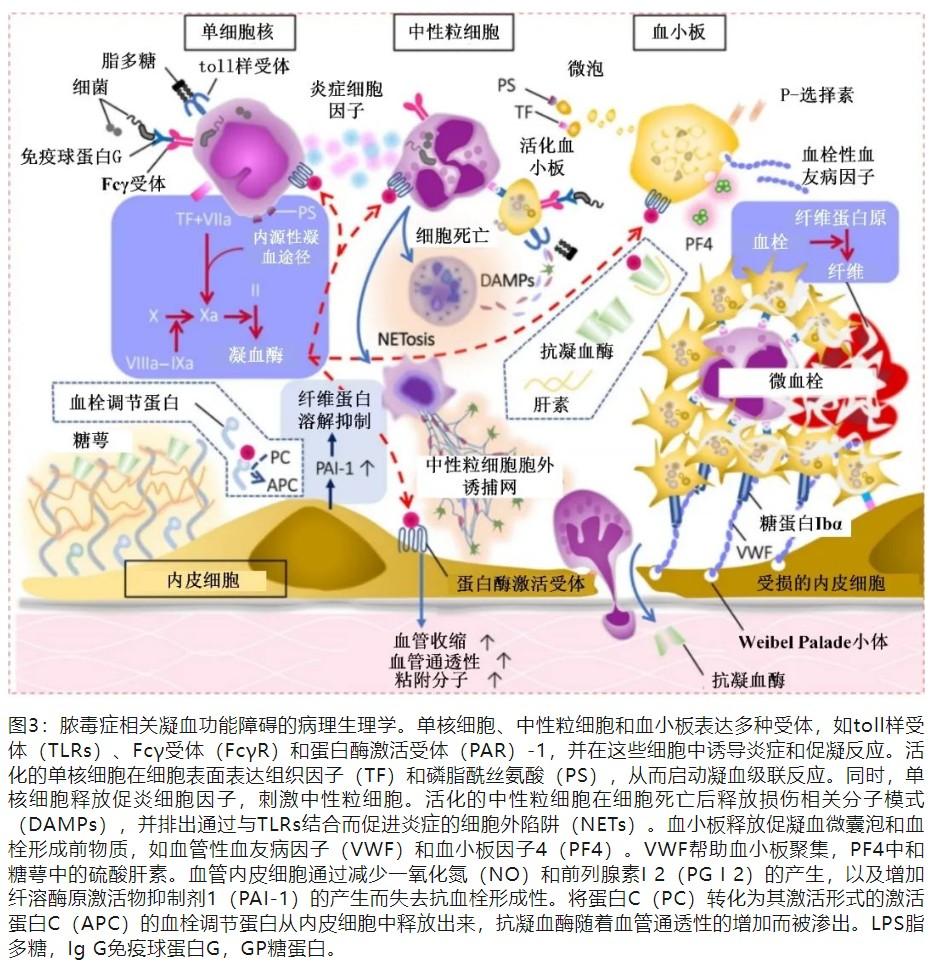
单核/巨噬细胞是入侵的病原体和吞噬细胞病原体的第一线应答者,它们通过感知特定的分子模式来检测细菌,并引发促炎和促凝血反应以捕获和定位它们。作为模式识别受体,单核/巨噬细胞表达Toll样受体(TLRs)、Fcγ受体和G蛋白偶联受体,以检测病原体相关的分子模式(PAMP)调节先天性免疫系统和凝血系统。TLRs不仅对PAMPs起反应,还传递宿主来源的应激分子的结合信号,即损伤相关分子模式(DAMP),从而启动一系列炎症和凝血的恶性循环。随后,单核/巨噬细胞产生促炎性细胞因子和趋化因子,激活中性粒细胞,促进细胞膜上组织因子(TF)和磷脂酰丝氨酸(PS)的表达。TF和PS启动外源性和内源性凝血级联反应,促进凝血酶原反应。激活的中性粒细胞通过蛋白酶、活性氧种、释放中性粒细胞胞外陷阱(Net)来杀死病原体,并通过细胞死亡机制进一步扩大炎症反应。细胞焦亡、坏死性凋亡、网状细胞外陷阱生成和坏死是典型的细胞死亡形式,它们通过释放DAMPs和其他细胞毒性物质来促进炎症和凝血。血小板还通过表达黏附分子、释放颗粒成分如血小板因子4(PF4)、血管性血友病因子(VWF)和促凝剂微泡来形成血栓,从而参与宿主防御。这些反应导致血管内微血栓形成(免疫血栓形成),以保护宿主免受感染(图2)。在凝血因子中,凝血酶是调节炎症和凝血的关键介质。
单核细胞、中性粒细胞、血小板和内皮细胞也表达蛋白酶激活受体-1(PAR-1),凝血酶通过与PAR-1结合上调促炎和促凝血反应。在脓毒症诱导的急性炎症反应中,血管内皮细胞由于一氧化氮/前列腺素I2产生减少和糖基化破坏等因素而失去了抗血栓特性。血栓调节蛋白被蛋白水解性裂解并从内皮表面被释放。此外,纤溶酶原激活物抑制物1(PAI-1)被激活上调,促进纤溶抑制作用。纤溶抑制是脓毒症凝血功能障碍的重要特征。受损的内皮细胞释放血栓形成VWF和黏附分子,刺激血小板黏附和聚集。此外,生理性抗凝血因子如抗凝血酶和蛋白C随着血管通透性的增加而外渗。以上过程促使脓毒症期间广泛的微血栓形成(图3)。

然而,该类研究还没有结果。但是,SIC标准似乎比JAAM DIC标准更简单,成本更低,因此更适合用于监测。此外,SIC已被证实可直接、持续的监测DIC是否进展。
SIC标准是专门为脓毒症相关的DIC设计的。同样,如考虑到潜在疾病的特异性,可能有助于我们制定简单和更好的标准;我们认为这种方法应该扩展到DIC的其他领域,即血液疾病DIC和癌症相关DIC。
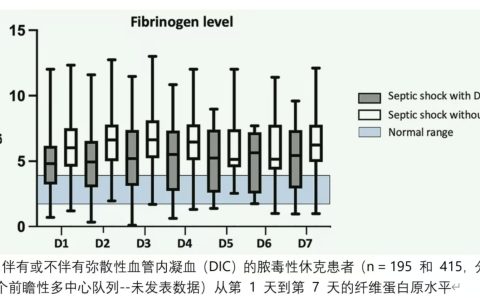
脓毒症相关DIC的患病率因目标人群和诊断标准而异,但总体来说,与非DIC患者相比,DIC患者的死亡率更高。Gando等人报告了ISTH显性DIC和JAAM DIC诊断标准的发生率和死亡率(Sepsis-1),分别为18.1%和46.8%,38.1%和38.4%。另一项前瞻性队列研究报告了1892例脓毒症患者(sepsis-1)诊断为显性DIC、JAAM DIC和SIC的患病率和死亡率,分别为29.3%和38.4%、61.4%和33.9%以及60.8%和32.5%。一项纳入296例Sepsis-3患者的队列数据显示,显性DIC、改良JAAM DIC(用抗凝血酶活性代替SIRS评分)和SIC的患病率分别为22.6%、43.2%和56.1%,28天死亡率分别为55.2%、47.7%和44.0%。以上数据表明,DIC的发病率因诊断标准而异,但无论使用哪一种诊断标准,脓毒症相关DIC的死亡率都已超过30%。诊断DIC的主要目的不是预测预后,而是帮助决策开始干预的时机,因为与非DIC患者相比,发生DIC患者的死亡率更高。值得注意的是,最近的研究支持抗凝治疗用于凝血障碍/DIC或疾病程度较严重的患者。此外,JAAM DIC和SIC评分反映了疾病的严重程度,与死亡率具有一定的相关性。Lu等人总结了9432例脓毒症患者的SIC评分,报告称SIC患者的28天死亡率为34%,而非SIC患者为25%,SIC是28天死亡率的一个独立风险因素。
SIC诊断标准的局限性是可能会被误诊为DIC,因为其只包括两种凝血生物标志物。例如,不容易与血栓性微血管病(TMA)疾病相鉴别,如血栓性血小板减少性紫癜(TTP)和非典型溶血性尿毒症综合征(aHUS),以及肝素诱导的血小板减少症(HIT)和SIC。为了提高准确度,ISTH DIC SSC绘制了有助于系统鉴别诊断的流程图。尽管TMA也有PT-INR轻度升高,但其血小板计数的下降更为突出,而TTP、aHUS和HIT中PT的升高程度较小。此外,抗凝血酶活性,一种反映内皮损伤的生物标志物,在SIC和DIC中显著降低,但在TMA中通常是正常的,也有助于鉴别。基于抗凝血酶水平在DIC早期阶段降低,Jackson Chornenki等人报道称,血小板计数、PT-INR联合抗凝血酶活性可以识别脓毒症早期DIC的患者。尽管发病率不高,但这些类似DIC的疾病的鉴别诊断至关重要,因为如果治疗不当,死亡率会相当高。
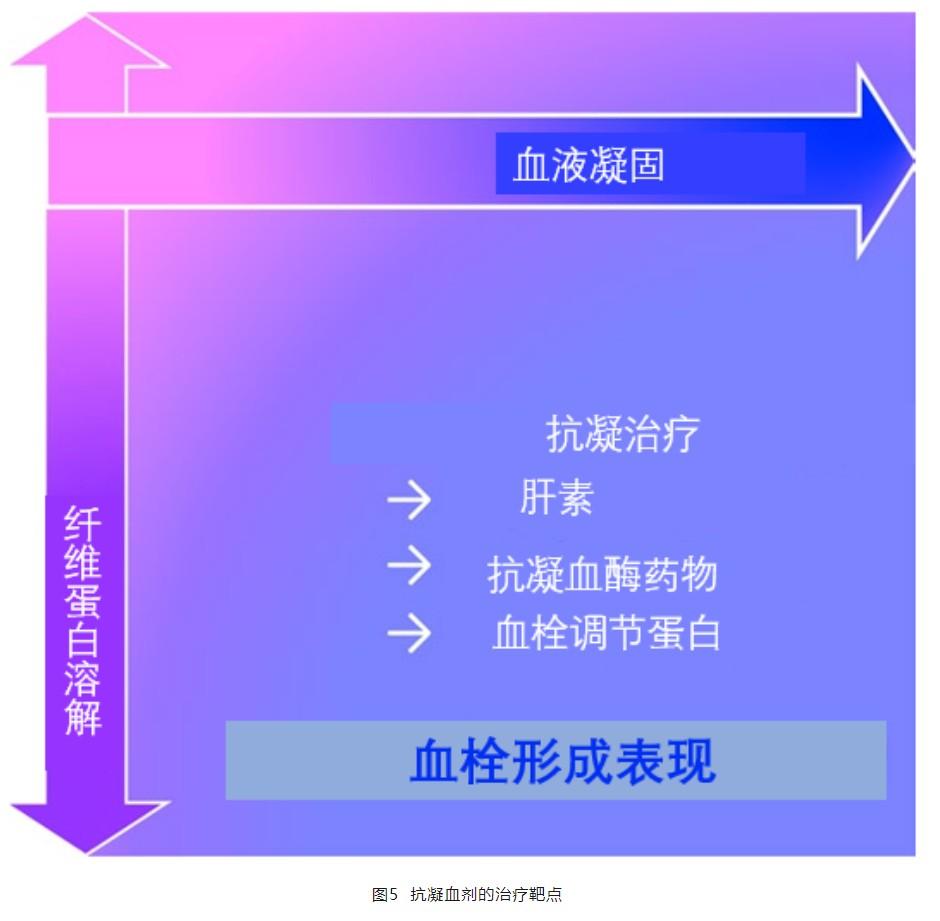
基础疾病的治疗在DIC患者中是关键。但对于脓毒症相关DIC患者,纠正器官组织持续灌注不良是基石。然而,除了抗生素和基础疾病治疗外,目前几乎没有研究显示出抗凝治疗的益处。尽管大规模随机对照试验对几种抗凝剂进行了对照,但目前还没有研究证实抗凝剂的有效性,可能的原因包括脓毒症临床表现的多样性,但如前所述,对于仅有凝血障碍的患者,或是非常严重的脓毒症相关DIC患者,都可考虑进行抗凝治疗(图4)。
肝素
出于各种原因,肝素常用于脓毒症患者。然而,没有关于单独使用肝素治疗脓毒症相关DIC的大型随机对照研究。最近的一项荟萃分析报道,普通肝素可以降低脓毒症死亡率,特别是疾病非常严重的患者中。然而,该项研究人群并不局限于凝血功能障碍/DIC患者。另一项关于肝素治疗DIC的系统综述中,仅只有3项(共8项研究)使用肝素作为对照。虽然肝素已被强烈推荐用于COVID-19,但其对脓毒症相关DIC的疗效尚不清楚。日本的一项随机对照试验比较了重组血栓调节素与肝素治疗在血液学恶性肿瘤或脓毒症相关DIC中的有效性和安全性。亚组分析显示,结果显示,重组凝血调节素组和肝素组DIC成功率分别为67.5%和55.6%,28天死亡率分别为21.4%和31.6%。
重组血栓调节蛋白于2008年被日本批准用于治疗DIC。如前所述,Aikawa等人对3期临床试验的80例脓毒症相关DIC患者进行了亚组分析,并报告了重组血栓调节蛋白的有效性。随后,2019年SCARLET研究纳入了患有凝血障碍和器官功能障碍的脓毒症患者(心血管和/或呼吸衰竭,血小板计数在24小时内下降30至150×/L或>30%,PT-INR>1.4[SIC评分>4])。尽管治疗人群中的差异在统计学上并不显著,但在基线时符合标准进入亚组的患者28天生存率更好的趋势。
近日,有研究称,抗凝血酶联合重组血栓调节蛋白具有潜在的益处,尤其是针对严重病例。该联合治疗的有效性应该在未来的研究中进一步验证。
至于SIC,肝素、抗凝血酶和重组血栓调节蛋白是目前脓毒症相关DIC的可选治疗。但到目前为止,没有任何一种药物获得了强有力的疗效证据。设计临床试验来验证这些抗凝剂的有效性方面存在一些障碍。这是因为,首先,研究终点通常设定为死亡率差异;然而,有许多因素会影响患者的预后,需要一个更全面而复杂的终点来反应其治疗效果。其次,确定最佳剂量、持续时间和停药时间较为困难。由于凝血激活是宿主防御机制的一部分,因此靶标的选择和药物剂量的选择也很重要。由于抗凝治疗越来越受到关注,因此有必要建立国际合作研究。
本文荟萃自 公众号 杭州市一重症,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。


 微信扫一扫
微信扫一扫