脓毒性休克中去甲肾上腺素的代替药物:什么药物?什么时候?

摘要:
血管加压药是脓毒性休克患者血流动力学管理的基石。去甲肾上腺素目前被推荐作为一线血管加压药。除去甲肾上腺素外,还有许多具有特定性质和(或)优势的强效血管升压药,在激活特定受体后通过不同途径作用于血管;这可能对脓毒性休克患者有意义。不再推荐脓毒性休克患者使用多巴胺,因为其与较高的心律失常发生率相关,但在死亡率或器官功能障碍方面没有任何益处。肾上腺素目前被认为是一种二线血管加压药物,因为与去甲肾上腺素相比,肾上腺素相关的代谢和心脏不良反应发生率更高。然而,在无法获得去甲肾上腺素的情况下或难治性脓毒性休克合并心肌功能障碍的患者中,可考虑使用该药物。由于其对死亡率和肾功能的潜在影响以及其减少去甲肾上腺素的作用,在脓毒性休克和持续动脉低血压患者中,血管加压素被推荐作为二线血管加压药治疗,而不是增加去甲肾上腺素的剂量。然而,两种合成的血管加压素类似物,即特利加压素和selepressin,尚未用于脓毒性休克患者的治疗,因为它们的使用与较高的指缺血发生率相关。最后,对于脓毒性休克患者,尤其是最严重的病例和/或需要肾脏替代治疗的急性肾损伤患者,血管紧张II似乎也是一种很有前景的血管加压药。然而,由于证据有限和对安全性的担忧(由于与血管加压素显著活性相关的潜在不良反应,安全性仍不明确),血管紧张素II目前不建议用于脓毒性休克患者。我们需要通过进一步研究来更好地确定这些血管加压药在这些患者治疗中的作用。
介绍:
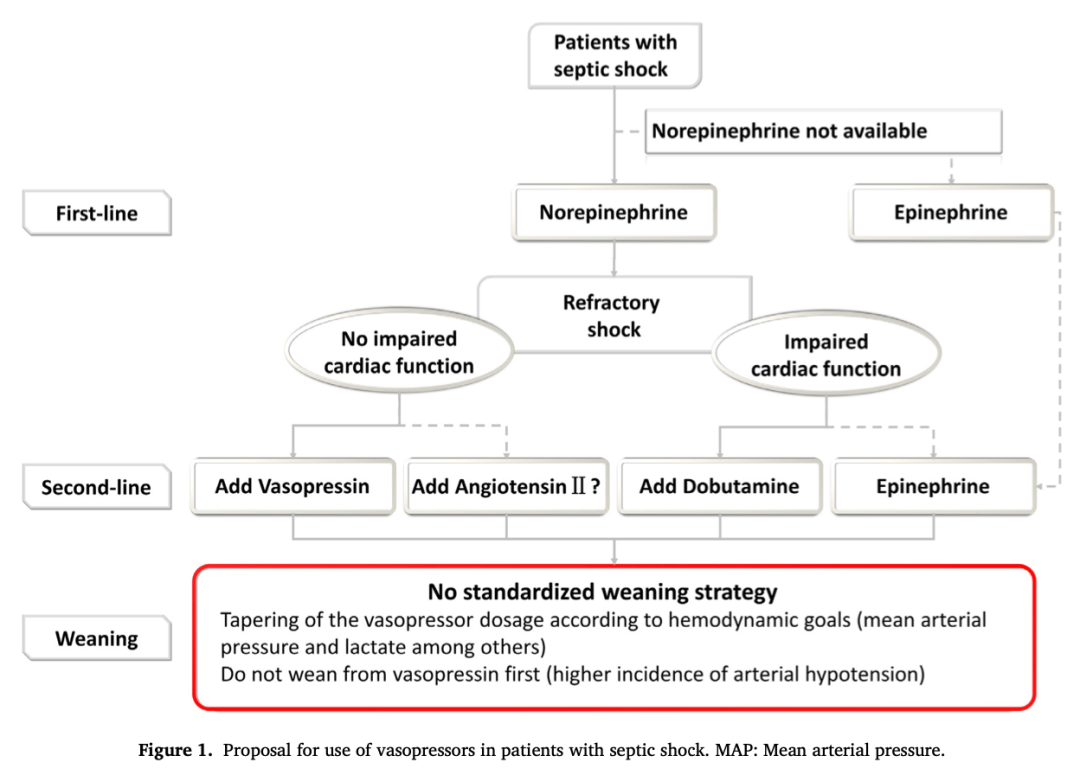
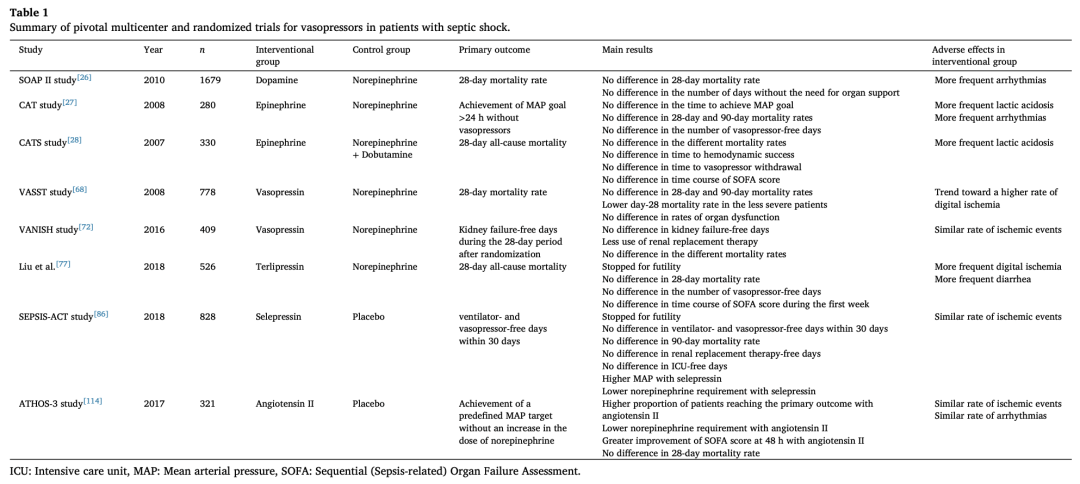
多巴胺:
肾上腺素:
加压素及其类似物:
血管加压素:
床旁使用血管加压素:
特利加压素
Selepressin
血管紧张素II:
肾素-血管紧张素-醛固酮系统在脓毒性休克中的作用
血管紧张素II在脓毒症中的应用:
亚甲蓝:
结论:
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫