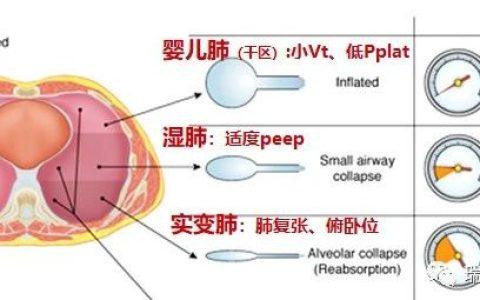
IPF 患者的自然病程异质性明显,大部分患者病情进展缓慢,可存活数年,也有部分患者在病程中出现短时间内的呼吸困难加重和肺功能急剧下降,这种突发的病情恶化有些可由已知原因的急性左心衰、肺栓塞、肺部感染等所致,而有些查不到明确的原因则被定义为 IPF 急性加重(AE⁃IPF)。下面我们一起来学习来自南京大学医学院附属鼓楼医院的曹孟淑教授,为我们带来的关于 AE-IPF/ILD 诊疗的经验分享。
AE-IPF/ILD 的概念及演变

AE-IPF/ILD 的发病率
AE-IPF/ILD 的发病率目前尚不明确。来自 IPF 临床实验的资料显示 AE-IPF 发病率为 5~15%。不同国家回顾性研究报道的发病率有差异。美国报道的年发生率 13%,韩国 1 年和 3 年的发生率为 14.2% 和 20.7%。日本 1~3 年的发生率为 8.6% ,12.6% 和 23.9%。汇报研究者认为中国的年发生率为 3.97~11.06%。CTD-ILD 估计 AE 年发生率为 1.25~7.2%,低于 IPF。
AE-IPF/ILD 的危险因素

AE-IPF/ILD 诊断



AE-IPF/ILD 治疗
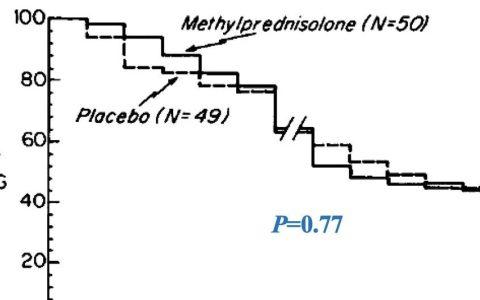
预后
总结
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫 

![[重症避错]: 心肺复苏后疼痛剌激反射消失持续24小时,眼球反射消失72小时,可以认为是永久性昏迷](https://www.icu.cn/wp-content/uploads/2021/12/OIP-C-480x300.jpg)