作者:陈棚棚1,杨杰1,金信浩2,张菠1,杨穗碧1,洪玉才1,倪红英3,章仲恒1,4,5*
作者单位:1.浙江大学医学院附属邵逸夫医院急诊医学科,浙江 杭州 310000;2.浙江大学医学院附属邵逸夫医院重症医学科,浙江 杭州 310000;3.金华市中心医院重症医学科,浙江 金华 321036;4.浙江省腹腔感染精准诊疗重点实验室,浙江 杭州 310000;5.绍兴文理学院医学院,浙江 绍兴 312000
基金项目:国家重点研发计划项目(2023YFC3603104,2022YFC2504503),国家自然科学基金项目(82272180,82472243),浙江大学龙泉创新中心项目(ZJDXLQCXZCJBGS2024016);浙江省自然科学基金华东医药企业创新发展联合基金资助项目(LHDMD24H150001);国家中医药管理局科技司-浙江省中医药管理局共建科技计划(GZY-ZJ-KJ-24082);浙江省医药卫生科技计划项目(2024KY1099);金华市科技局重点科技计划(2024-3-047)
DOI:10.12287/j.issn.2096-8965.20240406
通信作者简介
章仲恒,医学博士,主任医师/副教授,特聘研究员,博士生导师。浙江大学医学院附属邵逸夫医院急诊医学科副主任,浙江大学急救医学研究所副所长,浙江省医师协会急诊分会委员、浙江省医学会急诊青年委员,开展急危重症的临床大数据科研工作,发表SCI论著60多篇,被引超过8 000次,入选2021/2022爱思唯尔高被引学者。
【摘要】脓毒症是全球范围内的重大健康挑战之一,其复杂的病理机制和多器官功能损伤对患者生命构成了严重威胁。近年来,多模态组学技术结合机器学习在脓毒症研究中取得了显著突破,为早期诊断、精准治疗和个性化干预提供了新的前景。传统治疗手段如皮质类固醇、液体管理及抗生素的个性化调整,以及中医药与乌司他丁等在多模态组学研究中的应用,拓宽了脓毒症治疗的选择空间。中国脓毒症多模态组学研究联盟(CMAISE)通过整合基因组学、蛋白质组学、代谢组学等多模态组学数据,深入探索脓毒症的分子机制及生物标志物。本综述全面总结了多模态组学技术在脓毒症研究中的应用现状,并探讨了机器学习在个性化治疗中的潜力,为未来的临床应用及科研发展提供了理论依据和思路。
【关键词】脓毒症;多模态;组学
脓毒症是一种由宿主对感染反应失调引发的致命性器官功能障碍,已成为全球主要的健康挑战之一[1]。脓毒症显著特点是急性且严重的病情变化,伴随明显的生理、代谢和免疫功能紊乱。由于定义复杂且多变,临床诊断标准不断更新,旨在更精准地界定这一病理状态。最新的脓毒症-3定义强调了脓毒症的高致死率,凸显了早期识别和及时干预的重要性,以防止病情进一步恶化[1]。尽管医疗技术不断进步,脓毒症依然是住院患者死亡的主要原因之一,具有极高的死亡率和发病率,对全球医疗系统造成了沉重负担[2]。
近年来,多组学数据的兴起为揭示脓毒症背后复杂的生物学机制提供了全新视角。基因组学、转录组学、蛋白质组学和代谢组学等多模态数据涵盖了大量信息。然而,这些数据通常呈现出高维度、异质性和非线性等特征,传统的统计分析方法难以充分挖掘其潜在的生物学关联。相较之下,机器学习,尤其是深度学习和集成学习,展现了强大的数据处理和模式识别能力,能够从多组学数据中提取复杂特征与关系。随着多组学技术和机器学习方法的不断发展,脓毒症的个体化诊疗逐渐成为可能,为这一医学难题的解决带来了新的希望和突破(见图1)。
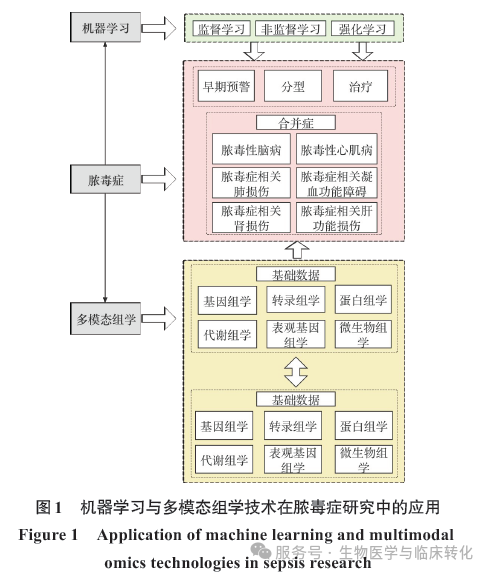
通过机器学习与多组学数据的结合研究脓毒症及其并发症。利用监督、非监督和强化学习方法,实现脓毒症的早期预警、分型与治疗优化。多组学(如基因组学、表观基因组学、微生物组学等)数据整合则提供了全面的分子信息,揭示脓毒症的生物学特征,为个性化诊疗提供支持。此策略有助于更好地理解并防治脓毒症及相关并发症。
1 组学的定义和多模态组学的进展
多模态组学技术能够深入挖掘与疾病及其亚型相关的生物信号,有助于从表型和内表型两个层次精确区分这些数据[3-4](见表1)。
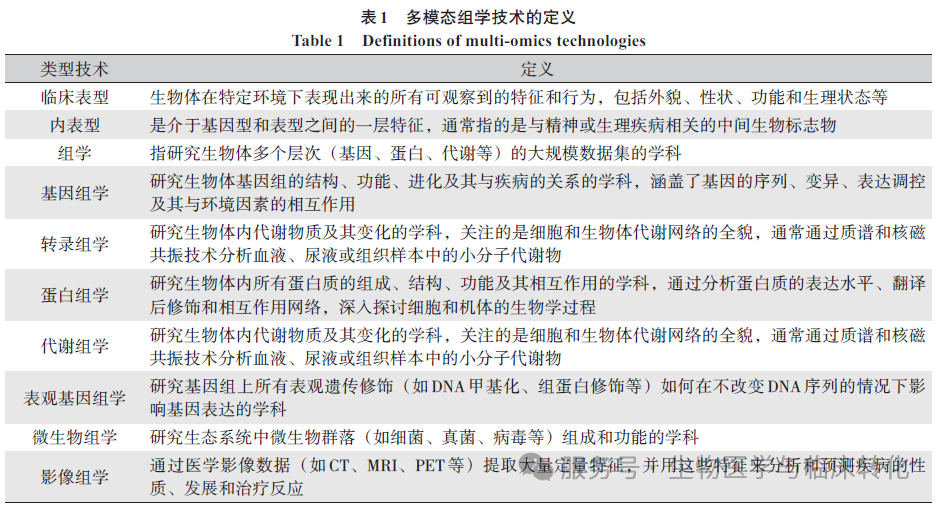
随着多组学技术的迅速发展,研究者能够从个体和群体中获取大量数据,为疾病的早期诊断和个性化治疗提供全新的视角[5]。在脓毒症研究中,通过多维生物学分析,多组学技术揭示了脓毒症背后的复杂分子机制[6]。结合临床特征的数据分析,多组学不仅有助于脓毒症的早期识别,还能预测并发症的发生,指导精准治疗并评估预后[3]。
具体而言,基因组学通过分析基因结构、功能和表达调控,识别与脓毒症易感性及严重程度相关的基因变异,推动了个性化治疗的发展[7]。表观遗传学研究基因表达调控机制(如DNA甲基化和组蛋白修饰),揭示了病原体感染引发的宿主表观遗传变化如何影响免疫反应[8]。转录组学通过检测脓毒症患者血液中的基因表达差异,识别病毒或细菌感染的特异性表达模式,提供新的诊断标志物,并预测不良预后[9]。蛋白质组学则关注蛋白质的表达变化,有助于区分感染性和非感染性系统性炎症反应综合征(Systemic Inflammatory Response Syndrome,SIRS),评估炎症反应的严重程度,并发现潜在的药物靶点[10]。代谢组学揭示了脓毒症患者能量危机与线粒体功能障碍的关系,发现脂肪酸代谢紊乱与免疫反应的相关性,进一步表明线粒体在脓毒症中的核心作用[11]。此外,药物基因组学和药物代谢组学通过分析药物代谢及其遗传学基础,为个体化治疗提供了有力支持[12]。
多组学技术的集成分析将多种生物数据结合,构建了脓毒症的系统生物学模型,为其诊断和预后提供了全新框架,推动了精准医疗的快速发展。例如,影像组学通过从标准临床影像中提取大量数字信息,结合人工智能模型预测脓毒症的临床结局。Li等[13]开发的模型结合了影像组学与临床特征,能够早期预测脓毒症诱发的急性呼吸窘迫综合征的发生及其严重程度。Boutin 等[14]通过影像组学分析,预测了腹腔感染性脓毒症患者在重症监护室(Intensive Care Unit,ICU)中的死亡风险及急性肾损伤的发生率。此外,心电图数据的应用在脓毒症研究中也取得了显著进展。通过收集心电图数据并应用深度学习模型,研究者能够提取隐藏特征,开发脓毒症筛查工具并验证其有效性[15]。例如,心电图异常已被用于评估新冠病毒感染患者的死亡风险,为临床预后提供了分层依据[16]。心电图标记物作为交感神经兴奋毒性的替代指标,也可用于预测术后感染[17]。自然语言处理(Natural Language Processing,NLP) 技术同样展现出巨大潜力。在脓毒症患者的诊疗中,Ⅴermassen 等[18]通过Intersystems iKnow®NLP 应用开发了一种自动化搜索策略,有效筛选电子病历数据,识别脓毒性休克患者,效果优于传统的ICD-9 编码方法。Patel等[19]则利用NLP 分析研究了儿童多系统炎症综合征与新冠抗原阴性脓毒症患者之间的血浆蛋白质差异,揭示了潜在的早期识别方法。
2 机器学习的定义和研究进展
机器学习作为人工智能的核心分支,已经在医疗领域展现出巨大的潜力[20]。通过对算法的开发与应用,机器学习系统能够从样本数据和历史经验中学习,识别大规模数据集中隐藏的变量关联,执行分类任务,并基于基线特征预测。随着硬件性能和软件技术的持续进步,尤其是在深度神经网络等先进框架的推动下,机器学习技术取得了飞速发展。这些框架能够处理复杂的生物医学数据,使机器学习成为医疗数据分析的关键工具。
在脓毒症研究中,机器学习被广泛应用于挖掘组学数据中的潜在模式,并用于患者分类,识别具有不同生物特征的亚群,从而揭示脓毒症的异质性。通过将患者划分为不同的内表型,并与临床结局结合,进一步揭示脓毒症的多样性[21-22]。这一分类过程不仅深化了研究者对脓毒症病理机制的理解,还为个性化治疗提供了新的可能性,使治疗方案能够依据患者的具体内表型特征进行个体化定制。尽管研究[22]表明,这些内表型与脓毒症患者的临床特征密切相关,但其背后的分子机制仍有待进一步揭示。未来的研究应继续探索这些内表型的分子基础,尤其是通过更精细的组学分析和多层次的生物数据整合(如基因组、转录组、代谢组等),并借助更复杂的机器学习模型,发现新的生物标志物和疾病通路。
此外,随着机器学习技术的不断进步,特别是在深度学习领域,未来的研究将变得更加自动化和精准,能够处理规模更大、结构更复杂的数据集,并从中提取出有临床意义的信息。这不仅将推动脓毒症研究的深入发展,还将为患者提供更加高效的诊断和治疗手段。通过这一路径,机器学习不仅为脓毒症研究提供了强大的理论支持,也加速了医疗领域个性化和精准化的实践进程。
3 多模态组学在脓毒症诊疗中的进展
3.1 通过机器学习早期预警
在脓毒症的早期检测中,尽管机器学习技术能够比传统临床判断更早地发现潜在的临床事件[23-24],但医务人员的干预率仍然较低,尤其是针对那些未表现出明显不稳定迹象的患者。这种现象主要源于机器学习模型的可解释性不足,导致医务人员对其不信任,并产生“警报疲劳”。虽然一些机器学习算法展现了较高的受试者工作特征曲线下面积评分,但缺乏透明性依然限制了其在临床中的广泛应用[25]。研究[26]表明,可以通过优化警报系统的设计等方式,尤其是使用直观的可视化工具(如颜色编码或在关键位置的显示屏上增强警报提示),能够显著提高医务人员的响应率,并降低脓毒症的发病率。
目前,许多机器学习算法已在不同的临床场景中得到验证[27-28]。Alge 等[29-30]利用特权信息和连续生理信号(特别是心电图和电子健康记录数据)预测脓毒症进展风险的方法。一项研究[31]探索了利用6 项生命体征进行脓毒症预测的算法,能够提前48 h 预测脓毒症。该算法在两家医院的数据集上表现出良好的泛化能力,表明机器学习在改善脓毒症早期诊断和治疗方面具有巨大潜力。另一个名为NAⅤOY® Sepsis 的机器学习算法,通过分析4 h内收集的生命体征、血气值和实验室数据,成功提前3 h 预警ICU 患者脓毒症的发生,显示出较高的准确性[32]。
在特定病种的脓毒症诊断中,Tran 等[33]开发了机器智能学习优化器的自动化机器学习平台,用于生成预测烧伤患者脓毒症的模型。Liu 等[34]基于13个预测因子构建了基于梯度提升决策树的模型,成功预测了急性胰腺炎患者的脓毒症风险,显示出良好的预测性能。Palma等[35]使用Luminex多因子检测技术检测血浆中的36种可溶性因子,发现CXCL10、IL-2、IL-10和IL-22 等生物标志物与坏死性筋膜炎的临床表型相关,而G-CSF、S100A8和IL-6能预测坏死性筋膜炎患者的脓毒性休克。针对儿童脓毒症的早期诊断,Lamping 等[36]开发并验证了一种基于常规数据的模型,用于区分儿科非感染性SIRS与脓毒症(见表2)。


3.2 利用多模态组学寻找生物标志物
脓毒症早期诊断的主要挑战在于如何有效区分其与其他类似病症(如SIRS),因为这些疾病在临床表现(如生命体征变化、发热)和分子特征(如宿主反应失调)上有很大的相似性[41-42]。生物标志物作为脓毒症诊断的辅助工具,虽然展现了一定的潜力,但由于敏感性和特异性不足[43-44],至今没有单一或组合的生物标志物被广泛接受。研究[45]发现,60 种生物标志物能够区分脓毒症和SIRS,但仅有7 种标志物(如PCT、预素、CRP、IL-6、sTREM1、LBP 和CD64)具有较充足的数据支持。然而,这些标志物在实际应用中仍有局限性,如单独使用时的诊断和预后准确性较低,浓度会随脓毒症的不同阶段变化,且缺乏统一的诊断临界值。
为应对传统生物标志物的局限,数据驱动的生物标志物发现逐渐成为新兴趋势。除了已有的PCT、CRP 等标志物,目前的研究着重发掘那些能反映脓毒症早期免疫反应、代谢紊乱和微环境变化的分子。例如,通过机器学习和多组学方法,研究[46]已揭示中性粒细胞亚群的关键基因(如ALPL、ACTB、CD177、S100A8、S100A9 等),这些标志物在中性粒细胞脱颗粒、激活及免疫功能中具有重要作用,未来应进一步验证这些基因在不同脓毒症表型中的诊断和预后价值。此外,外周T 淋巴细胞亚群、γδT 细胞的免疫表型变化,尤其是与脓毒症患者预后密切相关的CD28、OX40 等共刺激分子,也为潜在的生物标志物提供了新的研究方向[47-48]。
除了免疫相关标志物,代谢组学也为脓毒症的早期诊断和治疗提供了新的思路。例如,苯丙氨酸代谢在脓毒症中的作用已经被发现[38],而血浆甲基硫腺苷水平则与脓毒症的死亡风险密切相关[49]。这些代谢物作为潜在的预后标志物,需要进一步的临床验证和标准化。此外,代谢组学与基因组学的结合,尤其是通过多模态组学技术,能够揭示脓毒症中的系统性生物学变化,为新治疗靶点的发现奠定基础。
总的来说,未来的脓毒症研究应集中在以下3个方面:第一,继续深入挖掘新型生物标志物,尤其是那些能够反映脓毒症免疫反应、代谢变化及器官功能损伤的分子;第二,利用多模态组学技术全面解析脓毒症的复杂机制,识别潜在的治疗靶点;第三,推动机器学习等数据驱动的方法,结合多维度临床数据,提高脓毒症的早期诊断率和治疗效果。
3.3 基于多模态组学的脓毒症分型
近年来,研究[22]通过基因表达和分子分型深入探讨了脓毒症的异质性,为个性化治疗提供了新的方向。Davenport 等[50]通过外周血白细胞的全基因组转录组分析,将脓毒症患者分为2 类主要的脓毒症反应特征组(Sepsis Response Signatures,SRS):SRS1 和SRS2。SRS1 群体表现出免疫抑制特征,且与较高的14 d 死亡率相关;SRS2 群体的免疫反应较为正常,预后较好。此外,eQTL 分析揭示脓毒症患者的基因表达受特定遗传变异的影响,如HIF1A 和MTOR 基因变异,这些发现为开发个性化治疗提供了潜在的生物学基础。
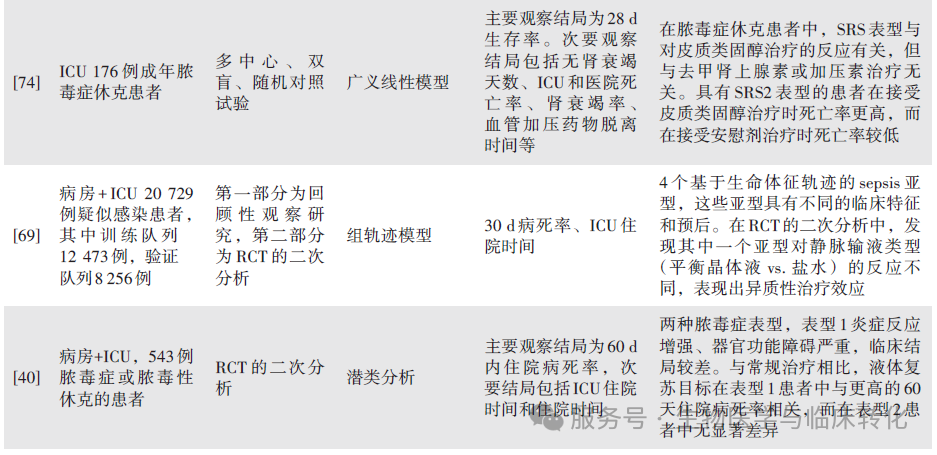
DeMerle 等[40]基于ProCESS 随机临床试验的数据和蛋白质生物标志物,识别出一种高度炎症性的脓毒症表型。通过分析20 个临床和生物标志物变量,发现表型1 的60 d 院内死亡率显著高于表型2的。与通常治疗相比,早期目标导向治疗仅在表型1 患者中与更高的60 d 院内死亡率相关。Seymour等[51]通过脓毒症小鼠模型,在临床恶化之前确定了2 种表型。其中,表型2 为“不太健康”的表型,表现为更快恶化、更严重的炎症反应,且对治疗更敏感;表型1 则相对“健康”,病情恶化较慢,炎症反应较弱,对治疗的敏感性较低。另外一项研究[52]通过分析脓毒症患者的数据,识别出与宿主反应模式和临床结果相关的4 种临床表型:α 表型病情较轻、β 表型年龄较大且伴有较高的慢性疾病负担、γ 表型表现为炎症反应活跃,δ 表型则表现为严重器官功能障碍。另一项基于全基因组表达谱的研究[9]识别出4 种脓毒症分子内表型(Mars1-4),其中Mars1 内表型与高死亡率相关,表现为先天性和适应性免疫功能的显著下降;Mars2 和Mars4 则与高炎症状态相关;Mars3 内表型则表现出适应性免疫基因的上调,预后较好且风险较低。此外,通过对脓毒症患者的转录组进行无监督聚类分析,识别出3 种宿主反应亚型:炎症性、适应性和凝血性。炎症性亚型患者的固有免疫活化水平较高,死亡率也较高;适应性亚型病情较轻,死亡率较低;凝血性亚型则伴随凝血障碍,预后较差[53]。这些研究揭示了脓毒症的分子异质性,强调了个性化治疗的重要性。
在儿科的感染性休克中,基因分型研究发现了3 种不同的亚型(A、B、C)。亚型A 患者表现出更严重的疾病、器官衰竭和较高的死亡率,其基因表达特征为适应性免疫系统和锌代谢相关基因的抑制;相对而言,亚型B 和亚型C 患者的基因表达和临床表现较为轻微[54]。
3.4 利用多模态组学研究脓毒症合并症
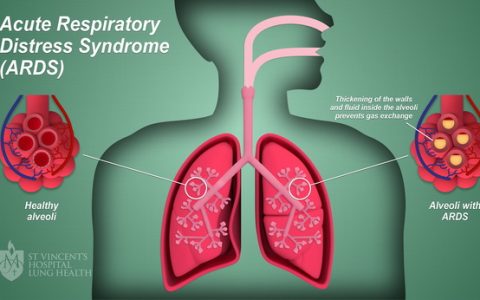
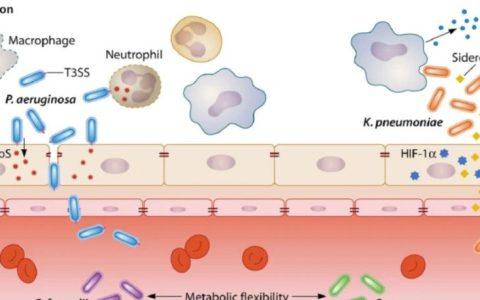
脓毒症的严重性主要源于其引发的多脏器功能损伤,这是全身性炎症反应导致器官受损的核心原因。感染激活免疫系统后,释放大量炎症介质,导致血管内皮细胞损伤、血管通透性增加和微循环障碍,进而引发急性肾损伤(Acute Kidney Injury,AKI)、急性呼吸窘迫综合征、肝功能衰竭和心肌抑制等多器官功能障碍综合征。这一过程进展迅速,预示预后不良并大幅增加死亡率[1]。为揭示脓毒症相关的复杂分子机制,多组学分析和机器学习技术被广泛应用,以整合基因、蛋白质和代谢物等数据,识别出与器官损伤相关的关键生物标志物和分子通路。
AKI是脓毒症最常见的并发症之一,全球发病率为5%~50%,且与较高的死亡率密切相关[55]。传统的AKI诊断依赖血清肌酐水平,但其在早期诊断中的敏感性较低。机器学习算法(如XGBoost)结合患者的人口统计数据和炎症标志物,开发了用于预测脓毒症相关AKI的高效模型,极大地提高了预测准确性[56]。从临床应用角度看,这些研究不仅提高了AKI的早期诊断能力,还推动了个性化治疗的进步。基于不同AKI表型的患者可以接受更为精准的治疗策略,例如预测哪些患者可能需要更积极的肾替代治疗[57]。
研究[58]表明,在感染性休克引发的心肌损伤中,补体、凝血和炎症相关标志物(如补体蛋白C2、C3、C5,凝血因子ⅩⅢ,纤维蛋白原,以及炎症介质IL-6和TNF-α等)在心肌病变中可能发挥重要作用。无监督聚类分析将心肌损伤患者分为3 个亚组(C1、C2、C3),其中C1 亚组的预后较好,表明吞噬作用在脓毒症心肌病中具有重要性[59]。此外,机器学习识别出与心肌损伤相关的6 个关键基因(如ATP11C、MAPK3),RNA 测序进一步验证了其在预后中的重要性。
针对脓毒症相关性脑病(Sepsis-Associated Encephalopathy,SAE)的研究通过RNA-seq 和代谢组学,利用主成分分析等方法揭示了海马区炎症反应和神经元损伤的关键机制,尤其是促炎因子上调及代谢通路紊乱,突显了PI3K-Akt 和钙信号通路在SAE 发病中的作用[43],为理解SAE 的分子基础提供了重要依据。
凝血功能障碍是脓毒症的常见并发症,尤其在新冠病毒感染患者中,表现为高D-二聚体和纤维蛋白原水平,增加了血栓形成的风险[60]。多组学分析[61]揭示,新冠病毒感染患者的促凝血活性增强,可能与血小板活化、内皮损伤和细胞因子风暴有关。研究[62]显示,新冠病毒感染脓毒症患者的抗凝血酶Ⅲ和蛋白C水平下降,提示凝血系统失衡可能是其主要致死机制。
脓毒症引起的多脏器损伤及其并发症显著影响患者的预后。多组学分析和机器学习技术提供了深入了解脓毒症复杂机制的工具,尤其帮助早期识别高风险患者并进行个性化干预。随着技术的不断进步,相关研究成果有望转化为临床应用,为脓毒症患者提供更精准的治疗方案,显著改善临床结局。
3.5 脓毒症治疗的研究进展
3.5.1 早期抗生素治疗
抗生素在脓毒症治疗中至关重要,“拯救脓毒症运动”建议在发病后1 h 内使用抗生素,因为每延迟1 h 会导致生存率下降4%~6%[1]。基于多组学数据的精准治疗策略,还可以识别对抗生素反应较差的患者,帮助临床医生调整治疗方案,从而改善预后。Worapratya 等[63]利用聚类分析发现,使用适当抗生素治疗的严重脓毒症和脓毒性休克患者的死亡率显著低于使用不适当抗生素治疗的患者。此外,Schinkel 等[64]通过对PHANTASi 试验的二次分析发现,早期抗生素治疗显著提高了年轻脓毒症患者的28 d 生存率,但对老年患者的效果相对不明显,因此年轻患者应尽早开始抗生素治疗,而老年患者则可以适当延迟,待确诊后再进行抗生素治疗。
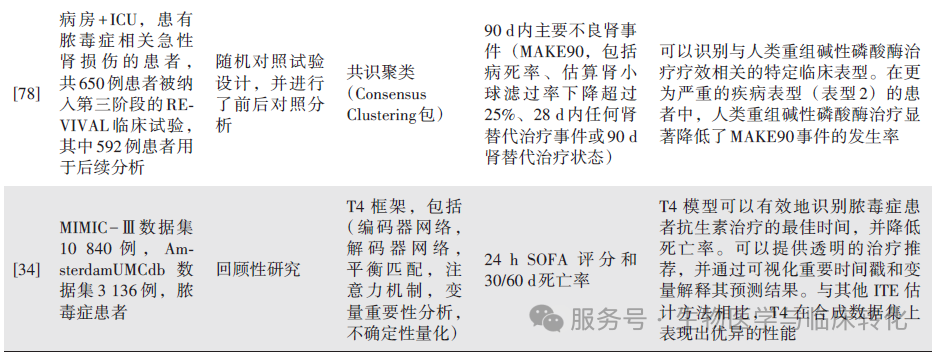
Ates 等[65]通过机器学习方法评估了治疗药物监测(Therapeutic Drug Monitoring,TDM) 在感染性休克患者中的作用。研究利用数据驱动框架动态追踪患者对药物的反应,发现基于TDM 指导的培卡西林/他佐巴坦治疗显著提高了患者的恢复率。Zheng 等[37]通过机器学习算法识别出能够区分脓毒症患者和革兰阳性菌、革兰阴性菌感染的特定生物标志物,为早期抗生素使用提供了科学依据。这些生物标志物的代谢途径分析揭示了脓毒症与异常氮代谢、细胞呼吸障碍及多器官衰竭的关联。此外,Liu 等[66]开发的T4 模型是一种抗生素治疗时间推荐系统,能够精准识别脓毒症患者的最佳治疗时机,并通过可视化重要时间点和变量解释预测结果,从而进一步降低了患者的死亡率。
3.5.2 液体复苏
液体治疗在脓毒症患者的管理中至关重要。Messmer 等[67]使用随机森林、多变量逻辑回归、快速傅里叶变换(Fast Fourier Transform,FFT)和决策树(Decision Tree,DT)等机器学习模型,预测重症患者液体过载的风险。结果显示,随机森林模型的预测准确性最高,其次是多变量逻辑回归、FFT 和DT 模型。一项研究[68]比较了脓毒症低血压患者,最初24 h内使用限制性液体策略(早期使用血管加压药)与自由液体策略的效果,发现尽管限制性液体组的患者使用了更多血管加压药且持续时间更长,两种策略在90 d内的死亡率和ICU住院时间等预后结果没有显著差异。表明早期优先使用血管加压药或液体的策略对预后影响不大。
Bhavani等[69]发现了4个基于生命体征轨迹的脓毒症亚型,这些亚型在临床特征和预后上存在差异。在随机对照试验(Randomized Controlled Trial,RCT)的二次分析中,发现其中一个亚型对静脉输液类型(平衡晶体液与盐水)的反应不同,呈现出异质性治疗效应,表明脓毒症亚型可能对不同治疗策略的反应存在差异。Bataille等[70]利用机器学习技术分析心脏超声数据,预测患者的液体反应性,发现机器学习模型在预测液体反应性方面的效果与传统的被动抬腿试验相当,尤其是偏最小二乘回归模型能够识别出关键的心脏超声参数,表明机器学习有望成为预测液体反应性的有效工具。Su等[71]利用强化学习为ICU中的感染性休克患者开发了一种液体治疗平衡策略。由于不同医生对液体治疗的判断差异较大,强化学习算法能够有效预测液体治疗策略。研究中使用的强化学习算法SARSA 模型模拟了液体治疗的预期和实际死亡率之间的关系,而深度Q 学习(Deep Q-learning)模型则表明,液体平衡预测越接近实际结果,患者的死亡率越低。这些表明机器学习和强化学习技术在优化脓毒症患者的液体管理中具有潜力,不仅可以帮助预测液体过载和反应性,还能通过个性化策略改善治疗效果。
3.5.3 糖皮质激素的应用
糖皮质激素因其抗炎和免疫抑制作用,广泛用于脓毒症的治疗,但其对生存率的影响仍存在争议[72]。多组学研究,特别是蛋白质组学和代谢组学的结合,揭示了类固醇在脓毒症中的复杂作用机制。例如,蛋白质组学分析显示,糖皮质激素可以调节脓毒症患者体内的炎症和抗炎蛋白质网络,从而优化免疫反应[73]。基于这些发现,多组学分析为个性化类固醇治疗提供了新的视角,帮助临床医生识别最佳的使用时机和剂量,从而减少副作用并提高疗效。
Antcliffe 等[74]进一步探讨了皮质类固醇在感染性休克中的效果,发现SRS在不同患者中具有重要影响。表明SRS2 表型的患者在接受氢化可的松治疗时,死亡率更高。这一发现可能解释了不同研究中类固醇对生存率影响的差异,提示未来的临床试验应根据SRS 表型进行分层治疗。此外,在新冠病毒感染相关的脓毒性休克研究中,研究者确定了IFNγ/IL-10 是一个重要的生物标志物,可用于决定是否应使用氢化可的松治疗。这一标志物有助于指导个体化的治疗决策,提高治疗效果,减少不必要的药物使用[75]。
3.5.4 个性化治疗
随着多组学技术的快速发展,个性化治疗逐渐成为脓毒症治疗的研究热点。通过分析患者的基因组、转录组、蛋白质组和代谢组数据,能够识别出每位患者独特的免疫学表型,从而制定更精准的治疗方案。这种基于多组学数据的精准医学方法,不仅提高了治疗的有效性,还能减少不必要的副作用。例如,在新冠病毒感染相关脓毒症的治疗中,多组学数据揭示了高密度脂蛋白胆固醇(High-Density Lipoprotein,HDL)功能的变化,为重组HDL(rHDL)的个性化应用提供了指导,显著改善了患者的临床结局[76]。Kudp 等[77]研究表明,重组人凝血调节素仅对伴有严重凝血障碍的重症脓毒症患者有效,显著降低了这类特定分型患者的病死率,进一步证明了个性化治疗在脓毒症中的重要性。
此外,Bruse 等[78]研究了人类重组碱性磷酸酶在脓毒症相关急性肾损伤患者中的表型特异性治疗效果,表明这种治疗方式具有潜在的优势。Hajjej等[79]通过一项RCT评估了左西孟旦对感染性休克患者肌肉细胞能量代谢的影响,结果显示,左西孟旦通过改善微循环中的氧输送,显著提升了肌肉细胞的葡萄糖和乳酸代谢。这种基于患者代谢特征的个性化治疗策略展示了其在脓毒症管理中的潜力,不仅为精准医疗提供了新方向,也推动了更有效的临床干预方案的发展。
3.5.5 中医的作用
中医在脓毒症的治疗中展现了独特的作用,其机制得到了基因和分子层面的验证支持。一项研究[80]系统探讨了羟基红花黄色素A 在减轻脓毒症引起的肝损伤中的潜在机制。发现羟基红花黄色素A能通过调节肠道微生物组成、改善肝代谢紊乱、降低炎症反应、增强肠道屏障功能,以及调节肝氧化应激,显著降低脓毒症小鼠的死亡率,并改善肝的生物化学指标和组织病理学表现。这些发现为羟基红花黄色素A在脓毒症相关肝损伤治疗中的应用提供了理论支持和临床潜力。
另一项研究[81]探讨了大柴胡汤对感染性肠损伤的作用机制。通过动物模型和多组学分析表明,大柴胡汤能调节肠道微生物群、增强谷胱甘肽代谢、降低炎症因子水平、改善肠道屏障功能,从而减轻感染性肠损伤的病理变化,且无明显的肝毒性和肾毒性。表明大柴胡汤在治疗感染性肠损伤方面具有安全性和疗效。此外,通过网络药理学和多组学方法,研究者[82]探讨了四逆汤和血必净在脓毒症治疗中的潜在机制。发现四逆汤通过靶向CX3CR1 基因,调节氧化应激和脂质代谢,从而改善脓毒症患者的预后;血必净则通过调节NF-κB信号通路,发挥抗炎作用,进一步支持其在脓毒症治疗中的应用潜力[83]。这些研究结合多组学分析,揭示了中药在脓毒症治疗中的多靶点作用机制,不仅为中医药的临床应用提供了新的思路,也展示了其在脓毒症治疗中的广阔前景(见表3)。

3.6 利用多模态组学预测脓毒症预后
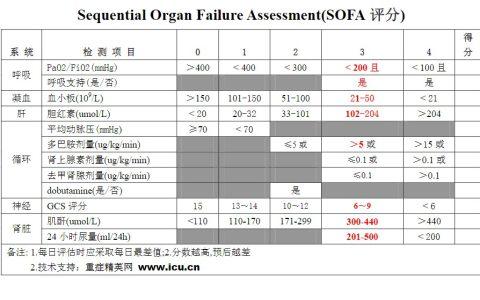
针对脓毒症患者的预后,多个研究通过机器学习和生物信息学技术探索了精准预测模型。Pan等[84]开发了基于SOFA 评分的逻辑回归和朴素贝叶斯模型,用于预测ICU病房中脓毒症患者的院内死亡率。Guo 等[85]利用MIMIC-Ⅲ和MIMIC-Ⅳ数据库,通过k-means 聚类分析脓毒症患者表型,并结合卷积神经网络和双系数二次多变量拟合函数预测28 d 生存率。研究将患者分为4 个集群,第4 集群预后最差,表现出脓毒症凝血功能障碍的特征。此外,Yang 等[86]通过RNA 测序数据和DNA 甲基化分析,构建了一个包含9 个基因的预后标记模型,并通过风险评分系统将脓毒症患者分为高风险组和低风险组,验证了该模型的有效性。进一步免疫浸润分析和基因集富集分析揭示了这些基因与脓毒症预后之间的密切关联,为临床提供了可靠的生存预测工具。
这些模型不仅提高了对高风险患者的早期识别能力,支持了临床精准管理,还为理解脓毒症的分子机制提供了新视角。未来的研究应继续优化这些预测模型,扩大样本量,并验证其在不同人群和临床环境中的适用性,以进一步提升脓毒症患者的生存率和生活质量。
4 中国脓毒症多模态组学研究联盟(Chinese Multi-Omics Advances In Sepsis,CMAISE)
CMAISE 是中国首个专注于脓毒症多组学研究的组织,成立于2020 年,致力于通过多中心、多组学的研究项目深入探究脓毒症的分子机制和临床特征。CMAISE收集了大量脓毒症患者的临床数据和生物样本,结合基因组学、蛋白质组学、代谢组学等技术,旨在通过多维数据分析揭示脓毒症的生物标志物和潜在治疗靶点,提升早期诊断率,优化治疗方案,改善患者预后,并已发表了多篇关于脓毒症研究的文章,涵盖AKI、中性粒细胞异质性以及脓毒症异质性的“疾病轴”表征等领域[87]。
其中一项关于脓毒症相关AKI的研究通过分析临床数据和转录组数据,探讨了其病理机制和预后情况。研究将患者根据肾功能轨迹分为4 类:无AKI、暂时性AKI、持续性AKI和恶化性AKI,发现持续性AKI患者病情最重,SOFA 评分最高,而恶化性AKI患者尽管初期症状较轻,但乳酸水平较高,且血管活性药物的使用时间较长[88]。转录组分析显示,暂时性和持续性AKI患者之间存在数百个差异表达基因,这些基因主要与适应性免疫和体液免疫通路相关。基于这些数据,研究开发的支持向量机模型在预测持续性AKI方面显示出高度准确性,提供了新的生物标志物和预测工具。此外,CMAISE还发表了一篇关于乌司他丁在脓毒症中免疫调节作用的文章。通过整合单细胞和群体RNA测序数据发现,乌司他丁通过调节中性粒细胞活性、下调中性粒细胞激活和脱颗粒相关基因的表达来发挥其作用。同时,乌司他丁显著增加了髓系来源抑制性细胞的数量,细胞间通讯分析揭示了其作用的关键信号通路[89]。这项研究为理解乌司他丁在脓毒症治疗中的免疫调节机制提供了新的视角,进一步支持了其临床应用潜力。
5 小结
脓毒症是一种由多种因素引发的复杂疾病,伴随着炎症反应和多器官损伤。多组学技术,如基因组学、蛋白质组学和代谢组学,以及机器学习技术,为深入解析脓毒症的异质性和精准治疗提供了全新的工具。通过将现代科技与传统医学相结合,脓毒症的治疗正朝着更加精准和高效的方向发展。未来的研究应继续致力于探索新的生物标志物和治疗靶点,为个性化治疗提供坚实依据,并推动临床实践的进一步优化。
(参考文献略)
学术交流文章,不做为临床依据,特此声明。发布者:Chu,转转请注明出处:https://www.icu.cn/?p=17726

 微信扫一扫
微信扫一扫