摘要
碳青霉烯类耐药鲍曼不动杆菌(CRAB)菌株的全球蔓延对医疗系统构成了严峻挑战,特别是在重症监护环境中,其治疗选择有限且死亡率居高不下。本综述探讨了导致碳青霉烯类耐药的流行病学特征和分子机制,包括多种β-内酰胺酶(尤其是OXA型酶)的产生、孔蛋白缺失、外排泵过表达以及抗生素靶位点突变。文章讨论了新兴治疗策略,如新型β-内酰胺-β-内酰胺酶抑制剂组合(例如舒巴坦-度洛巴坦)、铁载体头孢菌素、新一代多黏菌素,以及zosurabalpin和利福布汀(注射剂型,BV100)等新型药物。
同时评估了替代疗法——包括噬菌体疗法、抗菌肽、基于CRISPR的基因编辑和纳米颗粒递送系统——在规避传统耐药机制方面的潜力。此外,强调了人工智能和多组学整合技术在识别新药靶点和预测耐药谱方面的应用进展。这些创新共同构成了应对CRAB感染的多维策略,但其成功实施仍需进一步的临床验证和协同监测。本分析强调迫切需要持续投资创新疗法和有效的耐药监测,以遏制CRAB传播并保护最后防线抗生素的有效性。
关键词:鲍曼不动杆菌;碳青霉烯类耐药;β-内酰胺酶;替代疗法;噬菌体疗法;外排泵;抗菌肽;人工智能
1. 碳青霉烯类耐药鲍曼不动杆菌(CRAB)的出现
20世纪70年代初,不动杆菌属分离株通常对多种抗生素敏感,包括庆大霉素、米诺环素、萘啶酸、氨苄西林和羧苄西林,无论是单药治疗还是联合用药。然而自1975年起,几乎所有抗菌药物组的耐药性均呈上升趋势,治疗选择逐渐受限。
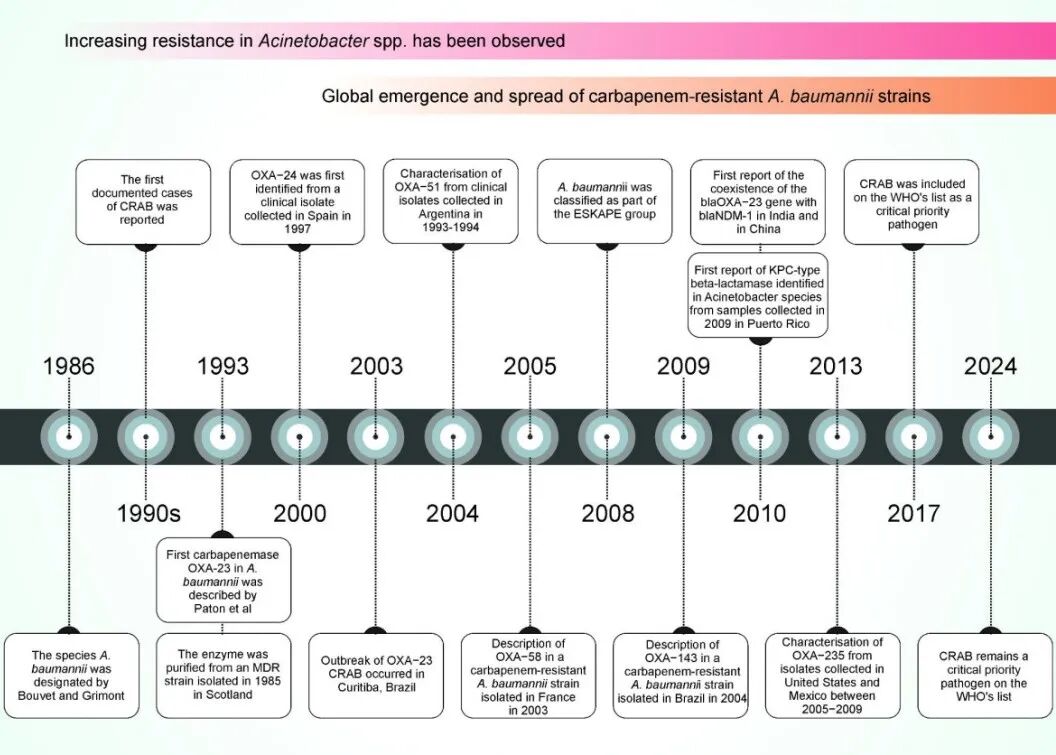
至20世纪80年代末和90年代,对亚胺培南耐药的鲍曼不动杆菌菌株在全球出现和传播,显著限制了治疗选择。碳青霉烯类成为对抗多重耐药(MDR)鲍曼不动杆菌感染的唯一有效药物。首例CRAB病例于1991年被报道,随后数年耐药率持续上升,对临床管理构成日益严峻的挑战。图1展示了耐药性出现的时间线。
一项系统综述分析了世界卫生组织定义的欧洲(EUR)、东地中海(EMR)和非洲(AFR)地区重症监护病房(ICU)的CRAB感染情况,报告合并发病率为每1000例患者41.7例(95%CI 21.6-78.7),发病密度为每1000患者日2.1例(95%CI 1.2-3.7)。此外,CRAB菌株导致ICU内13.6%(95%CI 9.7-18.7)的医院获得性感染,凸显了其在这些地区的临床重要性。
然而,鲍曼不动杆菌感染的全球流行病学特征(包括由碳青霉烯类耐药菌株引起或非耐药菌株引起的感染)具有高度异质性。欧洲疾病预防控制中心最新点流行率调查(2022-2023年)显示欧洲各国存在显著差异,在科索沃鲍曼不动杆菌占医院相关感染的17.6%,而在比利时、爱尔兰、卢森堡、马耳他和荷兰则不足0.1%。这种差异受多种因素影响,包括气候、感染控制基础设施和抗生素管理实践。值得注意的是,鲍曼不动杆菌具有明显的克隆性,易通过暴发传播,常在资源有限或感染预防策略欠佳的环境中蔓延。
中东和南亚地区(2012-2022年)耐药模式的系统综述进一步反映了这种区域差异性:血流感染中碳青霉烯类耐药率较高,土耳其为0.95(95%CI:0.92-0.97,n=1193),伊朗为0.82(95%CI:0.75-0.88,n=159),巴基斯坦为0.65(95%CI:0.17-1.00,n=240)。根据世界卫生组织全球抗菌素耐药性和使用监测系统(GLASS)仪表板最新数据(2022年),不动杆菌属血流感染(BCIs)表现出高碳青霉烯类耐药率,45,485例中有40,657例(89%)显示耐药。
基于全基因组的分子流行病学研究显示,国际克隆(IC)2构成了分布最广的鲍曼不动杆菌克隆谱系,在非洲、亚洲、欧洲、大洋洲和北美最为流行[20,21]。对超过15,000个公开基因组的最新分析表明,在国际克隆2(IC2)分离株中出现了一个流行超级谱系。值得注意的是,与其他地区不同,IC5和IC7在南美洲最为流行[20,21]。全球约66.9%至92.2%的鲍曼不动杆菌分离株携带获得性碳青霉烯酶基因,其中blaOXA-23-like和blaOXA-40-like基因最为普遍。令人担忧的是,碳青霉烯酶基因的全球流行率似乎随时间推移而上升,从2000-2014年收集分离株的66%上升至2024年收集分离株的96.2%。这一增长可能部分源于对碳青霉烯酶阳性分离株的测序偏好。
2. 鲍曼不动杆菌碳青霉烯类耐药的分子机制
CRAB的产生可能涉及酶促降解、膜通透性降低、抗生素主动外排和外膜修饰等多种机制的协同作用,这些机制共同增强了病原体在最后防线抗菌药物存在下的生存能力。理解耐药性的分子基础对制定靶向治疗策略至关重要。图2展示了CRAB的这些耐药机制概况。
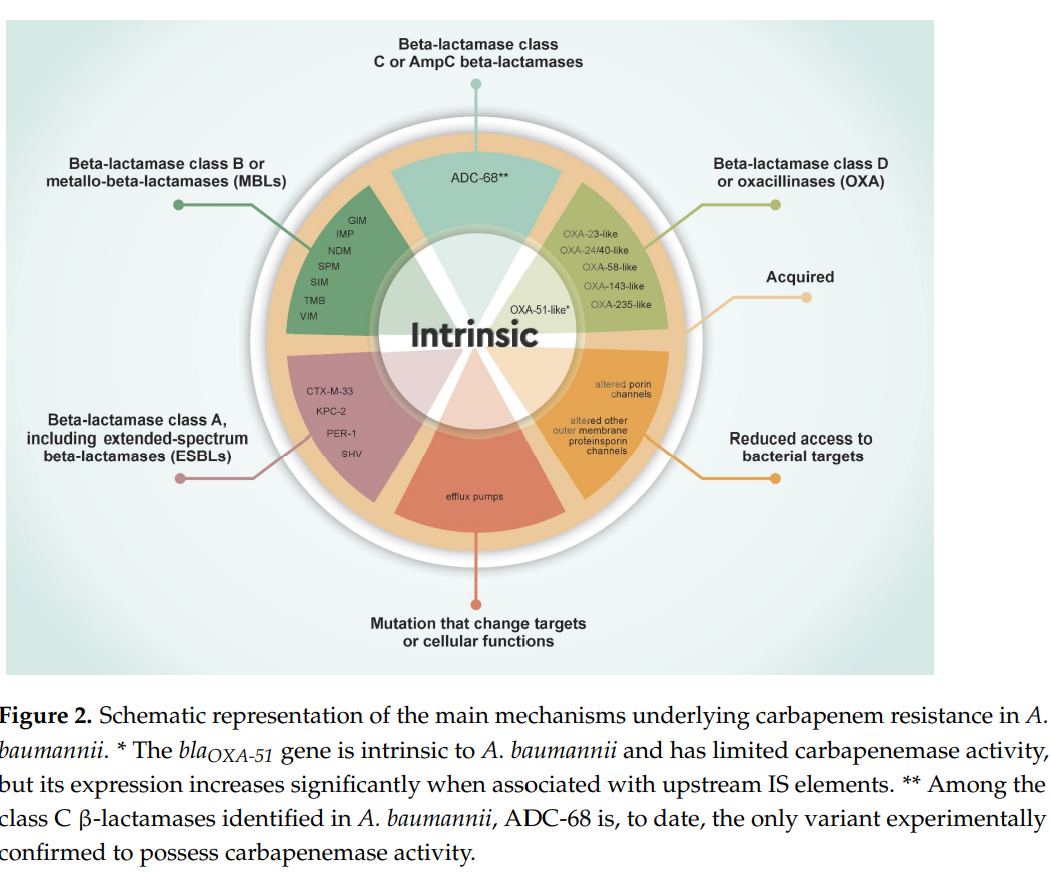
2.1 β-内酰胺酶
β-内酰胺酶可水解包括碳青霉烯类在内的β-内酰胺类抗生素,从而介导耐药性。鲍曼不动杆菌携带多种类别的β-内酰胺酶。本文采用Ambler分子分类系统,包括A类(含超广谱β-内酰胺酶——ESBLs)、B类(金属β-内酰胺酶——MBLs)、C类(AmpC型β-内酰胺酶)及D类(OXA型)。表1和表2列出了鲍曼不动杆菌中已鉴定的主要碳青霉烯类耐药基因。
2.1.1 A类β-内酰胺酶(含超广谱β-内酰胺酶ESBLs)
尽管在鲍曼不动杆菌中较为罕见,但PER、CTX-M和KPC等A类β-内酰胺酶已有零星报道,进一步限制了治疗选择。PER-1是鲍曼不动杆菌中最早发现的ESBLs之一,尤其常见于土耳其和欧洲分离株,并与多重耐药菌株的耐药性增强相关。值得注意的是,由于头孢他啶与头孢地尔的分子结构相似性,PER-1还可能通过其高效头孢他啶水解活性导致对头孢地尔的敏感性降低。哥伦比亚首次报道了鲍曼不动杆菌携带KPC(肺炎克雷伯菌碳青霉烯酶),表明质粒和转座子等可移动遗传元件可能介导肺炎克雷伯菌与鲍曼不动杆菌间的种间基因转移。
CTX-M家族变体在鲍曼不动杆菌中的零星检出,提示可能源自肠杆菌目细菌的水平基因转移。此外,SHV家族β-内酰胺酶虽主要存在于肺炎克雷伯菌,但在伊朗和中国的耐碳青霉烯类鲍曼不动杆菌分离株中亦有报道。同样,广泛分布于肠杆菌目中的TEM家族β-内酰胺酶也见于中国分离株。但需进一步研究确认SHV和TEM酶对碳青霉烯类耐药的确切影响,因其存在可能与其他耐药决定簇共选择相关,而非直接水解碳青霉烯类抗生素。
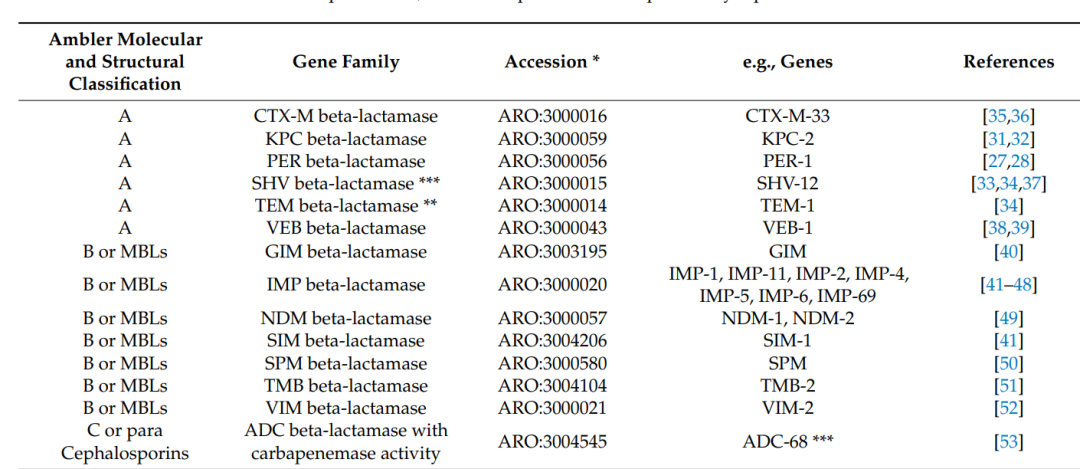
2.1.2 B类β-内酰胺酶(金属β-内酰胺酶MBLs)
NDM-1等MBLs需锌离子维持催化活性,可介导对除单环β-内酰胺类外几乎所有β-内酰胺类药物的耐药性。近期研究发现,NDM家族还能通过升高最低抑菌浓度(MIC)降低对FDA新批准药物头孢地尔的敏感性[29,54]。印度(2010年)和中国(2011年)分别首次报道了产NDM鲍曼不动杆菌。由可移动遗传元件携带的blaNDM基因已实现全球快速传播[56]。环境中的不动杆菌属细菌作为blaNDM的储存库,加速了其扩散。
2.1.3 C类β-内酰胺酶
C类β-内酰胺酶通常不能有效水解碳青霉烯类,因此在耐碳青霉烯类鲍曼不动杆菌(CRAB)中的作用有限。目前ADC-68是鲍曼不动杆菌中唯一经实验证实具有碳青霉烯酶活性的C类β-内酰胺酶。
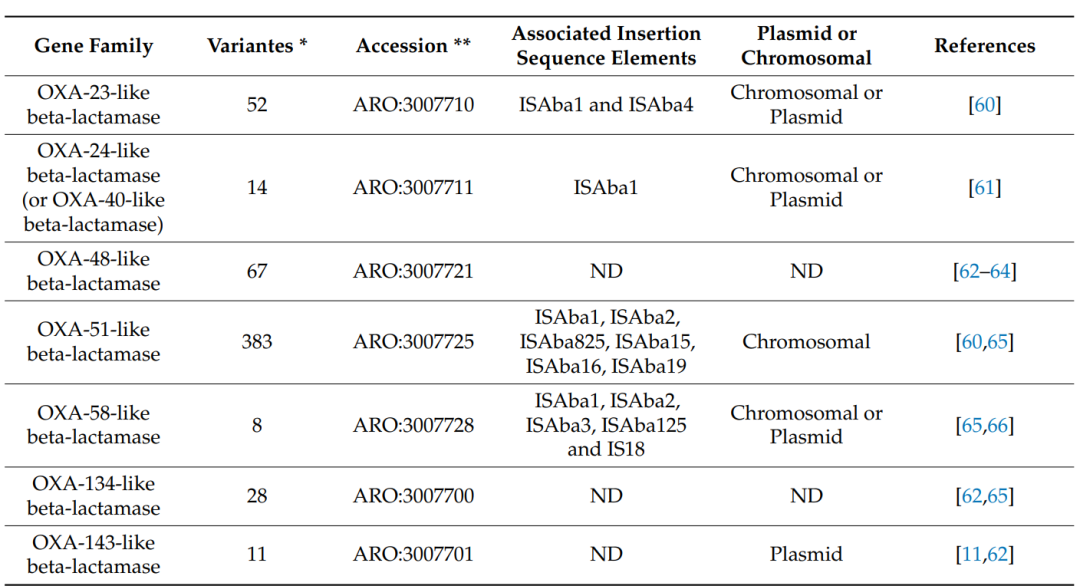
2.1.4 D类β-内酰胺酶(OXA型)
OXA型碳青霉烯酶在鲍曼不动杆菌中最为普遍。1985年苏格兰首次报道的亚胺培南耐药菌株[5]后被鉴定为OXA-23型。该酶已引发全球性传播,并与巴西(2003年)等地的重大暴发相关。随后在苏格兰、西班牙、法国、日本、新加坡、中国、巴西、古巴和科威特等地均发现其多种变体。OXA-24/40样、OXA-58和OXA-143样等OXA型碳青霉烯酶的出现也加剧了区域性耐药问题。
需特别指出,插入序列(IS)元件(如ISAba1和ISAba3)可通过提供强启动子序列显著增强OXA基因表达,从而提升碳青霉烯类耐药水平。典型例证是鲍曼不动杆菌固有携带的blaOXA-51基因:当其上游存在ISAba1时,表达量显著上调并介导高水平耐药。此外,IS元件还通过促进blaOXA变体的水平基因转移,加剧了跨菌株和跨地域传播的防控难度。
生物信息学分析显示,约60%的D类OXA酶信号肽中含有脂化盒序列,可介导细菌外膜锚定。实验证实OXA-23和OXA-24/40在鲍曼不动杆菌中呈膜结合状态,而肠杆菌目常见的OXA-48则为可溶性蛋白。鲍曼不动杆菌释放的外膜囊泡(OMVs)含有活性OXA-23和OXA-24/40,不仅能自我保护,还可使大肠杆菌和铜绿假单胞菌获得对哌拉西林和亚胺培南的抗性。这些发现表明,脂化修饰及OMV介导的运输可能在多微生物感染(尤其是涉及不动杆菌属时)的耐药传播中起关键作用。
2.1.5 其他基因家族
除上述基因家族外,需关注鲍曼不动杆菌中可能存在的未报道碳青霉烯酶编码基因。当前分离株中未检出这些基因,可能反映其真实缺失或研究不足。blaBKC(ARO:3004756)、blaGES(ARO:3000066)、blaIMI(ARO:3000018)、blaSME(ARO:3000055)、blaOXA-114样(ARO:3007698)和blaOXA-198样(ARO:3007703)等已在其他革兰阴性菌(特别是肠杆菌目)中发现的碳青霉烯酶基因,存在理论上的水平转移风险。持续基因组监测对及时发现新型耐药基因至关重要。
2.2 靶位修饰与抗生素渗透障碍
除产β-内酰胺酶外,鲍曼不动杆菌还可通过孔蛋白缺失/外膜修饰限制药物进入,或通过外排泵主动排出抗生素,这些机制的协同作用导致胞内抗菌药物浓度降低及多重耐药性发展。
2.2.1 外膜低渗透性
革兰阴性菌的双层膜结构构成抗生素渗透的选择性屏障。鲍曼不动杆菌因缺乏OmpF/OmpC等通用孔蛋白而天然具有低外膜渗透性。外膜蛋白(OMPs)的缺失或修饰会进一步限制抗生素进入。CarO(碳青霉烯相关外膜蛋白)曾被认为参与碳青霉烯类摄取,但近期晶体结构分析显示其三种亚型主要介导小分子氨基酸转运而非β-内酰胺类。
由于缺乏大孔道孔蛋白,鲍曼不动杆菌(A. baumannii)依赖其他外膜蛋白进行小分子转运。最新研究表明,外膜羧酸盐通道(Occs,旧称OprDs)可能在此过程中发挥关键作用,包括介导抗生素摄取。在鲍曼不动杆菌ATCC 17978和AB307-0294等菌株基因组中,编码有五种Occ同源蛋白。
近期研究通过X射线晶体学成功表达、纯化并解析了其中四个通道(OccAB1至OccAB4)的结构。结构分析显示这些通道具有不同直径的开放孔道,其中OccAB1孔径最大。电生理学和脂质体溶胀实验证实,OccAB1具有最高电导率和小分子摄取效率。值得注意的是,OccAB1对碳青霉烯类抗生素亚胺培南和美罗培南展现出最强的体外通透性,这支持了其在碳青霉烯类抗生素内流中的潜在作用。
2.2.2 抗生素作用靶点的分子变异
青霉素结合蛋白(PBPs)是细菌细胞壁合成过程中的关键酶,也是β-内酰胺类抗生素(包括碳青霉烯类)的主要作用靶点。虽然PBP修饰与鲍曼不动杆菌的碳青霉烯耐药性相关,但其具体机制尚不明确。一项针对西班牙临床分离株的研究鉴定了7个PBP基因和1个单功能转糖基酶(MGT)基因的等位变异。
尽管多数变异为沉默突变,但在流行性耐碳青霉烯克隆中发现插入序列破坏了PBP6b基因。这表明PBP编码基因的遗传重排可能参与耐药机制,但尚未发现特定PBP突变与β-内酰胺敏感性间的直接关联[71]。另一项针对血流感染分离株的研究发现,耐碳青霉烯菌株可产生额外β-内酰胺酶(等电点6.3和7.0),这些酶能增强对亚胺培南和美罗培南的水解作用。这些菌株还表现出22.5 kDa外膜蛋白(OMP)缺失导致的抗生素通透性降低,以及73.2 kDa PBP2条带缺失引发的碳青霉烯结合能力受损。
这些发现揭示了β-内酰胺酶产生、孔蛋白缺失与PBP修饰在碳青霉烯耐药中的协同作用[72]。另有研究证实PBP7/8是维持鲍曼不动杆菌生存和毒力的关键因子。该蛋白缺失会导致膜通透性增加,使细菌更易受补体攻击、溶菌酶活性和多种抗菌剂影响。此外,PBP7/8缺失引起脂质A减少、细胞聚集增强及球状形态转变。在小鼠肺炎模型中,其缺失使细菌致死率降低11倍,提示PBP7/8是治疗耐碳青霉烯鲍曼不动杆菌(CRAB)的潜在靶点。
系统综述显示,31.7%对新型CRAB联合用药舒巴坦-杜洛巴坦耐药的分离株存在PBP3变异,这些变异多位于活性丝氨酸位点(S336)附近。这进一步证实特定PBP修饰会削弱β-内酰胺类药物的疗效,甚至影响新型联合用药方案。
2.2.3 外排泵系统
鲍曼不动杆菌的外排泵通常由外膜通道、周质适配蛋白和内膜转运体组成三联复合物,这些复合物能主动排出细胞内的抗生素和毒性化合物。该转运系统可与孔蛋白缺失、β-内酰胺酶产生等其他耐药机制协同作用,进一步限制治疗选择。目前发现四个主要外排泵家族与鲍曼不动杆菌的耐药性相关:主要易化子超家族(MFS)、耐药结节化分化家族(RND)、小多重耐药家族(SMR)以及多药和毒性化合物外排家族(MATE)。其中RND系统具有最广的底物谱,AdeABC、AdeFGH和AdeIJK系统均与多重耐药相关。
对多重耐药临床分离株的研究表明,其碳青霉烯耐药性源于β-内酰胺酶产生和RND型外排泵(尤其是AdeABC)的过表达。在14株遗传差异菌株中,13株检出adeB基因(AdeABC系统),其中10株存在过表达;仅7株检测到AdeFGH的中度表达,未发现AdeIJK过表达。突变分析显示所有AdeABC过表达菌株均存在AdeRS双组分调控系统的功能突变,两个突变热点提示趋同进化及可能的水平基因转移。这些结果支持AdeABC及其调控突变在临床菌株外排泵介导的耐药中的作用,但其在碳青霉烯耐药中的具体机制仍需深入研究。
另一项研究显示亚胺培南可能作为强诱导剂引发多重耐药:敏感菌经亚胺培南筛选获得的突变株表现出OXA-51样碳青霉烯酶、外排泵和AmpC β-内酰胺酶的表达改变。使用外排泵抑制剂(CCCP和NMP)可部分恢复对亚胺培南和阿米卡星的敏感性,证实主动外排参与该耐药表型。
3. CRAB治疗新策略
3.1 新型抗生素
头孢地尔(Cefiderocol)是2019年获美国食品药品监督管理局(FDA)和2020年获欧洲药品管理局(EMA)批准的CRAB替代疗法。美国感染病学会(IDSA)和欧洲临床微生物与感染病学会(ESCMID)推荐将其与其他抗生素联用以发挥协同效应。该头孢菌素类抗生素具有铁载体活性,能利用细菌铁摄取机制穿透细胞膜,随后通过结合PBPs抑制细胞壁肽聚糖合成。荟萃分析显示,与常规黏菌素方案相比,基于头孢地尔的治疗方案可显著降低CRAB感染患者的死亡风险,且治愈率更高、肾毒性更低[85]。除头孢地尔外,目前尚有多种具有CRAB治疗潜力的分子正在研发中。
然而,与头孢地尔不同,这些新型药物大多仍处于研发早期阶段,尚未获得临床批准。需进一步研究和临床试验以验证其疗效与安全性。下文将重点介绍部分具有前景的候选药物。
其中,由束缚型大环肽(MCPs)衍生的临床候选药物zosurabalpine(RG6006)表现突出。该化合物在体外实验和鼠类感染模型中均显示出对耐碳青霉烯类鲍曼不动杆菌(CRAB)分离株的抗菌活性。其作用机制是通过抑制LptB2FGC复合物(负责将脂多糖(LPS)转运至外膜)导致LPS在菌体内蓄积,从而发挥杀菌作用。I期临床试验证实该药物在健康受试者中具有良好安全性、耐受性及药代动力学特征。
另一新型抗生素BV100是螺哌啶利福霉素衍生物利福布汀的肠外制剂。与传统利福霉素不同,利福布汀可通过FhuE铁载体受体主动穿越鲍曼不动杆菌外膜,使细胞内药物浓度达到抑制RNA聚合酶的水平。静脉制剂BV100旨在解决口服制剂生物利用度低导致的亚治疗浓度问题,其对CRAB展现出显著体内活性。I期试验证实其安全性后,II期研究(NCT05685615)显示:BV100联合多粘菌素治疗组的14天和28天死亡率(12.5%与25%)显著低于最佳可用疗法(BAT)组(40%与60%),微生物学应答率(75% vs 50%)和临床治愈率(75% vs 30%)亦更优。该结果为利福布汀联合疗法预防耐药性发生提供了依据。
研究者还通过结构修饰开发新型抗生素。氟环素类合成四环素TP-6076对CRAB的活性优于或相当于现有四环素类、氨苄西林-舒巴坦及黏菌素。新一代多黏菌素衍生物SPR206、QPX9003、FADDI-002和FADDI-003在实验研究中显示出更优的疗效与安全性[95]。在抗生素佐剂中,经疏水脂肪酰尾修饰的阳离子肽SPR741可增强其他抗生素的膜渗透性,但单用时对革兰阴性菌无效。此外,类芽孢杆菌M2产生的套索肽抗生素lariocidin在小鼠模型中显示抗CRAB活性,但尚需临床验证。
3.2 联合疗法
鲍曼不动杆菌的多重耐药特性使其感染治疗尤为困难。联合用药可降低耐药风险,部分组合在体外显示协同效应,但临床证据仍有限。目前推荐方案为含舒巴坦的高剂量氨苄西林-舒巴坦联合多黏菌素B或替加环素,但疗效尚未形成共识。
3.2.1 舒巴坦-度洛巴坦
新型固定剂量复方制剂舒巴坦-度洛巴坦(Xacduro)近期获美国批准用于治疗鲍曼不动杆菌复合体引起的医院获得性肺炎和呼吸机相关肺炎。其中度洛巴坦作为DBO类β-内酰胺酶抑制剂可保护舒巴坦免受A/C/D类酶水解。体外研究显示该组合对CRAB的活性与黏菌素相当且优于阿米卡星、米诺环素和单用舒巴坦。临床研究显示其对产OXA型碳青霉烯酶菌株的有效率达62%,优于黏菌素组(40%),且肾毒性更低[109]。临床用药评价公众号:目前IDSA推荐联用亚胺培南-西司他丁或美罗培南治疗CRAB。
3.2.2 头孢洛扎-他唑巴坦
他唑巴坦与头孢洛扎联用可增强黏菌素对CRAB的协同效应,或成为替代方案。
3.2.3 多黏菌素与四环素类/糖肽类的协同作用
四环素类(米诺环素、替加环素、依拉环素)与碳青霉烯类或多黏菌素联用可能产生协同效应。
3.2.3 联合用药方案的体外与体内研究证据
体外实验表明,与单药或双药方案相比,高剂量米诺环素-多黏菌素B-舒巴坦三联方案对耐碳青霉烯类鲍曼不动杆菌(CRAB)展现出最佳抗菌效果。在小鼠肺炎模型中,米诺环素分别与多黏菌素B、利福平或阿米卡星联用均较单药治疗获得更佳疗效。与米诺环素类似,体外研究显示高剂量多黏菌素B联合米诺环素衍生物替加环素时,对鲍曼不动杆菌的清除效果显著优于多黏菌素B单药治疗。
另有研究报道,大剂量舒巴坦与替加环素联用可有效治疗耐药鲍曼不动杆菌感染。然而目前对于替加环素单药或联合方案治疗CRAB感染的临床疗效尚未达成共识。鉴于鲍曼不动杆菌对替加环素尚缺乏明确的药敏折点,美国感染病学会(IDSA)推荐在联合治疗中优先选用米诺环素而非替加环素。
依拉环素作为新型氟环素类药物,于2018年获美国食品药品监督管理局(FDA)批准用于严重腹腔感染治疗。与其他四环素类相似,该药通过细菌孔蛋白(特别是鲍曼不动杆菌OmpA孔蛋白)进入菌体后,与核糖体30S亚基结合从而阻断信使RNA合成。近期研究显示,头孢地尔与依拉环素联用方案对CRAB感染具有潜在治疗价值。
多黏菌素与糖肽类联用可产生协同效应,其机制可能在于多黏菌素使细菌外膜通透性增加,促进大分子糖肽类药物的细胞内渗透。体外实验证实,多黏菌素-万古霉素以及多黏菌素-多尼培南-万古霉素三联方案均可完全杀灭耐多黏菌素鲍曼不动杆菌。在蜡螟感染模型中,这些联合方案较单药治疗显著提高幼虫存活率。类似结果也见于多黏菌素-替考拉宁及多黏菌素-新型脂糖肽类特拉万星联用方案。此外,4例耐多药鲍曼不动杆菌全身感染患者的病例报告显示,多黏菌素-万古霉素联合治疗取得良好疗效且未出现感染复发或严重不良反应。
3.2.4 联合治疗在耐药菌株中的疗效与挑战
针对CRAB的联合治疗方案虽旨在克服耐药机制并提高疗效,但仍面临疗效不一致性和潜在毒性的挑战。现有证据多源于回顾性观察性研究,存在较高偏倚风险。目前联合方案的评估主要基于低质量观察性研究,且不同抗生素组合的差异性使得疗效判定困难。此外,部分药物(如替加环素、依拉环素)尚未建立美国临床和实验室标准协会(CLSI)或欧洲抗菌药物敏感性试验委员会(EUCAST)的折点标准。对于氨苄西林-舒巴坦等药物,还需重新评估高剂量给药时的最低抑菌浓度(MIC)折点调整。
3.3 新型碳青霉烯酶抑制剂的研发进展
碳青霉烯酶能水解碳青霉烯类抗生素,严重削弱其对耐多药感染的疗效。因此,碳青霉烯酶抑制剂的开发成为恢复碳青霉烯活性的重要策略。基于环状(xeruborbactam/QPX7728)与双环(taniborbactam/VNRX-5133)硼酸结构的广谱抑制剂可同时靶向丝氨酸β-内酰胺酶和金属β-内酰胺酶。虽然现有研究主要针对肠杆菌目,但最新证据表明taniborbactam对产OXA-23和OXA-24/40酶的鲍曼不动杆菌亦具抑制潜力。该药可与头孢吡肟联用,而xeruborbactam则可与头孢地尔组合以增强协同效应。
二氮杂双环辛烷类抑制剂(DBOs)如瑞莱巴坦、度洛巴坦最初靶向A/C类β-内酰胺酶,新近研究则探索其对鲍曼不动杆菌D类碳青霉烯酶的抑制作用。其中度洛巴坦-舒巴坦与亚胺培南-funobactam联用方案对OXA-23、OXA-24/40及OXA-58型碳青霉烯酶(鲍曼不动杆菌主要耐药酶型)展现显著活性。这些组合已进入临床研发后期阶段,有望成为耐碳青霉烯感染的治疗选择。舒巴坦-度洛巴坦已完成临床开发并获得美国上市许可,而亚胺培南-西司他丁-funobactam虽完成III期临床试验,目前仅在中国提交上市申请,其针对复杂性尿路感染的全球III期试验(NCT05204368)尚未启动受试者招募。
另一颇具前景的候选药物WCK-4234作为新型DBO类β-内酰胺酶抑制剂,对A/D类碳青霉烯酶及C类酶均具显著抑制活性,可增强碳青霉烯类对鲍曼不动杆菌的抗菌作用。LN-1-255作为青霉烷砜类衍生物,能抑制D类碳青霉烯水解酶,同时对A/C类β-内酰胺酶有效。该药通过细菌铁摄取途径进入细胞,体外实验正评估其恢复亚胺培南、美罗培南等β-内酰胺类药物疗效的潜力。
3.4 替代性与创新性治疗策略
CRAB流行率的持续上升促使研究者探索传统抗生素以外的治疗途径。创新策略包括噬菌体疗法、抗菌肽、CRISPR基因编辑技术、质粒靶向疗法及纳米技术等,这些通过新机制克服耐药性的方法展现出良好前景。
3.4.1 新型外排泵抑制剂的研发
如前述讨论,外排泵在多重耐药性中起关键作用,目前虽无临床获批的外排泵抑制剂,但针对天然化合物(如生物碱、黄酮类)及其化学修饰物的研发工作正在推进。Verma等报道,柚皮素二氢查耳酮包被的银纳米颗粒(NDC-AgNPs)通过抑制AdeABC外排泵系统中AdeB组分介导的药物外排,对耐碳青霉烯类鲍曼不动杆菌(CRAB)具有显著抗菌效果。类似地,3-O-取代槲皮素不仅能有效抑制外排泵功能,还可作为碳青霉烯耐药肠杆菌科细菌金属β-内酰胺酶的抑制剂。天然化合物还可增强已知抗菌药物的疗效,如白藜芦醇与氯己定联用对CRAB表现出强协同作用,但其作用机制是通过抑制adeB基因表达而非直接阻断泵活性。
创新化合物与传统药物的联用策略已取得突破性进展。例如,通过肉桂油与甲氧苄啶联合调控外排泵相关基因表达,可完全消除临床分离株的碳青霉烯耐药性。对已知分子进行化学修饰同样具有应用前景:大肠杆菌AcrAB-TolC外排泵抑制剂4-二氢咪唑苯胺和4,6-二氨基喹啉经结构改造后,可特异性作用于鲍曼不动杆菌AdeIJK外排泵。近期发现的吡啶哌嗪类抑制剂经优化后,能选择性抑制AdeJ介导的外排活性。
小分子增效剂研究取得重要进展。由于AbaF泵介导的主动外排机制,鲍曼不动杆菌对磷霉素具有固有耐药性。双(4-甲基苄基)二硫化物(IITR08367)可通过抑制AbaF泵显著增强磷霉素抗菌活性,该发现为CRAB治疗提供了新的联合用药方案。
3.4.2 噬菌体疗法
噬菌体疗法作为治疗CRAB等多重耐药菌感染的新型策略,在常规抗生素治疗失败病例中展现出潜力。但现有研究多局限于个案报告、体外实验或动物模型,主要挑战在于缺乏标准化方案——不同研究使用的噬菌体鸡尾酒配方、给药剂量和疗程存在显著差异。临床用药评价公众号:需注意发表偏倚可能高估临床疗效,且对细菌噬菌体耐药机制的认知不足可能重蹈抗生素滥用的覆辙。
3.4.3 抗菌肽(AMPs)
抗菌肽作为先天免疫防御分子,通过多种机制对抗CRAB:LL-37破坏细菌膜完整性;Mastoparan具有膜穿透功能;ZY4通过形成膜孔增加通透性;合成肽P92则特异性靶向外膜蛋白A(AbOmpA)。尽管天然AMPs临床转化受限,但通过理性设计改造的合成肽在抗菌活性、结构稳定性和细胞选择性方面取得显著提升。新建立的AbAMP数据库为候选分子筛选提供了重要工具。
3.4.4 基因编辑技术
CRISPR-Cas系统因其精准靶向性成为逆转CRAB耐药性的优选工具。研究证实,利用AB43菌株内源性I-Fb型CRISPR-Cas系统下调群体感应合成酶abaI,可显著降低外排泵表达、削弱生物膜形成并增加活性氧累积,最终恢复抗生素敏感性。另研究开发的CRISPR干扰(CRISPRi)系统能有效实现靶基因转录沉默。
通过实验验证,新型细胞分裂蛋白AdvA的功能得到确认,同时发现一个未被表征的AraC家族转录调控因子(ACX60_RS03245)对细菌生长具有关键作用。近期研究报道了sgRNA-I/L@ZS纳米系统(一种可递送亚胺培南和CRISPR/Cas9的”纳米炸弹”)的开发,该体系对耐碳青霉烯类鲍曼不动杆菌(CRAB)展现出高效杀菌活性。
然而,CRISPR-Cas系统作为治疗工具应用面临的主要挑战在于其组分如何高效递送至细菌细胞内。目前存在两种主要策略:不依赖递送载体的CRISPR/Cas系统(如利用内源性系统)和基于递送平台的CRISPR/Cas系统(通常使用噬菌体或纳米颗粒)。噬菌体递送系统虽具前景,但存在宿主范围狭窄、免疫原性及监管标准缺失等局限性。通过改造噬菌体以扩展其宿主特异性是解决这些问题的潜在策略。为克服递送限制,纳米技术已被整合至CRISPR系统中。近期研究采用脂质体和聚合物封装CRISPR-Cas组分,既可防止降解又能提高细菌摄取效率,从而显著提升基因敲除效率。
3.4.5 纳米颗粒策略
纳米颗粒(NPs)是尺寸为1-100纳米的材料,其独特的物理化学性质可增强与细菌细胞的相互作用。在抗菌耐药性(AMR)领域,纳米颗粒通过膜结构破坏、活性氧(ROS)生成及靶向给药等方式规避传统耐药机制的能力备受关注。目前研究最深入的纳米颗粒既可作为固有疗法(如二氧化钛(TiO2)NPs、氧化锌(ZnO)NPs[26]、铜(Cu)NPs、镍(Ni)NPs、硒(Se)NPs和银(Ag)NPs),也可作为抗菌剂的纳米载体(”纳米抗生素”,如脂质体)[176,177]。最新研究表明,氧化铜纳米颗粒对包括鲍曼不动杆菌在内的多重耐药病原体具有生长抑制作用,最低抑菌浓度(MIC)范围为62.5-125 µg/mL。这些纳米颗粒还表现出抗生物膜潜力和抗氧化活性,与传统抗生素联用时可增强疗效。
尽管银纳米颗粒(纳米银;NAg)被公认为最有效的替代抗菌剂之一,但最新研究发现鲍曼不动杆菌可能对其产生耐药性。长期暴露于NAg可诱导该菌产生稳定的生理适应,包括生物膜形成改变和氧化应激反应变化。这些适应性与表面附着相关基因及荚膜多糖生物合成基因的突变有关。此外,暴露于银离子(Ag+)后观察到独特的耐受表型,表现为呼吸活性增强和形态学改变。这些结果凸显了鲍曼不动杆菌对纳米银和离子银的双重适应能力,提示临床中需谨慎控制NAg的使用以维持其疗效并降低耐药风险。
4. 计算生物学方法在抗击耐碳青霉烯类鲍曼不动杆菌中的应用
4.1 基于人工智能的抗菌药物筛选与设计
在所有应用中,人工智能(AI)最具颠覆性潜力。AI本身虽非最终产品,但可作为支撑平台贯穿诊断创新、治疗设计和疫情预防全过程。早在高性能计算和AI成为现实之前,科学家就已提出可利用蛋白质三维结构进行药物设计。AlphaFold等AI工具用于蛋白质结构测定[181],彻底改变了结构生物学领域,能在数分钟内实现高可靠性的蛋白质结构精准预测。基于确定的结构,可进一步使用其他AI工具分析酶类(如β-内酰胺酶)或转运蛋白(如外排泵)表面特征,进而设计具有抑制潜力的分子。
例如,在一项计算机筛选中,5种合成化合物针对鲍曼不动杆菌三种外排泵(AdeB、AdeG和AdeJ)进行测试。新型咪唑[4,5-g]喹啉-4,9-二酮衍生物KSA5因其抑制抗生素外排的能力脱颖而出。分子对接模拟显示,KSA5可通过与配体结合位点残基的稳定相互作用结合这些外排泵。另一项计算机筛选研究测试了7500种分子对鲍曼不动杆菌体外生长的抑制作用,这些数据用于训练能预测新型化学结构且对该病原体具有抗菌活性的神经网络模型。该计算策略发现了对鲍曼不动杆菌具有选择活性的化合物abaucin,其通过与LolE蛋白相互作用抑制脂蛋白转运。动物模型证实了其治疗价值,abaucin可有效治疗小鼠鲍曼不动杆菌皮肤感染。
通过对11,648种天然化合物的虚拟筛选,研究人员鉴定出靶向鲍曼不动杆菌OmpW的潜在分子。其中去甲氧基姜黄素因其良好的药代动力学特性和强结合稳定性成为最佳候选,实验验证显示其对多种鲍曼不动杆菌菌株(包括OmpW缺陷突变体)具有抗菌活性,与粘菌素联用表现出协同效应。
药物设计也被应用于β-内酰胺酶抑制剂研发。针对NDM-1 β-内酰胺酶的研究基于萘、噻唑和砜类分子设计了20种能与酶活性位点锌离子相互作用的化合物。通过分子对接鉴定出3种先导化合物,其中T016在分子动力学模拟中表现出高稳定性和良好药代特性,是体外测试的潜在候选物。关于AmpC抑制的研究采用深度学习预测非共价抑制剂,使用支持向量机(SVM)、随机森林和神经网络等分类模型,这些模型在识别新抑制剂时准确率高达83%,可分析分子的理化特征及结合模式。
4.2 人工智能在基因组解读与表型预测中的应用
DNA测序技术的演进与成本下降使得全球范围内数千株具有不同耐药表型的细菌基因组测序成为可能。这些海量基因组数据使得全基因组关联分析(GWAS)等原本仅限于人类基因组研究的方法得以应用于细菌研究。GWAS正在扩展鲍曼不动杆菌耐药基因型的认知范围,除经典耐药基因外,还发现糖基转移酶和保守假设蛋白等既往认为无关的基因参与耐药。基因组不同位点的单核苷酸多态性(SNPs)可作为特定抗生素耐药的指标,用于训练基于基因组数据的耐药预测网络。结合血液样本(临床宏基因组)快速DNA测序方法,经训练可识别耐药相关基因组模式的AI工具,有望彻底改变脓毒症等危重疾病的床旁治疗模式。
4.3多组学分析与人工智能整合
此外,整合基因组学、转录组学、蛋白质组学、脂质组学和代谢组学数据的多组学研究为深入探究细菌对抗生素的响应机制提供了强大工具。这些数据集的全面整合不仅深化了我们对鲍曼不动杆菌(A. baumannii)适应性可塑性的理解,更有助于发现新的药物靶点并开发更有效的联合治疗方案。然而,大规模多组学数据的整合与解析仍面临重大挑战。
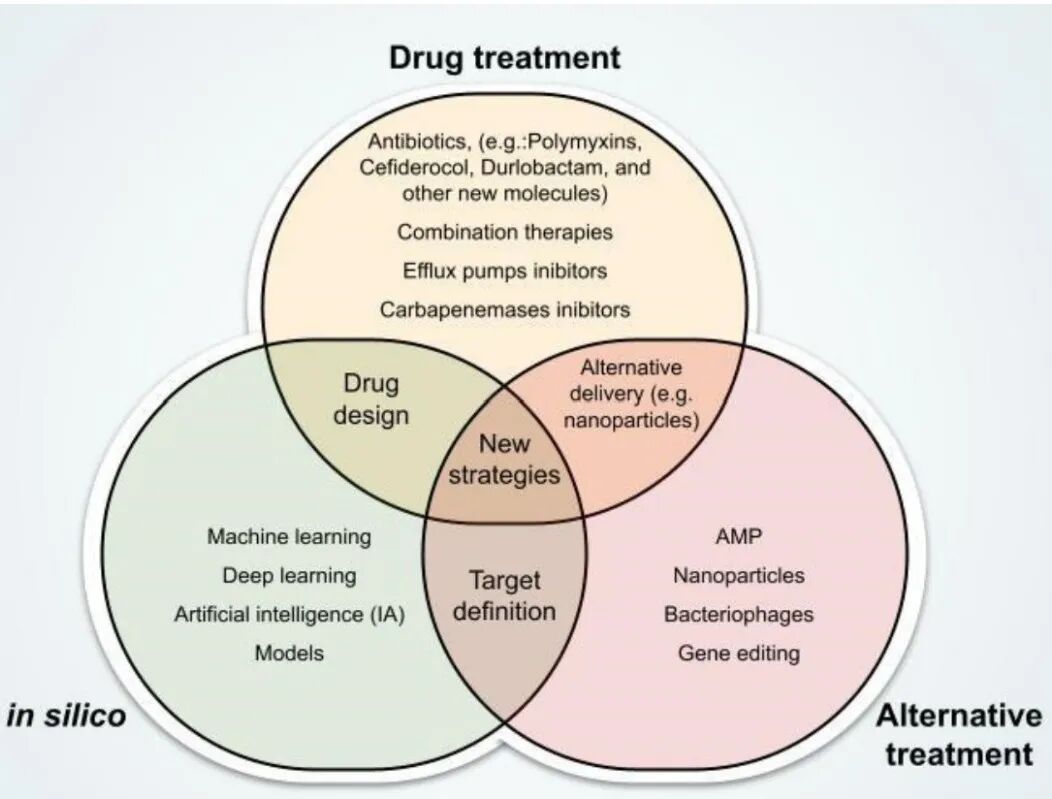
人工智能技术(包括机器学习算法、神经网络和深度学习方法)的应用对于推动该领域发展、充分释放多组学分析潜力具有不可或缺的作用。多组学数据可用于构建不同生理状态下的基因组尺度代谢模型,基于这些模型训练的人工智能工具可为核心代谢通路中的潜在靶点提供预测建议,这些靶点经失活后可产生杀菌或抑菌效应。图3通过维恩图展示了耐碳青霉烯类鲍曼不动杆菌(CRAB)治疗的创新策略及其交叉研究领域。
【结论】
CRAB的日益流行对全球公共卫生构成严重威胁,尤其在治疗选择极其有限的重症监护环境中。本综述系统阐述了耐药性产生的复杂分子机制,包括β-内酰胺酶的产生、外膜通透性改变、外排泵过表达以及抗生素靶位修饰,同时揭示了由可移动遗传元件介导的耐药基因全球传播态势。
在此背景下,基于全基因组测序的分子监测至关重要。大规模基因组分析揭示了高度耐药流行株(特别是国际克隆株IC1和IC2)的主导地位,这些菌株现被重新归类为流行超级谱系(ESL)成员,其构成了全球临床CRAB分离株的主体。这些克隆株通过同源重组和转座元件的作用,持续获得耐药基因和毒力因子。值得注意的是,基于基因组的方法可实现流行菌株的系统发育定位和耐药机制的时间追踪,这些工具对于疫情预警、经验性治疗指导和公共卫生干预具有重要价值。
尽管面临挑战,抗生素研发、β-内酰胺酶抑制剂和协同药物组合等领域的最新进展为治疗带来了新希望。噬菌体疗法、抗菌肽、纳米颗粒递药系统和CRISPR基因编辑等替代方案也展现出显著潜力,但尚需进一步临床验证。人工智能与多组学技术的融合为理解CRAB病理生理机制开辟了新途径,有助于发现新型治疗靶点和耐药生物标志物。未来,基于基因组和流行病学数据的精准治疗开发与强化监测系统的建立,对于控制CRAB传播、保障最后防线抗菌药物的疗效将发挥关键作用。
文献来源:de Souza J, D’Espindula HRS, Ribeiro IF, et al. Carbapenem Resistance in Acinetobacter baumannii: Mechanisms, Therapeutics, and Innovations. Microorganisms. 2025 Jun 27; 13(7): 1501.
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫