鲍曼不动杆菌对替加环素的耐药机制
【据《Frontiers in Cellular and Infection Microbiology》2023年5月报道】题:鲍曼不动杆菌对替加环素的耐药机制(中国浙江大学爱丁堡大学联合学院 作者Chunli Sun等)
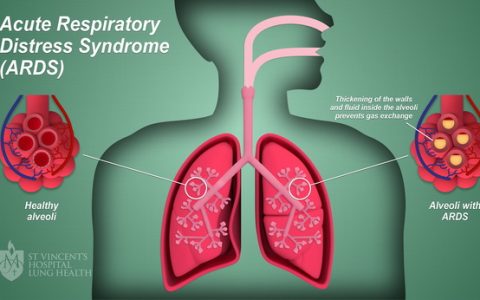
鲍曼不动杆菌是一种非发酵性革兰氏阴性细菌,与呼吸机相关肺炎、伤口和尿路感染、血流感染、心内膜炎和脑膜炎等的发生和发展密切相关,发病率和死亡率非常高,特别是在重症监护室(ICU)病人中。
由于抗生素的不合理使用、住院病人之间的交叉感染和耐药性遗传因子的传播等多种因素,越来越多的鲍曼不动杆菌菌株演变成多药耐药(MDR)、广泛耐药(XDR)甚至是泛药耐药(PDR)菌株,这限制了抗生素的临床治疗选择。近年来,耐碳青霉烯类药物的鲍曼不动杆菌(CRAB)也已被广泛报道。
替加环素是第三代四环素衍生物,对核糖体的亲和力增加,从而克服了TetM介导的四环素耐药性,表现出卓越的抗菌活性。此外,替加环素独特的化学结构增加了药物的脂溶性,还通过产生立体阻碍,防止其被大多数膜结合的外排蛋白泵出细胞。更重要的是,替加环素还克服了其他抗生素耐药机制,如药物靶点修饰、酶降解和DNA聚合酶突变,使其成为一种有前景的抗菌药物,可用于广泛的应用。
尽管如此,耐替加环素的鲍曼不动杆菌感染的临床病例正在增加。因此,急需对替加环素耐药性和鲍曼不动杆菌的耐药机制进行分析,为临床制定治疗策略和控制鲍曼不动杆菌暴发提供理论指导。中国浙江大学爱丁堡大学联合学院Chunli Sun等回顾了鲍曼不动杆菌对替加环素的耐药机制,以期为替加环素的合理临床应用和新的候选抗生素的开发提供参考。
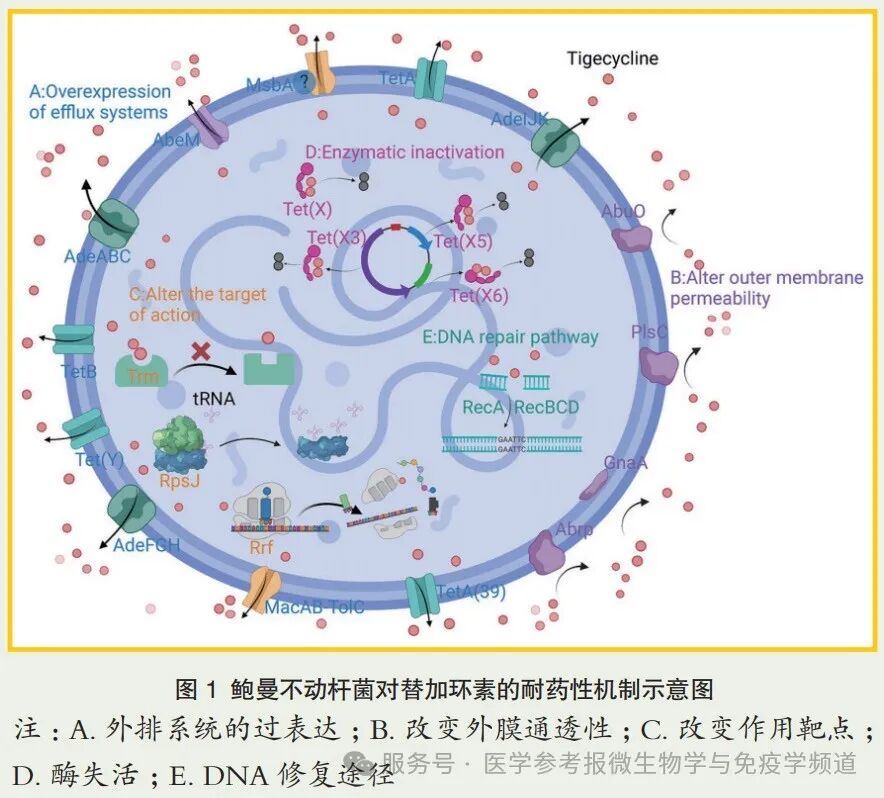
鲍曼不动杆菌对替加环素耐药的主要机制可分为五类(图1):(1)外排泵过度表达;(2)外膜通透性改变;(3)替加环素作用靶点改变;(4)替加环素失活酶产生;以及(5)DNA损伤后介导替加环素耐药的修复途径。
一、外排泵系统
外排泵的过度表达是导致鲍曼不动杆菌耐药的关键机制。外排泵将抗菌药物排出细胞,导致药物浓度降低和耐药性产生。与鲍曼不动杆菌耐药性相关的有5个超家族:耐药调制–细胞分裂(RND)家族、多药和毒性化合物挤出(MATE)家族、ATP结合盒(ABC)转运体、主要促进剂超家族(MFS)和小型多药耐药性(SMR)家族,其中前4个家族已被报道介导了替加环素耐药性。
1. RND外排泵和调节因子
RND外排泵是MDR鲍曼不动杆菌最普遍的外排泵,包含三个主要成员:AdeABC、AdeFGH和AdeIJK。它们都是由结构基因编码的三种结构蛋白组成的三联体。AdeABC是鲍曼不动杆菌中第一个被研究的RND系统,由adeA(主要融合蛋白)、adeB(多药转运体)和adeC(外膜蛋白)组成。研究表明,AdeABC、AdeFGH和AdeIJK的过表达与鲍曼不动杆菌对替加环素敏感性降低有关。
2. MATE家族
MATE转运体可以通过Na+或H+作为偶联离子,将各种有毒有害物质赶出膜外。它是细菌抵御外部环境压力的重要防御机制。属于MATE转运蛋白家族的AbeM是一种H+偶联的多药外排泵。有研究显示替加环素耐药鲍曼不动杆菌中abeM表达增加,但不同研究所得结果并不一致,表明还有其他机制影响鲍曼不动杆菌对替加环素耐药性。
3. ABC转运体
ABC转运体与其他家族转运体不同,它利用ATP结合和水解产生的能量来执行外排功能。MsbA是被分析的第一个ABC转运体。有研究认为msbA突变扩大了泵的特异性,促进了替加环素外排。MacAB-TolC是另一个涉及替加环素耐药性的重要外排泵系统。
4. MFS外排泵
MFS外排泵是一种依赖质子的抗菌药物外排系统,包括被动转运器和次级主动转运系统。TetA与TetB是MFS家族重要成员,二者与替加环素耐药性之间存在关联,但仍需更多的研究来揭示其潜在机制。另有研究发现质粒介导的tet(Y)基因也是鲍曼不动杆菌对四环素抗性的决定因素。
二、外膜通透性
为了防止抗菌剂进入细胞,降低外膜的通透性是另一种常见的抗性机制。研究表明,编码1-酰基-sn-甘油-3-磷酸酰化酶的plsC基因、编码肽酶C13家族的abrp基因、编码参与催化UDP-D-MANPNAC3NACA合成酶的gnaA基因都可通过影响细胞膜通透性介导鲍曼不动杆菌对替加环素的抗性。
三、抗生素的作用靶点
改变抗生素的作用靶点也是细菌产生抗性的机制之一。研究发现,在接触替加环素的情况下,各种病原体都出现了rpsJ突变,此突变引起S10环的结构变化,进而改变了16S RNA的构象,最终导致了替加环素和核糖体的结合亲和力下降。另有研究表明,trm基因可能像ArmA、RmtA和NpmA一样对核糖体靶点进行甲基化,阻碍替加环素与其靶点的结合,并介导替加环素抗性。rrf基因编码核糖体循环因子(RRF)的产生。研究证实rrf基因的突变降低了RRF蛋白的表达,影响了核糖体的回收过程,最终表现出对替加环素的耐受性表型。。
四、抗生素灭活酶
通过降解和修饰抗生素使其失去活性是细菌的一个重要的抗性机制。有研究报道Tet(X)及其变体通过质粒介导鲍曼不动杆菌对多种四环素耐药。替加环素是Tet(X)的底物之一,需要在FAD、NADPH、O2和Mg2+存在的情况下激活。Tet(X)通过改变替加环素的物理特性,削弱它与镁的结合,降低它与核糖体的亲和力,使其失活,从而使细菌产生抗性。迄今为止,在Tet(X)家族中已有8个与替加环素高度抗性有关的基因,即Tet(X)、Tet(X1)、Tet(X2)、Tet(X3)、Tet(X4)、Tet(X5)、Tet(X6)、Tet(X7),其中Tet(X1)是一个没有酶活性的截短变体。
五、DNA修复途径
已证实抗生素诱导下的DNA损伤可以介导鲍曼不动杆菌的死亡,而RecA和RecBCD是DNA修复的重要途径。其中RecA是参与基因同源重组和重组修复的主要酶,而RecBCD参与DNA双链修复。
六、其他潜在机制
除了上述相关机制外,研究发现与没有突变的菌株相比,parC和gyrA基因都有突变的鲍曼不动杆菌对替加环素的抗性水平更高。Hammerstrom等人使用生物信息学方法推断rnpA、rpoD、rppH、wzc和pcaF是候选的替加环素抗性基因。
七、结论
耐替加环素的鲍曼不动杆菌是一个全球性的公共卫生恐怖分子。为了适应外部环境的压力,细菌已经进化出多种抗性策略。许多研究表明,RND外排泵的过度表达是导致鲍曼不动杆菌耐替加环素的主要原因。外排泵的表达也受到各种调节因子的调节,并相互影响。因此,外排泵的作用机制是多样而复杂的,需要进行全面研究。
脂质双分子层是鲍曼不动杆菌的重要屏障,通道蛋白的缺失或基因突变降低了外膜的通透性,会导致替加环素进入细胞的困难和细菌的最低抑制浓度增加。此外,深入了解通道蛋白的功能和特性,以及确定可能影响外膜通透性和通道蛋白封闭性的调节因素,将有利于有针对性地开发新型药物,改善目前的临床药物治疗。
rpsJ和rrf可以通过突变来降低结合核糖体蛋白的能力,而trm可能通过酶的修饰来改变药物的作用部位,所有这些最终都会导致对替加环素的抗性。重要的是,由于rpsJ突变导致的替加环素耐药的高频位点是第57位氨基酸,这不仅发生在鲍曼不动杆菌中,也发生在多种病原体中。这为将来通过筛查rpsJ突变来识别替加环素耐药性提供了一种独特的方法。
Tet(X)可以使替加环素失活并产生抗性。令人担忧的是,新的Tet(X)变体不断被发现,它们可以通过水平基因转移在广泛的病原体中迅速传播,似乎正处于全球流行的边缘。因此,需要深入研究Tet(X)变体的起源、结构和进化机制,以及设计针对这种酶的抑制剂和干扰剂,以克服Tet(X)和变体介导的高水平的替加环素抗性。
RecA和RecBCD是参与损伤后DNA修复的重要因素。研究证明,RecA可以保护鲍曼不动杆菌免受紫外线、热冲击、干燥和包括替加环素在内的几类抗生素的影响。recA和recBCD的缺失有助于替加环素介导的对鲍曼不动杆菌的致死性。因此,未来的注意力可以集中在对recA、recBCD的抑制上,以达到治疗鲍曼不动杆菌感染的目的。
田小芳 编译]
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫