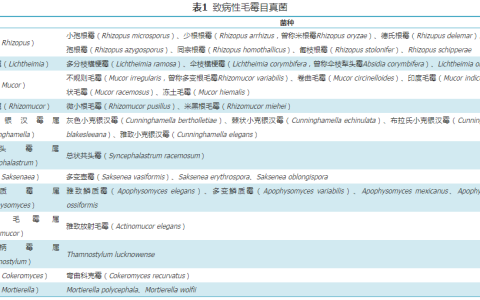
2025 年,中南大学湘雅医院、湖南师范大学、南方医科大学珠江医院等多家单位联合在 Signal Transduction and Targeted Therapy发表综述《Tissue macrophages: origin, heterogeneity, biological functions, diseases and therapeutic targets》。文章系统梳理了组织巨噬细胞的胚胎起源(原始造血祖细胞、卵黄囊 EMP、成年 HSC)与组织特异性驻留(TRMs)的最新研究进展,指出传统 M1/M2 二元分型已难以覆盖其高度可塑性与异质性。作者聚焦的核心问题是:如何基于单细胞测序、谱系示踪等新技术,重新定义巨噬细胞的发育谱系与功能亚群,并阐明其在肿瘤、自身免疫、心血管、神经退行性及代谢疾病中的双重作用,从而为精准靶向巨噬细胞的临床治疗提供路线图。
-
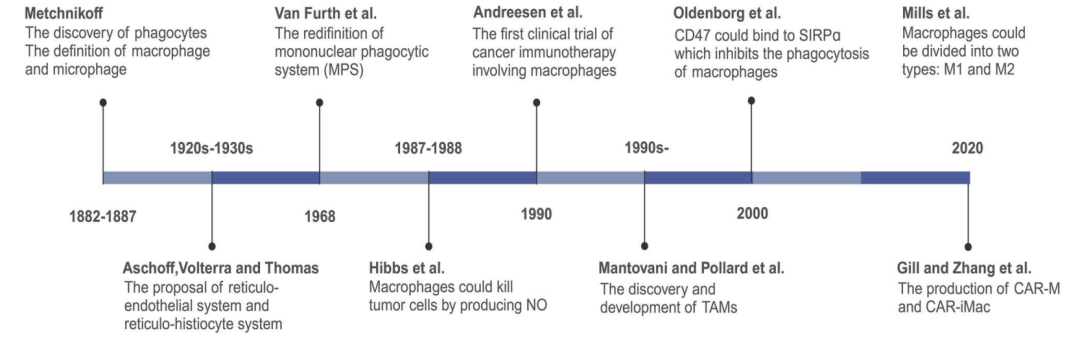
1882 年,Metchnikoff 首次在棘皮动物幼虫中发现能清除异物的“吞噬细胞”,奠定巨噬细胞概念;1887 年将其分为巨噬细胞与微噬细胞(即后来的中性粒)。
-
此后“网状内皮系统”等假说被证伪,1968 年 van Furth 等提出单核吞噬细胞系统(MPS),认为巨噬细胞源自骨髓单核细胞。
-
1990–2010 年间研究揭示胚胎来源的组织驻留巨噬细胞(TRMs)可长期自我更新,与成体 HSC 来源的单核细胞互补。
-
关键里程碑:
– 1987–1988 年发现 NO 介导的杀瘤活性;
– 2000 年阐明 CD47–SIRPα “别吃我”信号及 M1/M2 分型;
– 1990 年首次开展 MDM 肿瘤免疫治疗试验;
– 2020 年 CAR-M 与 CAR-iMac 技术问世,FDA 批准首个抗 HER2 CAR-M Ⅰ期临床(NCT04660929),标志巨噬细胞治疗进入基因工程时代。
-
传统观点认为组织巨噬细胞全部来自造血干细胞(HSC),但系列研究证实成年组织巨噬细胞主要起源于胚胎期的卵黄囊或胎肝。
-
小鼠命运图谱显示卵黄囊 EMP 至少分两波:
– E7.5 第一波:原位分化为巨噬细胞 → 迁入脑原基 → 成为小胶质细胞主流来源。
– E8.25 第二波:EMP 先迁至胎肝 → 分化为 EMP-PreMacs → 经血循环定植各组织(脑除外)→ 发育为表皮朗格汉斯细胞、肝脏 Kupffer 细胞等异质性 TRMs。 -
EMP 胎儿期后消失,TRMs(及部分肥大细胞)可持续至成年并局部自我更新。
-
TRMs 能否源于 HSC 仍有争议:
– 多数命运图谱表明主动脉-性腺-中肾区胎儿 HSC 不生成巨噬细胞。
– 实验性脑炎/中风模型中,外周单核细胞来源巨噬细胞(BMDMs)介导炎症后消退,小胶质细胞则持续驻留。 -
两个例外提示部分 TRMs 可融合 HSC 来源:
– 成年破骨细胞为 EMP 与 HSC 核融合形成的嵌合体。
– 肠道固有层可由 HSC/BMDM 补充并维持自我更新。
-
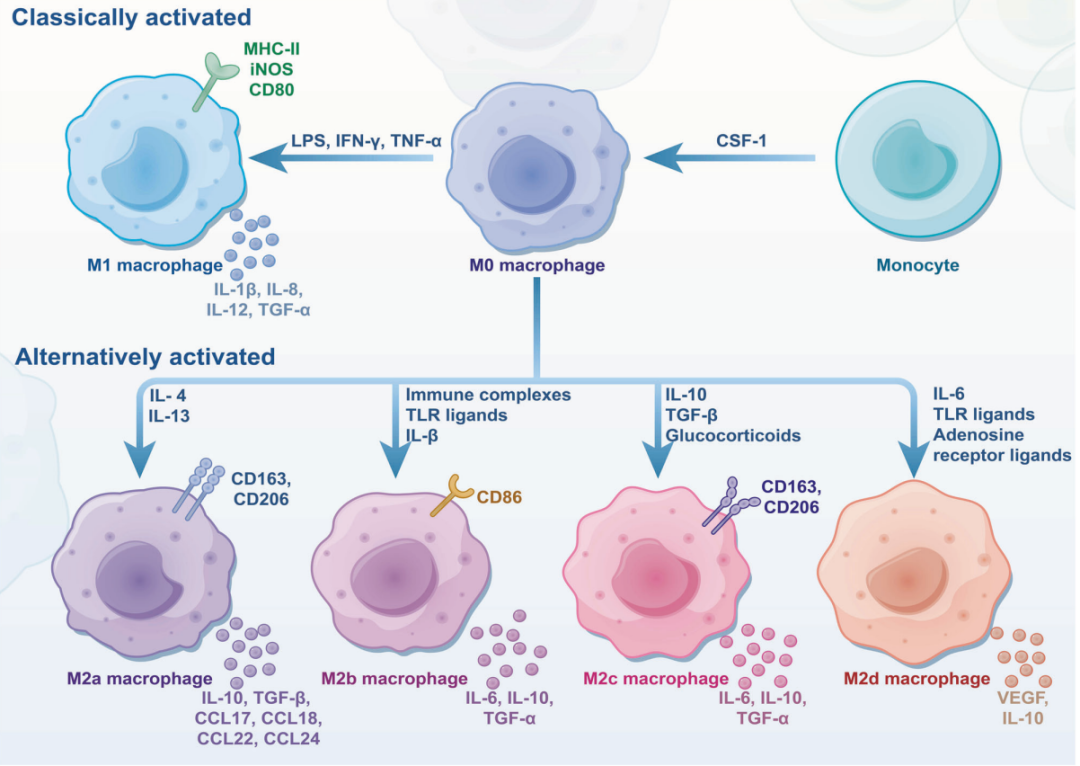
巨噬细胞极化是其针对微环境刺激产生特定表型与功能应答的过程;2000 年 Mills 等据此提出 M1/M2 二元分型,CD68 为共同标志。
– M0→M1:LPS + Th1 细胞因子(IFN-γ、TNF-α);M0→M2:Th2 细胞因子(IL-4、IL-10、TGF-β)。 -
信号轴决定命运:
– M1:TLR4/NF-κB、IFN-γ/JAK/STAT1;
– M2:PI3Kγ-Akt-mTOR、TGF-β/Smad、IL-4/STAT6、Wnt/β-catenin 等;
– PI3Kγ 通过 mTORC1-CEBPB/ITGA4 抑制 NF-κB,促 M2 并构建免疫抑制微环境。 -
M1(经典激活):高表达 MHC-II、iNOS、CD80、IL-1β、IL-12 等,产生 NO/ROS,抗微生物、抗肿瘤。
-
M2(替代激活)分 4 亚群:
– M2a(IL-4/IL-13):CD206/CD209/Dectin-1^hi,分泌 IL-10、CCL17-22、Arg-1,促修复但耗竭精氨酸、抑制 T 细胞,亦可促肿瘤。
– M2b(IC+TLR/IL-1β):双信号激活,CD86^hi,产 IL-10、IL-6、TGF-α,抑制 IL-12,介导免疫逃逸。
– M2c(IL-10/TGF-β/糖皮质激素):CD163/MerTK/CD206^hi,分泌 CCL16-18,高效清除凋亡细胞,降解 ECM,维持抗炎。
– M2d(IL-6+LIF+腺苷):CD14/CD163^hi、CD86^lo,分泌 VEGF/CCL18,促血管生成、抑制 T 细胞,助力肿瘤进展。 -
巨噬细胞可“再极化”,动态切换表型;M2 富集常与肿瘤不良预后相关。
-
M1/M2 框架简明,但单细胞测序显示真实异质性远超二元模型;同一亚群可在不同疾病背景下兼具促/抑功能,限制精准治疗。未来需细化亚群标志与功能,为个体化策略提供依据。
-
单细胞测序与谱系示踪等技术逐步揭示巨噬细胞在来源、分布、刺激、抗原表达、分泌因子及功能等多维度的高度异质性。
-
可高分辨率追踪其从前体到成熟的发育路径,发现肝、肺、肾、脑等部位存在独特亚群与功能特征,弥补传统 bulk 测序盲区。
-
借助 CellChat、CellPhoneDB 等工具可构建免疫微环境中细胞-细胞、配体-受体及信号通路互作网络,深入解析巨噬细胞的作用机制。
-
人鼠巨噬细胞在吞噬、抗原提呈、炎症与修复等核心功能上高度保守,使小鼠成为研究常用模型。
-
差异显著:人源高表达 CD14、HLA-DR;鼠源特异表达 F4/80、Arg-1、YM1;且同一组织内的亚群分类在两物种间并不完全对应。
-
实验设计与数据解读必须充分考虑物种特异性,以确保结果准确、可转化。
-
骨巨噬细胞分三类:骨髓巨噬细胞(含红细胞造血岛巨噬细胞 EIM、HSC 龛巨噬细胞等)、破骨细胞(osteoclasts)及骨膜/骨内膜巨噬细胞(osteomacs)。
-
EIM(红细胞造血岛巨噬细胞)
– 位于中央,周围包裹未成熟红系前体;>90% 小鼠 EIM 为 F4/80+EPOR+,人胎肝亦可见 EPOR+ 亚群。
– 高表达 VCAM1、CD169,分别与前体细胞的 VLA-4、CD43 结合,支持其增殖分化。
– 含 Mertk(吞噬去核后残余核质“pyrenocytes”)与 DNase2α(清除 DNA),维持红系生成微环境清洁。 -
破骨细胞
– 位于骨内膜吸收陷窝,分泌酸与蛋白酶完成骨吸收;TRAP 为其特异性标志。
– M-CSF 诱导前体表达 RANK → 与成骨/基质/T 细胞来源的 RANKL 结合 → 成熟破骨细胞。
– 胚胎期起源,成年后仍可融合循环单核细胞形成多核合胞体;活性不足致骨硬化,过度致骨质疏松。 -
OsteoMacs(骨膜/骨内膜巨噬细胞)
– 驻骨表面,星状突起形成网络;表达 CD68、F4/80、CD169,不表达 TRAP,可与成骨/破骨细胞直接对话。
– 调控成骨细胞活性与骨基质矿化,并具吞噬坏死细胞、抗原应答及免疫监视功能。
– 通过巨核细胞诱导的 Embigin 与 CD166 上调,支持小鼠造血维持。
-
外周血单核细胞是巨噬细胞的前体,骨髓释放后循环 1–3 天,随即迁入组织并分化为各型巨噬细胞或 DC。
-
人单核细胞三群:
– 经典型 CD14⁺⁺CD16⁻
– 中间型 CD14⁺⁺CD16⁺
– 非经典型 CD14⁺CD16⁺⁺
在 GM-CSF 或 CSF-1 刺激下均能获得巨噬细胞形态、分泌相关细胞因子并增强吞噬。 -
小鼠单核细胞按 Ly6C 表达分两群:
– Ly6Chigh:高 CCR2,趋化性强,多向促炎 M1 巨噬细胞分化。
– Ly6Clow:沿血管内皮巡逻,参与组织修复,倾向分化为 M2 巨噬细胞。
-
稳态肺内按解剖位置主要分为:
– 肺泡巨噬细胞(AMs):暴露于肺泡气腔;
– 2–3 群肺间质巨噬细胞(IMs):位于上皮-毛细血管间质区。 -
AMs 特征与功能
– 来源:卵黄囊 EMP;表型 CD11c⁺SiglecF⁺CX₃CR1⁻。
– 出生后填充肺泡,自我维持;成熟依赖 GM-CSF 与 TGF-β 诱导的 PPARγ 信号。
– 主要任务:清除肺表面活性物质、吞噬吸入颗粒、执行免疫监视。 -
IMs 特征与功能
– 表型 CX₃CR1⁺CD11b⁺SiglecF⁻;胚胎期单核细胞起源,成年后由循环单核细胞补充。
– 稳态时数量少,免疫挑战时迅速扩增;承担肺内免疫监视。
– 可再分亚群:
‑ 两群:LYVE1hi MHC-IIlow vs LYVE1low MHC-IIhi;
‑ 三群:依据 FOLR2、CCR2、TIM4、LYVE1、MHC-II 表达差异。
-
肝脏巨噬细胞组成多样:Kupffer 细胞(KCs)、肝被膜巨噬细胞(LCMs)、中央静脉巨噬细胞、脂质相关巨噬细胞等。
-
Kupffer 细胞(KCs)
– 占人体全部驻留巨噬细胞的 80–90%,源自卵黄囊 EMP,成年期定居肝窦。
– 核心标志:F4/80⁺、CLEC4F⁺、TIM4⁺;CLEC4F 为 KC 特征性 C 型凝集素,参与病原体识别与清除。
– 功能:清除血液内细胞碎片、衰老细胞、病原体;促进免疫耐受;调控铁、胆固醇及脂质系统代谢。
– 小鼠 KC 分两个亚群:
‑ KC1:CD206^low ESAM⁻ CD36^low
‑ KC2:CD206^hi ESAM⁺ CD36^hi(代谢活跃,通过脂肪酸转运体 CD36 调控肝脏代谢)。 -
肝被膜巨噬细胞(LCMs)
– 单核细胞来源,表型 F4/80⁺ CX₃CR1⁺ MHC-II⁺;参与中性粒细胞募集与免疫监视。 -
单细胞 RNA 测序(人肝)进一步将 CD68⁺ 肝内巨噬细胞分为两群:
– 群体 1(高 LYZ、CSTA、CD74):可能代表炎症性巨噬细胞;
– 群体 2(高 MARCO、VSIG4 等):与免疫耐受相关,发挥抑炎/耐受功能。
-
心脏与心包巨噬细胞对维持心肌稳态及应对病理刺激至关重要。
-
人心脏巨噬细胞(scRNA-seq)按 CCR2/HLA-DR 表达分三群: – CCR2⁺HLA-DR^low
– CCR2⁺HLA-DR^hi
– CCR2⁻HLA-DR^hi -
小鼠心脏巨噬细胞(scRNA-seq + 谱系追踪)分四群:
-
TIMD4 群:TIMD4⁺LYVE1⁺MHC-II^lowCCR2⁻,自我更新,不依赖血单核细胞。
-
MHC-II 群:TIMD4⁻LYVE1⁻MHC-II^hiCCR2⁻,部分可被单核细胞替代。
-
CCR2 群 & ISG 群:TIMD4⁻LYVE1⁻MHC-II^hiCCR2⁺,完全来源于单核细胞。
-
TIMD4⁺巨噬细胞功能: – 吞噬凋亡心肌细胞,减轻炎症;
– 调控纤维化,促进损伤修复,维持心脏结构与功能。 -
LYVE1 在心脏巨噬细胞表面与平滑肌细胞的透明质酸互作,维持血管稳态。
-
小鼠心包腔两群主要巨噬细胞: – Gata6⁺心包巨噬:表达 GATA6,转录谱与腹膜/胸膜 Gata6⁺巨噬相似,调控心肌损伤与梗死后纤维化。
– MHCII⁺心包巨噬:高表达 MHCII,主导抗原提呈,促进适应性免疫,协助清除损伤组织。
脾脏至少存在 4 个空间、表型与功能各异的巨噬细胞亚群:红髓、白髓及分隔二者的边缘区。
红髓巨噬细胞(RPMs)
– 起源:卵黄囊 + 胎肝祖细胞;表型 F4/80⁺VCAM1⁺CD11b^low。
– 功能:清除衰老红细胞、血小板等,防止自身免疫并回收铁/血红素;依赖 Spi-C、NRF2、PPARγ、LXRα、SREBP1 调控铁脂代谢。
– VCAM1(Spi-C 下游)也参与免疫调节与铁代谢,但其在 RPM 中的具体作用仍需深入研究。
边缘区巨噬细胞
– CD169⁺边缘区金属亲和巨噬细胞:与 B 细胞及 DC 互作,介导窦状免疫。
– MARCO⁺SIGNR-1⁺边缘区外层巨噬细胞:负责抗原捕获。
白髓巨噬细胞(WPMs)
– 位于 B 细胞滤泡,表型 CD68⁺F4/80⁻,类似淋巴结生发中心“tingible body”巨噬细胞;吞噬并清除凋亡 B 细胞。
-
淋巴结亚囊窦(subcapsular sinus)驻有窦状 CD169⁺巨噬细胞,表型与脾边缘区金属亲和巨噬细胞相似;负责捕获抗原并递交给 DC,进而激活 B、T 淋巴细胞。
-
髓质巨噬细胞表达 CD68 与 F4/80,其表达水平可因吞噬凋亡淋巴细胞而显著上调。
-
淋巴结被视为“巨噬细胞墓地”,因巨噬细胞在此区域发生局部更新与凋亡清除。
-
肠壁四层:黏膜、黏膜下层、肌层、浆膜;黏膜再分上皮、固有层、黏膜肌层;不同层存在不同巨噬细胞群,以固有层最为丰富。
-
固有层巨噬细胞(CD64⁺MHC-II^hiCD206⁺)
– 位于上皮下,出生前胎儿来源,出生后迅速被 CCR2 依赖的短寿命单核细胞替代,并需活菌共生。
– 功能:吞噬凋亡细胞/抗原,向隐窝干细胞提供 Wnt 配体维持增殖;大量分泌 IL-10,诱导菌群特异性调节性 T 细胞,维护肠屏障稳态。 -
外肌层与黏膜下亚组织龛中存在长寿命巨噬细胞(TIM4⁺MHC-II⁺),可自我更新,靠近血管及肠神经丛,参与维持肠蠕动、支持肠神经系统与血管发育与功能。
-
中枢神经系统(CNS)组织驻留巨噬细胞(TRMs)分布明确:
-
-
脑实质内为 小胶质细胞(microglia);
-
脑界面(脑室、脑膜、血管周围间隙)存在其他巨噬细胞亚群。
-
-
小胶质细胞来源与标志:
-
-
起源于卵黄囊EMPs,稳态下不受HSC贡献;
-
特异性表达 CX3CR1(脑内唯一),并可用 SALL1、P2RY12、TMEM119、HEXB 等与CNS其他巨噬细胞区分;
-
这些分子参与其转录调控、发育分化、炎症调节及神经保护。
-
-
自我维持与成熟依赖:
-
-
胚胎期进入CNS后,通过细胞自主增殖自我更新;
-
成熟依赖神经元产生的CSF-1和星形胶质细胞产生的IL-34激活CSF-1R信号;
-
成年期极少增殖,长期存活,发挥免疫监视、清除凋亡细胞、调节神经发生和突触功能。
-
-
脑周血管巨噬细胞(PVMs):
-
-
包括软脑膜巨噬细胞、脉络丛基质巨噬细胞等,分区与表型不同于小胶质细胞;
-
多数PVMs(如软脑膜)仅源于卵黄囊EMPs,成年期不被HSC或血单核细胞替代;
-
脉络丛基质巨噬细胞出生后可被血单核细胞替换;
-
脑室内(如Kolmer epiplexus细胞)为胚胎来源;硬脑膜巨噬细胞可部分由单核细胞补充。
-
-
功能:
-
-
PVMs通过调控动脉运动影响脑脊液(CSF)流体力学;
-
其TIM4⁺亚群促进细胞外基质(ECM)动态平衡。
-
-
病理状态:
-
-
一旦血脑屏障(BBB)受损,外周单核细胞和巨噬细胞亦可进入脑实质。
-
-
小鼠骨骼肌驻留巨噬细胞表型为 CD11b⁺F4/80⁺CD64⁺,来源包括卵黄囊与胎肝的胚胎造血祖细胞及成年后骨髓 definitive HSC。
-
单细胞测序将其分为三群:
– 自我更新驻留群:F4/80⁺LYVE1⁺TIM4⁺,可局部长期维持;
– F4/80⁺TIM4⁻ 群与 F4/80^lowCD11c⁺MHC-II⁺ 群:均源自单核细胞。 -
成体肌内两类巨噬细胞的存活均依赖成纤维-脂肪祖细胞(FAPs)产生的局部 CSF-1。
-
不同肌型巨噬细胞均差异表达转录因子 Maf、Mef2c、Tcf4,提示亚群特异性调控程序。
-
功能:维持组织稳态、促进肌肉生长与再生。
-
基本职责
-
清除细胞碎片、病原体、衰老或突变细胞;平衡炎症启动与消退;参与组织重塑、代谢调控和免疫防御。
-
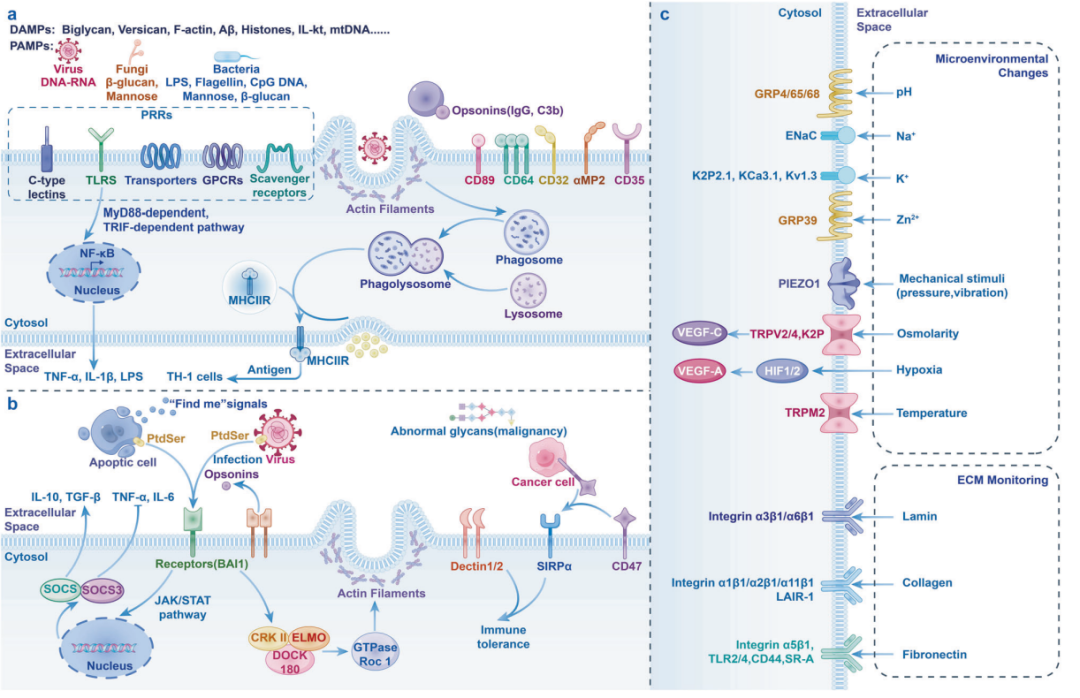
吞噬与清除
-
通过 PRR(TLR、CLR、SR)直接识别 PAMP/DAMP,或经 FcγR/CR 识别 IgG/C3b 调理颗粒。
-
形成吞噬杯 → 吞噬体 → 与溶酶体融合成吞噬溶酶体降解内容物;肌动蛋白重塑、BAR 蛋白、动力素等参与膜封闭。
-
凋亡细胞清除(efferocytosis):“find-me”(ATP、CX3CL1 等)→“eat-me”(PtdSer、calreticulin)→“don’t-eat-me”(CD47、MHC-I)调控;防止继发性坏死、维持耐受。
-
亚型与代谢
-
M1 型:依赖糖酵解,产生 IL-1β、TNF-α、NO 等,杀菌、抗肿瘤。
-
M2 型:依赖 TCA 循环与 FAO,分泌 IL-10、TGF-β,促进修复、血管生成。
-
α-KG、miR-155/125(M1)、miR-187/378-3p(M2)等代谢物/微小 RNA 控制极化。
-
抗原交叉提呈
-
脾边缘区(CD169⁺MZMM)、淋巴结被膜下窦、肝 Kupffer 细胞等摄取血源/淋巴抗原,通过 MHC-I 向 CD8⁺T 细胞交叉提呈,启动抗病毒、抗肿瘤免疫。
-
TIM4 延缓吞噬体成熟,保护抗原完整性;FOLR2⁺TAM 密度与乳腺癌存活正相关。
-
炎症调控
-
GM-CSF 驱动骨髓生成,增强单核/巨噬细胞功能;感染时迅速释放 TNF-α、IL-6、IL-12,激活血管内皮、招募 NK/T/B 细胞。
-
肠 CX3CR1⁺巨噬细胞分泌 IL-10、TGF-β,诱导 Tregs,维持屏障;肾巨噬细胞经 FcγRIV 清除免疫复合物。
-
组织修复与再生
-
心:TIM4⁺CCR2⁻ 驻留群吞噬凋亡心肌细胞,抑制炎症与纤维化;EphrinB2 促进修复。
-
肝:Kupffer 细胞分泌 WNT、HGF,支持肝祖细胞再生;缺失时肝修复延迟。
-
骨:破骨细胞降解 ECM,释放 IGF-1 刺激成骨;骨基质巨噬细胞吞噬凋亡骨细胞,调节钙磷平衡。
-
皮肤/肌肉:真皮 TIM4⁺、MHC-II⁺ 血管周围群与感觉神经互作,分泌 IGF-1、PDGF-CC 促进成纤维细胞与卫星细胞增殖,加速创面闭合与肌再生。
-
神经:小胶质细胞合成 desmosterol 促进再髓鞘;视网膜与 Müller 胶质协同清除凋亡细胞,维持昼夜节律。
-
生殖:Sertoli 细胞通过 efferocytosis 清除凋亡精原细胞,维持睾丸稳态。
-
稳态多水平信号网络
-
缺氧时 HIF-1/2 诱导 VEGF-A 促血管生成;肺泡巨噬细胞 PPAR-γ 感知表面活性物质,维持肺泡表面张力平衡。
-
机械力:PIEZO1 激活→EDN1、CXCL2 分泌,清除细菌;TRPM2 通道被发热温度敏化,调控细胞因子释放。
-
离子与 pH:GPR65/68 感知酸化,GPR65 抗炎、GPR68 促炎;K2P2.1 控制 K⁺外流激活 NLRP3;KCa3.1、Kv1.3 影响动脉粥样硬化、哮喘、卒中等炎症程度。
-
渗透压:TonEBP 上调 VEGF-C,驱动淋巴管增生;锌受体 GPR39 增强 IL-10,抑制肝纤维化。
-
铁循环:RPM/BMM 中 SPI-C 被血红素-Bach1 解抑制,促进 HO-1 表达,回收衰老红细胞铁。
一、总体概述
-
巨噬细胞是先天免疫系统的核心细胞,在多种疾病中发挥多重生物学功能。
-
作为第一道防线,它们维持组织稳态、调节炎症反应并促进伤口愈合。
-
最新研究揭示其在癌症、心血管病、自身免疫病、代谢病及神经退行性疾病中具有“双刃剑”作用。
-
作用机制涵盖:免疫微环境调控、促/抗炎、组织修复、细胞死亡通路干预等。
-
本部分聚焦巨噬细胞在上述疾病中的具体作用机制、表型多样性及动态可塑性。
二、癌症
2.1 肿瘤微环境(TME)中的巨噬细胞(TAM)
-
TME 中肿瘤细胞与基质/免疫细胞互作,重塑微环境,促进免疫逃逸、血管生成、耐药及共适应进化。
-
GM-CSF 是招募 TAM 的主要细胞因子;早期低水平 GM-CSF 具抗肿瘤作用,晚期高水平促瘤。
-
多种细胞因子(IL-17、IL-34、CXCL4/12、CCL2/5/20、CSF2 等)协同参与 TAM 招募。
-
泛癌分析:外周血巨噬细胞显著扩增,免疫检查点抑制剂(ICB)无应答者更多;抗原加工提呈能力下降。
-
肿瘤核苷酸代谢(CDA→UDP→P2Y6)驱动 TAM 招募并诱导免疫抑制表型,抵抗抗 PD-1 治疗。
-
IFI35 通过非经典 NF-κB 信号促进 TAM 招募。
2.2 M1-TAM
-
早期肿瘤:M1 型通过吞噬、提呈抗原、分泌 NO/ROS 及趋化因子(CCL5、CXCL9/10)激活 Th1/NK,抑制肿瘤。
-
举例:
-
GBP5 通过 JAK2/STAT1 诱导 CXCL9/10/11,促进 M1 极化。
-
敲低 YTHDF2 增强 M1 招募与 CD8+T 细胞毒活性。
-
奈铂激活 MAPK-p38/NF-κB 使 M2→M1 重编程。
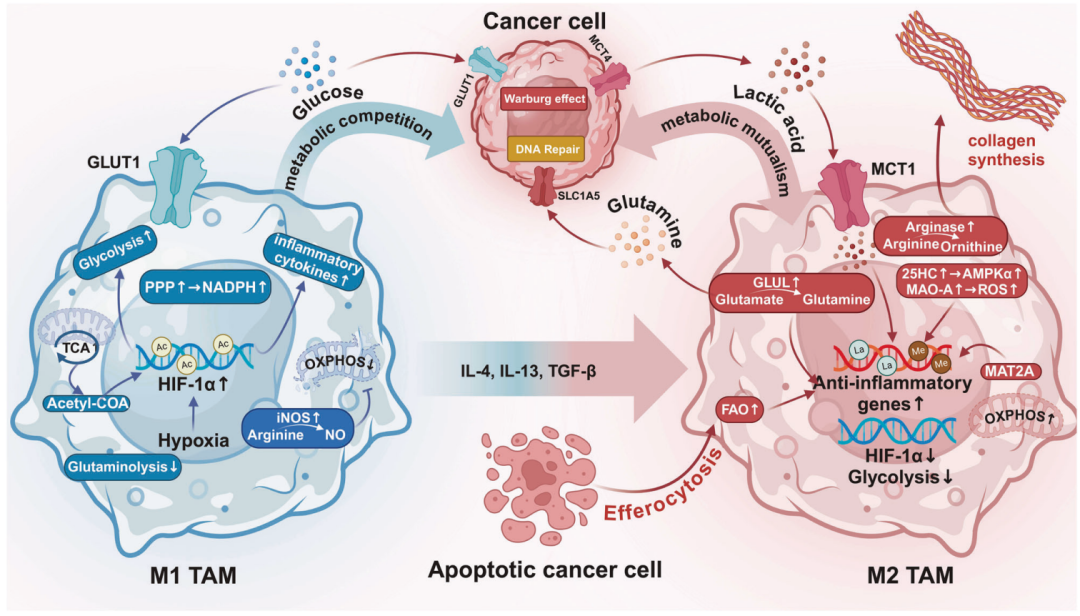
2.3 M2-TAM
-
晚期肿瘤以 M2 为主,具高度异质性,可共表达 M1/M2 基因。
-
M2 通过分泌 VEGF、MMP、TGF-β、Arg1、IDO、IL-4/10 等构建免疫抑制微环境,促进血管生成、侵袭、转移。
-
M2 代谢特征:氧化磷酸化、脂肪酸氧化、谷氨酰胺代谢活跃;乳酸/CSF-1 强化 M2 极化。
-
关键分子:SPP1、TREM2、APOE/C1、VEGFA、COL1A1/2/3、HMOX1 等定义不同 TAM 功能亚群。
-
空间分布:M2 多位于血管周围及坏死区,与缺氧适应、血管生成密切相关。
2.4 M1→M2 转化机制
-
缺氧、免疫-代谢重塑驱动 M1→M2。
-
肿瘤来源 IL-4/13、CSF、TGF-β、ECM 硬度、病毒(EBV)等参与极化。
-
凋亡肿瘤细胞释放 KRASG12D、B2M、外泌体等诱导 M2。
-
血小板通过 CD62P-PSGL1-JNK/STAT1-C5a 轴促进 M2。
2.5 促瘤生长与转移
-
TAM 分泌 TGF-β1、PTN、GPNMB、lncMMPA、galectin-3 等增强肿瘤干性、EMT、胶原交联、基质重塑。
-
脂质负载巨噬细胞(LLM)与胶质瘤细胞形成“脂质共生”,LXR-ABCA1/ABCG1 调控胆固醇外流。
-
CAF 与 TAM 互作:CAF 分泌 CXCL14/Chi3L1→M2 极化;M2 分泌 MMP 降解 ECM,共同促转移。
2.6 抑瘤作用与 M2→M1 重编程策略
-
CCL2+ TAM 在室管膜瘤中高表达促炎基因,可诱导肿瘤凋亡。
-
肿瘤释放 PTEN 结合 PLXCD2→JAK2/STAT1 重编程 M2→M1。
-
M1 外泌体(OX40L+)、PCB 高表达、YTHDF2 缺失、铁死亡标记 SAPE-OOH 等均可增强吞噬与 CD8+T 浸润。
-
阻断 CD47-SIRPα、CSF-1R、CCL2-CCR2、PI3Kγ、HDAC、Arg1 等靶点可诱导 M2→M1 转化。
2.7 促血管生成
-
TAM 分泌 EGF、PDGF、VEGF、FGF2、CXCL8、CCL18、ADM、PGE2 等诱导内皮增殖与趋化。
-
Tie2+ TEM 受 ANG2 趋化,与 EC 互作放大 Tie2 信号。
-
缺氧-HIF-VEGF、TEAD1-VEGFA、miR-21-5p-YAP1/HIF-1α、miR-301a-PTEN/PI3K/AKT 等轴促血管生成。
-
策略:PCN 纳米脂质体稳定血管连接,增强周细胞覆盖,改善药物递送。
2.8 免疫逃逸
-
M2-TAM 分泌 TGF-β/IL-10→抑制 NK、诱导 Treg、下调 DC 成熟与 CD8+T 功能。
-
消耗精氨酸(Arg1)、上调 PD-L1、分泌 CCL5/17/20/22 改变 T 细胞浸润谱。
-
凋亡肿瘤细胞诱导 AIM2-PD-L1/IDO、LXR/RXR-TGF-β/IL-10 轴,形成免疫耐受。
-
肥胖-代谢状态:mTORC1-PD-1、OXCT1-琥珀酸-H3K4me3-Arg1、TIM3+VISTA+ TAM 等机制导致 CD8+T 耗竭。
2.9 治疗策略与挑战
-
四大方向:抑制 TAM 招募、诱导 M2→M1 重编程、清除 TAM、增强吞噬(CD47-SIRPα 阻断)。
-
临床难点:脱靶(单核细胞减少)、免疫相关不良反应、耐药、转移加速、患者免疫反应异质性。
-
未来需整合多组学、单细胞-空间转录组、纳米递送、联合免疫检查点抑制剂,实现精准调控。
三、自身免疫病
3.1 类风关(RA)
-
滑膜巨噬细胞浸润程度与疾病活动度正相关,为生物标志物。
-
AtoM(CX3CR1hi 低 Ly6C/F4/80/IA-IE)是破骨细胞前体,驱动骨破坏。
-
IL-6/STAT3-RANKL 轴、NOTCH、ERK/MAPK、HIF-α-糖酵解等促 M1 极化。
-
治疗策略:
-
抑制 M1:GSKJ4、NOTCH 抑制剂、MB-3(KAT2A 抑制剂)。
-
促进 M2:SIRT1 激活、IL-10、GRK2-PPARγ 轴、M2-外泌体-PEG-MMP 可裂解纳米颗粒。
-
滑膜衬里层 MLS 与 FLS 互作:MET、PTX3、HBEGF 型巨噬细胞加剧炎症与侵袭。
3.2 系统性红斑狼疮(SLE)
-
巨噬细胞高表达 CD40L,激活 B 细胞、促进抗体产生;M1 主导,分泌 IFN-γ/IL-1β/IL-6/TNF-α。
-
吞噬凋亡细胞与免疫复合物能力下降;LAMTOR5 缺失致溶酶体功能障碍。
-
PKM2 高表达增强 TLR4/7/9;LPS- Caspase11-GSDMD 焦亡途径促 B 细胞分化。
-
治疗探索:
-
抑制 GSDMD(双硫仑)、EBI2-7α,25-OHC、miR-4512、精子素-JAK1 抑制。
-
诱导 M2(IL-4)、敲除清道夫受体、低 TGF-β 与预后相关。
-
注意 IL-10 在 IFN-α 存在下可转促炎,抑制 IFN-α 或 AKT2-IRF3 相互作用可缓解病情。
3.3 系统性硬化(SSc)
-
M2(CD163+)为主,分泌 TGF-β/PDGF/CCL18 促纤维化。
-
SPP1+ 巨噬细胞在肺/皮肤高纤维化区聚集;FCGR3A+ 巨噬表达 IL-6/CCL18。
-
混合 M1/M2 表型:Fli1 下调同时上调 CD163 与 CXCL10;ADAR1 缺失减轻纤维化。
-
JAK 抑制剂(鲁索替尼)同时阻断 IFN 与 IL-4/13 信号,减轻皮肤与肺纤维化。
-
纳米 PLG 抑制 MARCO+ 巨噬激活;B 细胞耗竭促促纤维化巨噬分化,为潜在靶点。
四、心血管疾病
4.1 分型与功能
-
心脏巨噬 8% 非心肌细胞;CCR2+ 单核来源(M1 样)与 CCR2- 组织驻留(M2 样)。
-
血管巨噬:新生儿 60% 源于卵黄囊,成人降至 20%,随年龄被骨髓来源替代。
-
亚群:Ly-6C/MHC-II/CD206/MerTK/CD11c 等标记定义 4 群;TRM 负责吞噬与稳态,MDM 主导炎症与重塑。
-
心肌纤维化:M1 分泌 IL-1/6/23、MMP 促胶原沉积;M2 分泌 IL-10/TGF-β 抑制炎症但亦可促纤维瘢痕。
-
代谢调控:NPM1 促糖酵解→氧化磷酸化转换增强修复;线粒体复合体 I 缺失则削弱囊泡分泌与瘢痕形成。
4.2 动脉粥样硬化(AS)
-
内皮低剪切力→LDL 滞留→oxLDL 激活内皮释放 M-CSF/CCL2/VCAM-1→Ly-6Chi 单核细胞迁入。
-
M1 主导进展期斑块,分泌 IL-1β/6/TNF-α、MMP1/3/10 促炎症、血栓、斑块不稳定;mTORC2 缺失、TRIM64-IκBα 泛素化加剧炎症。
-
M2 分泌 IL-10/TGF-β、促进胆固醇外排与胶原合成,但 CD163+ M2 通过 HIF-α/VEGFA 促血管新生与血栓。
-
泡沫细胞:SR-A/CD36/LOX-1 摄取 oxLDL,后期内质网应激-凋亡释放 MMP,扩大坏死核心。
-
治疗靶点:
-
促胆固醇外排:PPARα↑ABCA1/ABCG1/SR-BI;asprosin-p38/Elk-1↑ABCA1/ABCG1。
-
抑制 MMP:阻断 MCT4→组蛋白乳酸化修饰↑修复;激活 PPARγ 促 M2 极化。
4.3 心肌梗死(MI)
-
三阶段:炎症期(DAMP-TLR→Ly6Chi-CCR2+ M1 吞噬但分泌蛋白酶/ROS/细胞因子促纤维)、抗炎期、修复期。
-
修复性巨噬:Nr4a1 依赖,高 CD206/MerTK,分泌 IL-10/TGF-β/VEGFA/SPP1;TGF-β/Smad3 促胶原沉积,IL-10 亦可抑制 HuR/MMP9-胶原累积。
-
干预策略:
-
ADPN/AdipoR2/HMGB1 轴、IL-7 抗体、KLF2-EV、NPM1 代谢重编程、Bhlhe41+ 巨噬抑制肌成纤维细胞。
-
M2-sEV 减少 CCR2+ 促炎亚群,改善 AMI 预后。
五、神经退行性疾病
5.1 阿尔茨海默病(AD)
-
病理:Aβ 沉积与 tau 磷酸化;巨噬细胞(DIM 促炎、DAM 调节免疫)试图清除病理蛋白但能力有限。
-
DIM:高表达 IL-6/1β/TNF-α;DAM:依赖 TREM2,表达 Spp1/Igf1/Gpnmb,具吞噬与免疫调节功能。
-
治疗线索:
-
25-HC 促 DAM-IL-1β→DMM 抑制 SDH 可逆转。
-
EPO 信号增强外周巨噬细胞 Aβ 清除;IL-34 缺失降低 CD36/TREM2/MMP9 加重 AD。
-
抑制 Smad3、METTL3-YTHDF1-DNMT3A 轴增强 Aβ 清除;组蛋白乳酸化促 Aβ 生成需阻断。
5.2 帕金森病(PD)
-
α-突触核蛋白(α-syn)激活 LRRK2 激酶,招募单核细胞;过度表达致溶酶体功能下降、M1 极化、NADPH 氧化酶-ROS 恶性循环。
-
NLRP3 炎症小体激活加重神经炎症,其抑制可促进 M2 极化并减少 α-syn 聚集。
-
微胶质外泌体传播病理性 α-syn;PAAN/MIF 核酸酶抑制可保护多巴胺神经元。
-
未来方向:靶向 TREM2、修复血脑屏障、单细胞水平干预 DAM/DIM/BAM 亚群。
六、代谢性疾病
6.1 肥胖与胰岛素抵抗
-
肥胖脂肪组织巨噬(ATM)占比由 5% 升至 50%;M1 分泌 TNF-α/IL-6/1β→JNK/ERK/p38/NF-κB 通路诱发胰岛素抵抗。
-
特殊亚群:代谢激活型(MMe,高 CD36/PLIN2/ABCA1)、TREM2+ LAM、CD9+ ATM。
-
保护因素:嗜酸性粒细胞、运动-TRIB3-AKT、IL-4 条件外泌体、GPSM1 缺失-TNFAIP3-NF-κB 抑制、NOTCH 信号。
-
风险因素:mTORC1、P53、IgG-Ras-TGF-β/SMAD、PEPD-EGFR、胚胎维生素 D 缺乏-JARID2-MEF2/PGC-1α 轴。
6.2 非酒精性脂肪肝病(NAFLD)
-
病程:NAFL→NASH→纤维化→HCC;关键细胞:KC、LAM(GPNMB/SPP1/TREM2/CD9)、MoKC(TIM4- Ly6Chi CCR2+)。
-
早期:肝细胞脂肪变→CCL2/CXCL10-EV 激活 KC-IL-1β/TNF-α→抑制 PPARα 加重脂肪变。
-
NASH:YAP、XBP1、MS4A7-脂质滴-NLRP3、Zbtb18-FXR-FAO 等调控巨噬炎症与纤维化;持续肥胖致 TREM2 脱落,efferocytosis 丧失。
-
纤维化:瘢痕巨噬(IL-1β/SPP1/LGALS3/CCR2/TNFSF12)激活肝星状细胞;MerTK、MAIT 细胞促纤维化;METTL14-YTHDF1-GLS2 轴、CYR61-IRAK4/SYK/NF-κB 轴参与。
-
HCC:TREM2+ GPNMB+ APOE+ TAM 营造免疫抑制微环境;FGFR1 缺失、FGF21-TLR4-IL-17A、Neuregulin 4、瘦素、Rab27a-EV-YAP-CYR61 等调控肿瘤生长与免疫逃逸。
-
治疗前景:CCR2/CCR5 双拮抗、TREM2 抑制剂、PPAR/GLP-1 激动剂、巨噬药物递送系统(硬壳微泡、脂质体)正在临床试验。
一、巨噬细胞作为治疗靶点的总体思路
-
巨噬细胞在“炎症启动”与“炎症消退”中均起主动作用,是自身免疫病与肿瘤免疫治疗的有希望的靶细胞。
-
干预方向需区分“癌症”与“非癌症”场景:
-
肿瘤:抑制或重编程促肿瘤的 M2 型→促炎 M1 型;或联合免疫检查点(PD-1、CTLA-4)。
-
炎性疾病:抑制过度活化的 M1 或诱导 M2 样抗炎反应,促进组织修复。
-
纤维化疾病:M2 促纤维化、M1 抗纤维化,因此需阻断 TGF-β 等促纤维化信号、促 ECM 降解、阻断巨噬细胞募集。
-
目前抗癌策略归纳为:耗竭、重编程、招募调控、代谢/功能调节(见原文 Table 3)。
二、药物递送新平台(细胞、病毒、纳米颗粒)
-
利用巨噬细胞把细胞因子(IFN-α、IL-12)“驮运”到肿瘤部位,已进入临床前/临床探索。
-
相比传统给药,细胞/病毒/纳米载体对“耐药”或“血脑屏障(BBB)渗透性差”的疾病提供更多可能。
-
可递送肽、DNA、miRNA、circRNA 等,直接调控巨噬细胞分化与极化(含 TAM)。
三、已上市或已进入临床的“小分子/抗体”类药物
A. CSF-1/CSF-1R 轴
-
机制:阻断 CSF-1R→减少巨噬细胞存活/增殖,促使 TAM 从 MHC-II^low 向 MHC-II^high 转变,增强免疫刺激能力。
-
代表药物:
-
Pexidartinib(PLX3397):FDA 已获批用于腱鞘巨细胞瘤;对复发胶质母细胞瘤耐受性好但 PFS 无显著延长。
-
JNJ-40346527:复发/难治霍奇金淋巴瘤显效。
-
BLZ945:与 IGF1R/PI3K 抑制剂联用可逆转 TAM 表型,治疗胶质瘤的试验进行中。
-
Emactuzumab(RG7155):人源化抗 CSF-1R 单抗,腱鞘巨细胞瘤 I 期客观缓解率 86%(24/28),但长期耗竭巨噬细胞可致体内稳态失衡。
B. 双膦酸盐选择性清除 TAM
-
Clodronate-脂质体:被巨噬细胞吞噬后诱导凋亡;动物模型显著减少肺癌骨转移、乳腺癌转移、黑色素瘤转移。
-
乳腺癌 1069 例 RCT:clodronate 降低骨转移发生率;与顺铂/索拉非尼等化疗药协同增效,但不同癌种临床结果不一致。
C. GM-CSF 及其抑制剂
-
GM-CSF 激动剂
-
Sargramostim(Leukine):FDA 批准用于 AML 化疗后、NHL/ALL/霍奇金病自体/异体 BMT 后。
-
Molgramostim:联合抗生素逆转脓毒症免疫抑制,减少感染并发症。
-
作为疫苗佐剂:前列腺癌 DNA 疫苗Ⅰ/Ⅱ期试验中,GM-CSF 仅带来轻度获益,并非必需。
-
GM-CSF 抑制剂
-
Mavrilimumab 等用于类风湿关节炎、COVID-19 细胞因子风暴;其它抑制剂(Gimsilumab、Namilumab)疗效未优于安慰剂。
D. CCL2-CCR2 轴
-
肿瘤分泌 CCL2→招募 CCR2^+ 单核细胞→分化为 TAM;阻断该轴可抑制肿瘤生长与转移,但停药后出现“反跳”加速转移。
-
临床单药疗效不足;代表药物:
-
Carlumab(抗 CCL2):前列腺/卵巢癌模型增敏化疗,临床未达主要终点。
-
PF-04136309(CCR2 小分子抑制剂):联合 FOLFIRINOX 改善晚期胰腺癌疗效,但与白蛋白紫杉醇+吉西他滨联用出现肺毒性且无额外获益。
E. CD47-SIRPα 轴
-
肿瘤细胞高表达 CD47→结合巨噬细胞 SIRPα→抑制吞噬;阻断该轴促吞噬。
-
临床/临床前药物:
-
Magrolimab(Hu5F9-G4):AML 1b 期试验中位 OS 9.8 月(TP53 突变)/18.9 月(野生型)。
-
TTI-621:血液肿瘤 I 期 ORR 13%。
-
新一代策略:
-
氧增强光动力+铁死亡+CD47 阻断仿生纳米平台(Ce6+Hemin+PEP20)→乳腺癌原发灶及肺转移显著减少。
-
杂交膜纳米囊(hEL-RS17)联合 RRX-001、IR820、聚甲双胍→4T1/B16F10 模型显著抑瘤。
-
副作用:CD47 广泛表达,抗体可致红细胞结合→严重贫血;靶向 QPCTL(催化 CD47 焦谷氨酰胺化)可望降低在靶脱毒。
F. CD40-CD40L 轴
-
CD40 激动→促 M1 极化、增强 IL-12/TNF-α 等促炎因子;代表药物:
-
Sotigalimab(APX005M):与化/免疗联用耐受良好。
-
Selicrelumab:实体瘤中与免疫检查点抑制剂联用显效,但需警惕细胞因子释放综合征(CRS)。
四、基于巨噬细胞的“细胞疗法”
A. 三大策略
-
体外教育或扩增的自体/异体巨噬细胞(Ex vivo educated)。
-
巨噬细胞作为“活药物载体”递送小分子、质粒 DNA 等。
-
基因工程巨噬细胞(如 CAR-M、CAR-iMac)。
B. 代表产品/试验
-
Ixmyelocel-T(自体骨髓 MSC+M2 样巨噬+造血细胞混合制剂)
-
用于严重肢体缺血、扩张性心肌病;Ⅱ期试验显著降低主要不良心脏事件(MACE),改善截肢率与生活质量。
-
CAR-M
-
体外把 HER2-CD3ζ-CAR 转入巨噬细胞→小鼠卵巢癌模型抑瘤、延长生存、减少肺转移,且能把 TME 中的 M2 转为 M1。
-
首次人体试验:CT-0508(抗 HER2 CAR-M,NCT04660929)初步显示安全、可耐受、肿瘤浸润与免疫激活。
-
CAR-iMac(iPSC 来源)
-
高产量、纯度;对 CD19^+ 淋巴瘤、间皮素^+ 卵巢癌显示抗原依赖吞噬与杀伤;CD19-CAR-iMac 小鼠白血病模型显著延长生存。
-
已开展 GBM、胰腺癌等临床前研究。
五、纳米药物递送系统(NDDS)在巨噬细胞治疗中的进展
A. 总体优势
-
提高药物稳定性、生物利用度,降低副作用;可穿越 BBB;易实现多药联合。
-
两大设计思路:
-
靶向巨噬细胞的 NDDS(配体-受体识别)。
-
以巨噬细胞/其胞外囊泡(EV)为载体的 NDDS(膜包裹或 EV 包被纳米粒)。
B. 典型纳米平台与机制举例
-
pIL12+PLX@cR-PssPD:肿瘤微环境降解释放 PLX3397(CSF-1R 抑制剂)+ IL-12 质粒→协同促 T 细胞激活、减少 MDSC、重极化 TAM。
-
Sun 等-唾液酸修饰纳米粒:通过 CD169 靶向 M2 巨噬,递送 CSF-1R siRNA→前列腺癌模型重极化 TAM。
-
CCR2-MM@PLGA/Cur:工程化巨噬膜高表达 CCR2,主动靶向脊髓损伤区,中和 CCL2→减少微胶质 M1 极化、促神经再生。
-
Mg₂Si 纳米片水凝胶(MSN@CS/HA):长效产氢→促进深Ⅱ°烧伤 M2 极化、促血管生成、减纤维化。
-
BBLZ-945@PAC-PTX“多米诺”纳米凝胶:ATP 触发释放 BLZ-945 耗竭 TAM,同时 PAC-PTX 阻断 CXCR4→增强免疫细胞浸润。
-
CV-S NPs(载 VPA):抑制 TLR4-MyD88-NF-κB 轴→减少人原代巨噬 TNF-α 分泌。
-
PIR@M(巨噬膜包裹 PLGA-ION-R837):TLR7 激动剂协同 Fe₃O₄→将 TAM 由 M2 转为 M1。
-
RP-182-DNA 纳米载体:靶向 M2 的 RP-182 肽激活 CD206→促自噬、恢复 M1 表型;随后引入 ErbB2-CAR 形成 CAR-M,增强抗原提呈与 CD8^+ T 细胞浸润。
-
OP-101(PAMAM-NAC):靶向活化巨噬,COVID-19 Ⅱa 期试验降低 60 天插管/死亡复合终点,安全且减炎。
六、挑战与未来方向
-
M1/M2 二元分类的局限
-
巨噬细胞状态动态可变,组织特异性亚群多样;现有标志物特异性不足,各研究标准不一。
-
亟需发现“更精准”的极化标志与亚群分选方法,以指导靶向治疗。
-
安全性平衡
-
过度激活可诱发/加重自身免疫或炎症;治疗设计需兼顾“有效”与“安全”。
-
NDDS 瓶颈
-
新型纳米材料的免疫原性、长期毒性未明;生产工艺复杂、成本高;体内精准释药仍需优化。
-
临床转化
-
目前进入临床的纳米-巨噬细胞项目极少,除 OP-101 外多处于临床前;需扩大规范试验、优化联合方案。
一、组织巨噬细胞的核心地位
-
维持组织稳态、调控免疫、介导多种疾病病理过程。
-
来源:原始造血祖细胞(EMP)、造血干细胞(HSC)等;EMP 及其前体(PreMac)是胚胎期组织驻留巨噬细胞(TRM)的主要贡献者。
-
组织微环境显著塑造其身份与功能,表现为组织特异性转录谱与表型;不同祖细胞来源的 TRM 在相同组织中的整合与反应差异仍需阐明。
二、功能与病理关联
-
生理功能:清除病原体、抗原提呈、修复组织、调节铁代谢。
-
病理失衡:
-
肿瘤微环境(TME):TAM 可与其它细胞交叉对话,既可促瘤也可抑瘤。
-
自身免疫:释放促炎因子维持炎症。
-
代谢病:脂肪组织浸润→促炎因子→全身胰岛素抵抗。
-
神经退行:释放神经毒性物质加速神经元死亡。
-
未知领域:
-
组织特异性编程的精确分子机制。
-
HSC 来源与 EMP 来源巨噬细胞在相同信号下的整合反应差异。
-
长期互作对组织完整性的影响及反向调控。
-
调控自我更新与长期维持的具体信号。
三、技术推动深度解析
-
单细胞组学、空间转录组、遗传操控、先进成像、高维流式/质谱、生物信息学+传统细胞分子生物学,将提供前所未有的洞察。
四、治疗新机遇(基于异质性与可塑性)
-
表型重塑
-
促炎 M1 ↔ 抗炎 M2 的可逆转换是治疗杠杆;需进一步解析调控网络以精准干预。
-
选择性清除/重编程致病亚群
-
抗体-药物偶联、脂质体、基因编辑等手段靶向肿瘤或纤维化相关巨噬细胞。
-
“特洛伊木马”递送
-
巨噬细胞可内化并运载药物、纳米粒或基因治疗载体至病灶,提高局部浓度、降低脱靶。
-
体外工程化细胞疗法
-
自体/异体巨噬细胞体外极化或基因修饰后回输,补充/替代功能失调群体,促进组织再生(心梗、慢性创面等)。
-
挑战:规模化生产、长期存活与功能维持。
-
信号通路精细调控
-
小分子或生物制剂靶向炎症、吞噬、代谢等关键通路,微调而非整体耗竭。
-
微生物组-巨噬细胞互作新领域
-
肠道菌群可影响巨噬细胞极化与全身炎症;解析有益/有害菌株或代谢物,可为代谢病、IBD 等提供新干预思路。
五、亟待解决的关键问题
-
如何精准重塑 TME,实现 TAM 从“促瘤”到“抑瘤”表型的高效转化?
-
如何设计更高效的巨噬细胞基药物递送系统?
-
如何增强 CAR-M 细胞的细胞毒与抗肿瘤功能?
-
如何开发更有效策略以选择性清除特定有害巨噬细胞亚群?
-
需要更准确的巨噬细胞分型与预测模型,指导个体化治疗。
-
如何确保巨噬细胞疗法的安全性,避免脱靶与长期副作用?
-
需持续研究并克服针对巨噬细胞干预的耐药机制。
-
鉴定哪些特定菌株或菌群代谢物对巨噬细胞功能有益/有害?
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫