1.发生机制和病理生理改变
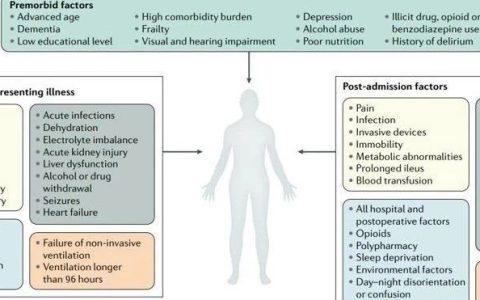
2.诱发因素
3.临床表现和诊断依据
4.围术期管理
4.1术前评估与准备
4.2术中管理
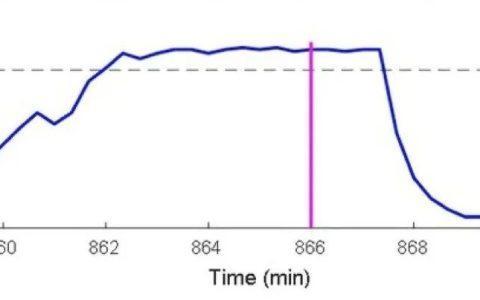
4.3“寂静肺”的处理
-
增加纯氧吸入浓度,加大氧流量至8 L/min,进行手动通气维持氧合。 -
加深麻醉,通过增加七氟醚吸入浓度至最大(8%),和/或静脉输注丙泊酚来增加麻醉深度。 -
肾上腺素,因其具有β2受体激动作用,扩张支气管作用较强,其β受体作用可以改善气道黏膜水肿,建议首次静脉推注10~30 p.g,并根据患者“寂静肺”缓解的具体情况增加剂量。由于肾上腺素具有的α受体作用,用药期间需要密切监测,防止心动过速以及高血压的发生;对于孕妇以及糖尿病、青光眼(开角型青光眼除外)、甲状腺功能亢进症、精神神经症和严重心律失常患者,需要谨慎使用。 -
β2受体激动剂,如沙丁胺醇气雾剂8~10揿经气管导管喷入气管内用以扩张支气管。 -
糖皮质激素类药物,具有抗炎和减轻气道水肿的作用,可采用氢化可的松100 mg或甲强龙80 mg静脉滴注。 -
硫酸镁可能对难治性支气管痉挛有效,可静脉滴注硫酸镁2 g,滴注时间不少于20 min。此外,“寂静肺”患者PEEP升高,外源性PEEP(extrinsic positive end-expiratory,PEEPe)介入治疗有助于纠正通气/血流比例失调,改善患者血气状态及预后,减少住院时间,故术中可根据PEEP水平设置PEEPe。
4.4拔管处理
4.5术后管理
-
调整患者枕头高度; -
预防胃一食管反流,对有胃一食管反流病的患者,视情况应用抑酸药; -
对于术后剧烈疼痛及紧张焦虑的患者,应及时给予对症支持治疗; -
对于哮喘患者,术后需及早恢复术前的规律治疗; -
并根据患者手术后具体情况,鼓励其及早进行肺功能锻炼及下地活动,促进肺功能恢复。
5.小结
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫