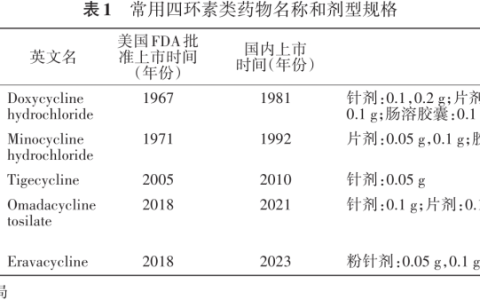
文献特点:发表于最近5年,能提供很高的循证医学依据。设及到的是临床常用的技能,值得深入学习。
期刊特点:本文发表在《Progress in Cardiovascular Diseases》(Prog Cardiovasc Dis),这是一心血管领域期刊,创刊于1958年,由Elsevier出版,专注于心血管疾病的综合研究。2020年影响因子约为3.5(近几年都呈上升趋势),JCR Q1,属于心血管领域中等偏上水平,学术认可度高。
主动脉内球囊反搏(IABP)已在心血管疾病治疗领域常规临床应用长达五十年。然而,其常规使用价值愈发受到质疑。IABP反搏作用的治疗目标在于增加冠状动脉血流并降低左心室后负荷。然而,多项体内研究揭示了生理性代偿反应可能抵消该装置预期疗效的机制。
大型随机对照试验表明,在IABP的主要适应症(如心肌梗死相关心源性休克、无休克的高危心肌梗死患者以及择期高危经皮冠状动脉介入治疗)中,该装置未能显示出临床获益。由于国际指南对这些结果的解读存在差异且证据评估标准不统一,IABP的实际使用频率呈现出显著的地区性差异。当前研究重点已转向其他主动型机械循环辅助装置,这使得基于循证医学证据界定IABP潜在最终适应症范围的研究面临更大挑战(更难界定IABP的应用范围)。
关键词
intra-aortic balloon pump; intra-aortic counterpulsation; mechanical
circulatory support, myocardial infarction; cardiogenic shock; percutaneous coronary
intervention; coronary artery bypass grafting; decompensated heart failure
主动脉内球囊反搏(IABP)是过去五十余年间临床应用最广泛的机械循环辅助装置。
其首次人体应用可追溯至1967年,用于治疗心肌梗死相关心源性休克(CS),这一适应症在随后数十年间始终占据重要地位。然而,过去十年间,一项大型随机对照试验的中性结果与观察性研究数据共同导致IABP的临床应用模式发生显著转变。
本综述旨在系统阐述IABP的作用原理、不良反应、当前循证医学证据、指南推荐意见及其可能保留的残余适应症。
IABP基本原理
IABP系统由球囊导管与驱动泵控制台组成。球囊容积可达50 mL,通过股动脉穿刺在透视引导下将球囊定位于锁骨下动脉远端1-2 cm处(肾动脉开口上方)。控制台以心电图(ECG)触发同步,于舒张期向球囊内注入氦气使其充盈,收缩期快速排气。这种反搏机制通过提升舒张期血压峰值(BP)改善冠状动脉血流,同时收缩期球囊塌陷可减少主动脉内容积(相当于球囊体积),从而降低左心室(LV)后负荷并实现潜在的心室减负(如图)。
动物实验及早期临床试验表明,该机制可增加心肌氧供并降低氧耗。然而,一项针对心源性休克(CS)患者的前后对照观察性研究显示,IABP的血流动力学效应微弱,心输出量仅增加约0.5 L/min。另一小型随机对照试验亦证实其心输出量改善效果与对照组无显著差异。相较于微型轴流式左室辅助装置或静脉-动脉体外膜肺氧合(ECMO)等主动型机械循环支持装置,IABP提供的血流动力学支持强度最低(若存在)。
近期一项针对缺血性心肌病经皮冠状动脉介入治疗(PCI)患者的体内研究表明,IABP对冠状动脉血流的影响可能被冠状动脉自身调节机制所削弱——远端冠脉压力升高导致微血管阻力增加。研究者据此推测,IABP仅能在局部微循环储备耗竭时提升心肌灌注(IABP导致的远端冠脉压力升高,反而触发微血管收缩-阻力增加,抵消了压力升高带来的血流增加效应)。
尽管报道的并发症发生率存在较大差异,但主动脉内球囊反搏(IABP)治疗可能增加局部及全身并发症风险。
早期使用大口径导管(达15F)的IABP系统研究发现,其与肢体缺血、血管夹层及穿刺部位出血等血管并发症风险升高相关。因此,现行导管系统已显著改良为更小尺寸(6-7F)并引入无鞘置入技术,使得严重全身并发症(如大出血、卒中及全身性感染)发生率降低。
表1总结了近期IABP与对照组在不同适应症中各类并发症发生率的随机试验数据。
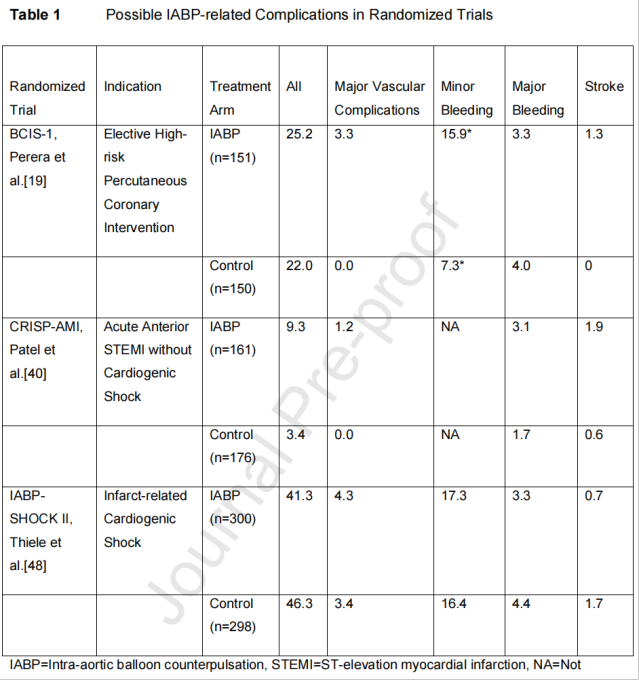
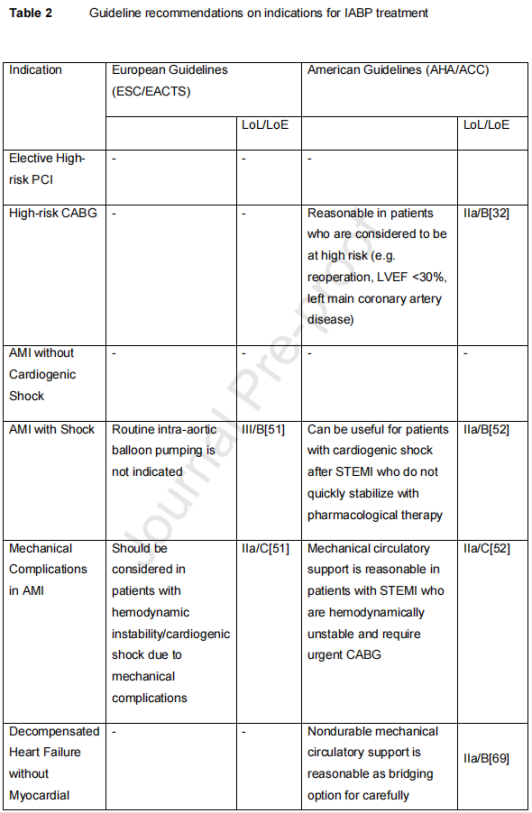
表2总结了IABP临床适应症的指南建议
择期高危经皮冠状动脉介入治疗
择期高危经皮冠状动脉介入治疗(PCI)曾被视为IABP的主要适应症之一。尽管回顾性研究提示其可能改善临床预后,但欧美指南从未对此情境下的IABP使用给出明确推荐。
2010年,Perera等发表了首个针对高危PCI术中常规IABP支持的随机对照试验(BCIS-1研究),共纳入301例患者。研究将高危PCI定义为:左心室射血分数(LVEF)≤30%且通过改良Duke Jeopardy评分评估存在广泛冠状动脉病变。主要复合终点(住院期间死亡、急性心肌梗死、脑血管事件或再次血运重建)在常规IABP组与临时IABP组间无显著差异。然而,该试验51个月的长期随访显示,常规IABP组患者生存率显著优于对照组(风险比0.66;95%CI 0.44–0.98;p=0.039)。这一结果仍无明确解释,因短期随访中两组主要不良心脑血管事件(MACCE)发生率相同,且心肌梗死面积亦无差异,提示可能为偶然发现。目前,BCIS-1仍是该领域唯一随机对照研究,尚无专门针对择期高危PCI的Meta分析。
目前欧洲指南始终未对择期高危PCI中的IABP使用提出具体建议。美国指南指出在经严格筛选的高危患者(如无保护左主干或唯一通畅血管PCI、LVEF严重减低且靶血管支配大面积心肌区域)中,择期使用适当血流动力学辅助装置辅助PCI可能是合理的(推荐等级IIb,证据水平C),但未明确指定器械类型,同时提及BCIS-1的中性结果。
知识点归纳:
“无保护左主干”,是心血管介入治疗中的专业术语,特指左冠状动脉主干(Left Main Coronary Artery, LMCA)存在严重狭窄或闭塞,且缺乏有效的侧支循环或其他桥血管代偿供血的状态。
IABP在高危冠状动脉旁路移植术(CABG)
中的应用现状
在心血管外科临床实践中,术前使用IABP仍是高危CABG患者的常见策略。早期小型随机研究表明,对于左室射血分数(LVEF)降低、优化药物治疗后仍存在不稳定型心绞痛或接受二次CABG的患者,无论采用体外循环(on-pump)或非体外循环(off-pump)术式,术前IABP均可降低死亡率并缩短住院时间。然而,这些研究普遍存在以下缺陷:样本量小(多数纳入
既往欧洲指南未对高危CABG中IABP使用提出具体建议。美国指南认为IABP适用于无严重症状性主–髂动脉闭塞或外周动脉疾病的高危CABG患者(如二次手术、LVEF或左主干病变),推荐等级IIa(证据水平B)。
目前仍缺乏大规模RCT验证IABP在高危CABG中的确切价值。需明确可能获益的精准高危亚组(如心肺转流脱机困难或术后心源性休克患者)。现有指南未涵盖术后IABP支持(如2-6%患者发生的术后心源性休克)的循证推荐。
IABP在AMI不伴CS患者中的应用
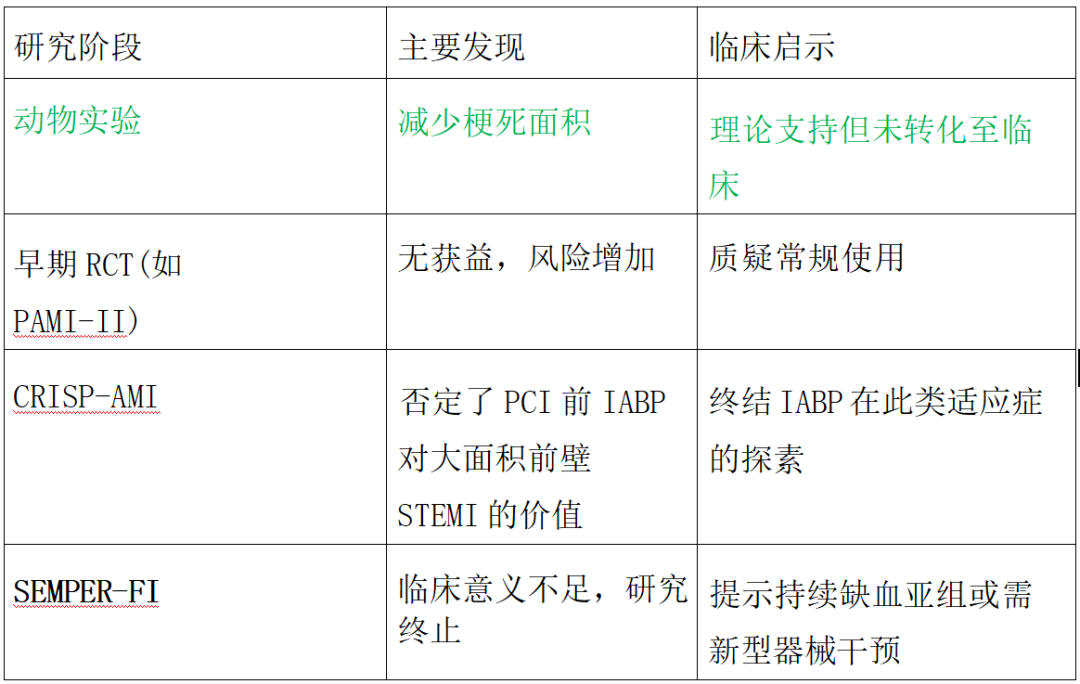
在血运重建治疗(PCI)普及前的动物实验及小型临床研究中,IABP在AMI(无心源性休克)患者中显示潜在获益,包括减少梗死面积。其机制被认为与改善再灌注前冠状动脉血流相关。后续随机研究(如PAMI-II试验)表明,在高危STEMI患者中(即使定义标准各异),无论IABP在PCI前或后置入,均未显示临床获益。这些研究的局限性包括:PCI中支架置入率低,IABP多在PCI后使用,”高危”定义不一致(如Van’t Hof研究仅基于ST段偏移程度)。
为进一步验证”PCI前IABP支持对大面积前壁STEMI有益”的假说,CRISP-AMI试验将337例大面积前壁STEMI患者随机分为PCI前IABP组与单纯PCI组,结果显示主要终点(心脏磁共振评估梗死面积)无差异;次要终点(30天及6个月全因死亡率、主要心血管不良事件)无差异。
多项Meta分析(涵盖上述研究)证实,IABP在无心源性休克的STEMI患者中无显著临床获益,IABP治疗显著增加出血与卒中风险,基于此,国际指南均未推荐IABP用于此类适应症。
后续的实验进一步进行了探索。CRISP-AMI亚组分析显示,PCI后持续缺血患者(n=36)可能从IABP中生存获益,但6个月死亡率达24%,样本量过小限制结论可靠性。SEMPER-FI试验初步结果(n=100/计划400例),主要终点(6个月死亡率)无差异(效能不足),IABP组ST段回落更显著(73% vs 56%, p无临床转化意义。因而作者未计划继续推进该试验。
IABP在心肌梗死相关心源性休克
(MI-Related CS)中的应用
过去,非随机研究和观察性Meta分析提示IABP可能改善心梗合并心源性休克(CS)患者的预后。基于此,欧美指南曾推荐其常规使用(美国指南:IB类;欧洲指南:IC类)。然而,这些获益结论高度依赖于再灌注治疗时代背景:在溶栓治疗主导时代(如CRISPR-AMI试验)显示潜在优势;直接PCI时代下,部分Meta分析反而提示IABP增加死亡率。
而进行随机试验相关结果均未显示额外获益。IABP-SHOCK I(n=40),首个RCT显示IABP对APACHE II评分改善无显著差异,且未能优化心脏指数或外周血管阻力。IABP-SHOCK II(n=600),主要终点(30天全因死亡率),IABP组相对风险RR 0.96(95%CI 0.79-1.17; p=0.69),中期(1年)与长期(中位6.2年)随访均无生存差异。
因此欧洲指南将常规IABP使用降级为Ⅲ类推荐(证据水平B)。美国指南(未纳入IABP-SHOCK II研究结果),仍保留IIa类推荐(证据B级)。在使用率上两者也存在明显差异,美国约30% vs 欧洲
IABP-SHOCK II中87%病例于PCI后置入。回顾性研究提示PCI前置入或改善生存,但存在显著选择偏倚(纳入患者CS严重度低)。波兰注册研究,PCI失败者(TIMI 0-1级血流)使用IABP可能获益,成功PCI者反增死亡风险;而Shock亚组分析,IABP-SHOCK II队列显示PCI成功与否均无差异。
未来的研究中,主动型装置(如Impella、ECMO)使用率仍,且缺乏生存获益证据,因此更加需要明确IABP在特定亚组(如难治性微循环衰竭)中的潜在价值,PCI前置入的最佳时机选择需更高证据等级研究验证。
IABP在急性心肌梗死(AMI)机械并发症时的应用
AMI机械性并发症较为罕见。这一特点使得为这类患者寻求最佳治疗方案时难以积累足够的循证医学证据。
动物实验表明,在急性二尖瓣反流(MR)情况下,置入主动脉内球囊反搏(IABP)可提高心输出量、血压及颈动脉血流。然而,左心室收缩力与冠状动脉血流并未发生改变,血压升高的机制仍不明确。
一项针对81例室间隔破裂或急性二尖瓣反流患者的小型回顾性研究分析了IABP置入对心源性休克(CS)或未完全符合CS标准但存在严重血流动力学不稳定患者,30天死亡率影响。总体而言,术前应用IABP的CS患者30天生存率得到改善;而对于未出现明确休克表现但存在严重血流动力学不稳定的患者,IABP的使用并未改变其死亡率。Cox回归分析显示,未进行手术修复及心源性休克早期进展是30天死亡率的独立预测因素。近期一项针对93例缺血性二尖瓣反流接受外科二尖瓣修复术患者的回顾性研究指出,35%的患者接受了IABP治疗(主要适应症为术前心源性休克),但研究发现围术期IABP使用与患者死亡存在独立相关性。不过需注意该研究中可能存在心源性休克与IABP使用之间的强共线性干扰。
当前美国与欧洲指南基于专家共识(证据等级C),推荐将IABP用于心源性休克合并机械并发症的治疗。
IABP在非心肌梗死(MI)相关失代偿性心力衰竭(HF)IABP的使用
与急性心肌梗死(AMI)患者不同,非缺血性病因导致的失代偿性心力衰竭(HF)患者具有显著差异。目前,关于此类患者使用主动脉内球囊反搏(IABP)的最佳随机证据来自den Uil等人开展的一项小型试验。该研究纳入33例因低心输出量(包括新发或慢性HF急性加重)且对大剂量利尿剂无效的失代偿性HF患者,按1:1比例随机分配至单纯IABP治疗组(不使用正性肌力药物)或正性肌力药物治疗组(依诺昔酮或多巴酚丁胺)。主要终点为随机分组后3小时混合静脉血氧饱和度(SvO₂)的变化。结果显示,IABP组的SvO₂升高幅度更大。此外,IABP组的液体负平衡更显著,呼吸困难严重程度评分及N末端脑钠肽前体(NT-proBNP)水平下降更明显。但两组30天全因死亡率无差异。
该试验对预后相关终点的统计效力不足,且仅观察3小时SvO₂的变化可能对临床实践指导意义有限,因此无法为常规应用提供充分证据。
一项回顾性研究比较了IABP对心肌梗死相关心源性休克(CS)患者与急性失代偿性HF患者的血流动力学影响,进一步支持上述发现。结果显示:心肌梗死相关CS患者:心输出量几乎无改善(0.12±1.00 L/min);急性失代偿性HF患者:心输出量中度增加(0.58±0.79 L/min;p=0.0009)。两组基线血流动力学参数(除急性失代偿性HF组肺动脉压较高外)接近一致。此外,急性失代偿性HF患者的全身血管阻力下降,而MI相关CS患者则无此变化。尽管为回顾性设计,该研究仍强化了现有证据。
欧洲指南,未对失代偿性HF患者使用IABP提出明确推荐;
美国指南,建议将机械循环支持作为过渡治疗选择,但未特别提及IABP。
主动脉内球囊反搏(IABP)也被用于静脉-动脉体外膜肺氧合(VA-ECMO)治疗中辅助左心室(LV)减压。目前,尚无针对此适应症的随机对照试验,观察性研究结果亦存在矛盾。
部分研究(如心脏术后或心脏移植后的场景)显示,联合IABP治疗可显著降低死亡率;但另一些研究(尤其是针对心肌梗死相关心源性休克CS患者)发现,联合IABP并未改善生存率,甚至可能因联合使用VA-ECMO和IABP导致冠脉灌注受损。
一项纳入4576例接受ECMO治疗的CS患者的Meta分析显示,联合IABP与生存率改善相关(风险比0.90;95%置信区间0.85-0.95;p
一项针对非随机试验的Meta分析(研究不同LV减压方式对ECMO患者的影响)表明,采用减压策略的患者死亡率显著降低。但当前证据不足以明确IABP的应用价值,或是否需优先选择其他减压策略(如经皮心室辅助装置、直接LV引流等)。
目前尚无指南对VA-ECMO治疗中的LV减压策略提出具体建议。
IABP应用总结
IABP,到底是“救命神器”,还是已经“跌落神坛”?
由于IABP的适应症及潜在病理生理机制差异巨大,目前无法对其是否有效给出普适性结论。对大多数可能的IABP适应症而言,尚缺乏来自大样本随机对照试验的充分证据支持。
具体来说,
急性心肌梗死(AMI)伴或不伴休克,常规使用IABP无科学依据,对于无心源性休克(CS)的AMI患者,IABP甚至可能存在危害。若AMI合并机械并发症(如室间隔破裂、二尖瓣反流),国际指南一致建议考虑IABP,但支持证据仍不足。
高风险患者的冠状动脉旁路移植术(CABG),IABP可能作为潜在适应症,但需大样本随机试验验证以制定指南推荐。
急性失代偿性心力衰竭(HF)及VA-ECMO中的左心室(LV)减压,类似地,IABP的应用需进一步研究支持。
后续进一步研究方向,需评估IABP技术升级(如光学传感器优化同步性)的疗效,但目前尚无新的大规模随机研究开展,且IABP使用率持续下降。当前研究重点转向可能更有效的设备,如微轴左心室辅助装置和ECMO。尤其在IABP于其最受关注的适应症(心源性休克)中被证实无效后,新的其他设备的应用变得更广泛。
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫