
概述
心源性休克(CGS)是一种常见且发病率很高的疾病。根据国家住院患者样本,尽管重症监护实践和旨在恢复正常血流动力学的新型力学治疗有所改善,但每年仍有超过100000例病例,30天死亡率接近50%。这个问题旨在提高临床医生对CGS的理解,这篇综述特别关注潜在的病理生理学。我们研究了CGS的定义和病因、风险评估方法,以及作为概念化心室力学、心室血管相互作用和CGS中观察到的紊乱的基础的压力-容量环机制。本综述还将结合后续章节,讨论在特定情况下(即心肌梗死后、急性失代偿性慢性心力衰竭、心脏手术后)遇到的CGS的细微差别,阐述CGS的药理学和力学治疗,并以基于案例的形式对CGS进行综述。
关键词
心源性休克,发病机制,血流动力学,压力-容量分析
引言
失代偿性心力衰竭和心源性休克(CGS)的综合发病率正在上升,这为基于设备的治疗创造了一个新兴的市场,以满足对更有效治疗的需求。由于医疗指南无法跟上创新的步伐,临床医生只能依靠自己对不同患者血流动力学异常以及不同药物和设备的治疗效果的理解。然而,指导临床医生决策的CGS主要是心输出量减少的结果这一普遍概念现在被认为是不完整的。越来越多的证据要求对CGS有一个更细致的看法,即心室与全身或肺血管系统之间的复杂相互作用、左心室和右心室之间的相互依存关系,以及经常伴随CGS的分子和炎症环境。本文通过全面回顾CGS的定义、病因和先进的血流动力学原理,探讨了CGS的关键细节和病理生理学。
心源性休克的原理
定义
心源性休克和急性失代偿性心力衰竭(ADHF)的休克前状态代表了心血管疾病患者的一系列血流动力学不足。ADHF和CGS都描述了心输出量不足以提供足够的组织灌注或虽然足够但需要的代偿性血流动力学变化的状态是有害和无法持续的。失代偿性心力衰竭有四种不同的表型,它们根据容量状态(容量不足与容量超负荷)和心输出量的充足性(充足与不足)进行分类。显著的人与人之间的变异性限制了高心输出量与低心输出量的分类,但这一事实强调了临床、物理和血流动力学检查在诊断和管理CGS中的重要性。尽管缺乏证据支持在大多数ADHF患者中使用肺动脉导管,但肺动脉导管可以通过提供定量测量来评估血流动力学参数和治疗反应的相对变化,从而帮助临床医生管理CGS危重患者。因此,我们提倡在难治性CGS患者中使用肺动脉导管,特别是对于那些需要机械循环支持的患者。
心源性休克也在许多临床和研究环境中得到了定义,这些环境补充了上述实用定义(图1)。两个主要的研究定义是从两个试验中演变而来的——SHOCK(我们是否应该为心源性休克紧急重建血管闭塞的冠状动脉血运)和IABP-SHOCK II(心源性休克中的主动脉内球囊泵II)——这两个试验评估了急性心肌梗死(AMI)背景下的CGS。SHOCK和IABP-SHOCK II定义的共同标准如下:(1)收缩压和(2)末端器官灌注不足的证据,定义为四肢凉爽、精神状态改变、尿量2.0毫摩尔/升。IABP-SHOCK II定义没有纳入任何血流动力学参数,避开了肺动脉导管衍生的数据,并且包含了胸部放射学上肺水肿的存在,作为肺毛细血管楔压升高(PCWP)的替代指标。相反,SHOCK试验纳入了心脏指数(CI)≤2.2 L/min/m2和PCWP≥15 mm Hg等参数,尽管并非所有参与研究的患者都必须使用肺动脉导管。
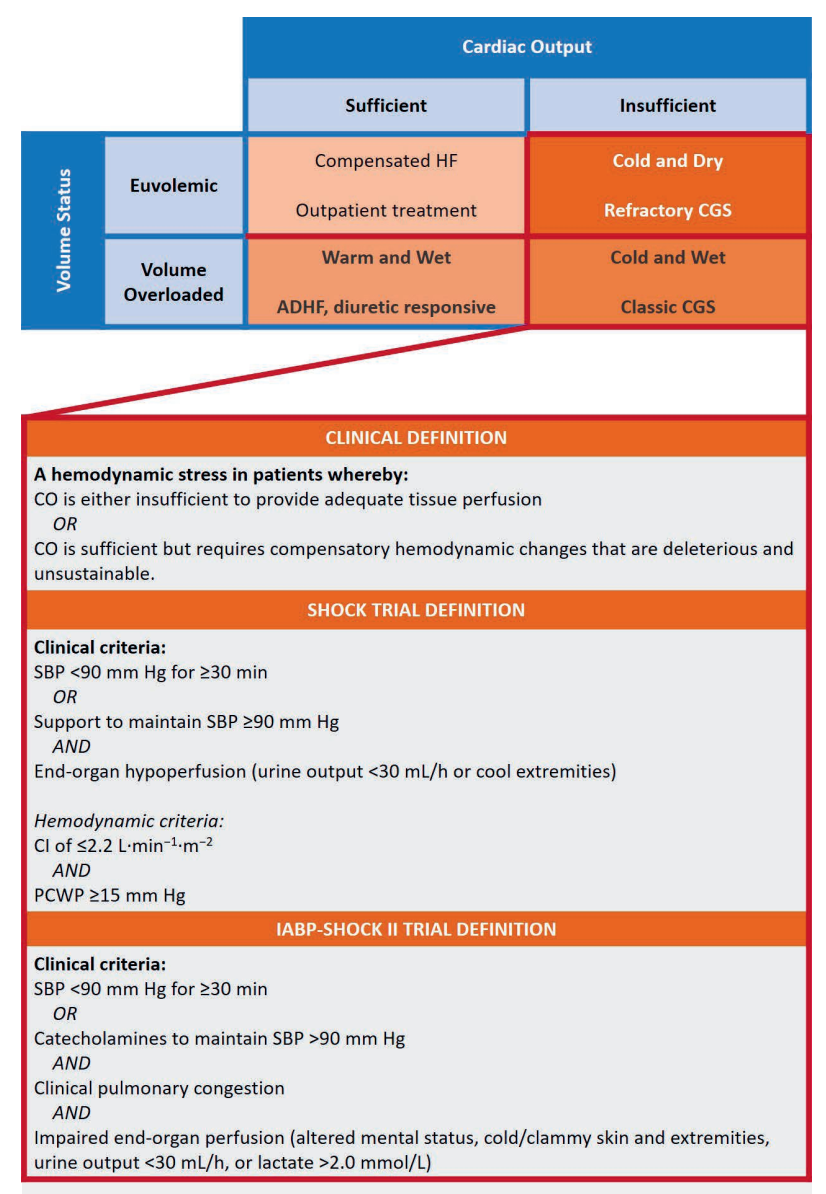
图1 :根据容量状态和心输出量概念化急性失代偿性心力衰竭的Stevenson模型,以及SHOCK和IABP-SHOCK II试验中心源性休克的定义。
最近,冠状动脉造影与介入学会(SCAI)发布了一份共识文件,其中包含CGS的定义和分级CGS程度的分类方案,作为临床和研究目的的风险分层步骤(图2)。该模式将患者分为五个阶段:CGS的“有风险”(阶段A);在CGS的“开始阶段”(阶段B);表现为“经典”CGS(C阶段);CGS“恶化”,需要第二种正性肌力药或机械循环支持(D阶段);以及血流动力学对先前治疗无效的“临终”患者(E期)。无论患者的CGS分期如何,心脏骤停都是影响预后的重要因素。该模式创建了一个分类法,承认患者存在不同程度的临床和血流动力学损害,并且处于不同阶段的患者可能受益于也可能不受益于不同形式的治疗。它还允许在更晚期进行积极的也可能是徒劳的治疗。
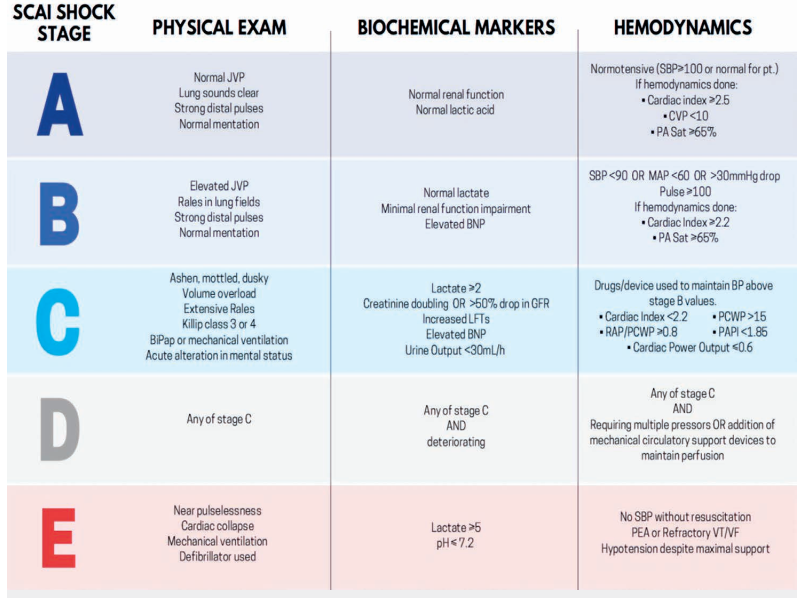
图2 :最近发布的冠状动脉造影和介入学会对心源性休克患者进行分类的方案。 JVP:颈静脉压;SBP:收缩压;CVP:中心静脉压;PA Sat:肺动脉血氧饱和度;BNP:脑钠肽;RAP:右心房压;PCWP:肺毛细血管楔压;PAPI:肺动脉搏动指数;PEA:无脉冲电活动;VT/VF:室性心动过速/心室颤动。
风险评估和预测
预后可以通过各种易于计算的风险评分来估计,这些评分可以深入了解CGS的病理生理学。最近调查的两个分数是IABP-SHOCK和CardShock分数。IABP-SHOCK评分使用六个变量估计30天死亡率:年龄>73岁,中风病史,入院时血清乳酸≥5 mmol/L,血清肌酐≥1.5 mg/dL,血糖≥191 mg/dL,经皮冠状动脉介入治疗后心肌梗死溶栓(TIMI)评分75岁,左心室射血分数≤40%,血清乳酸水平(0分4 mmol/L),估计肾小球滤过率(0分>60 mL/min/1.73 m2,1分=30-60 mL/min/1.76 m2,2分
病因学
多种过程可导致ADHF和CGS。急性心肌梗死并发心源性休克占CGS病例的近80%,可能由ST段抬高型心肌梗死和非ST段抬高性心肌梗死引起。尽管在治疗和血运重建方面取得了进展,但CGS仍然是MI的致命并发症,不同队列的死亡率从38%到65%不等。在当今血运重建时代,室间隔、游离壁或乳头肌破裂等机械并发症很少发生,心肌梗死后低血压和休克更常见的原因是心输出量减少(由于心肌收缩力丧失)或炎性细胞因子(如TNF-α和一氧化氮)引发的严重血管舒张。
CGS的非冠状动脉原因是原发性心肌、瓣膜、电学或心包异常的结果。CGS的各种原因的患病率估计如下:慢性心力衰竭的进展(11-30%)、瓣膜和其他机械原因(6%)、应激诱发/Takotsubo心肌病(2%)和急性心肌炎(2%)。进展为ADHF并最终发生CGS的慢性心力衰竭患者可能与急性冠状动脉综合征相关的CGS患者不同。在这些环境中观察到的肾素-血管紧张素-醛固酮轴的慢性上调和循环儿茶酚胺的增加诱导血管收缩和心室重塑,在CGS出现时产生不同表型的底物。事实上,急性心肌梗死中CGS患者的预后与慢性心力衰竭患者的预后不同。
心血管血流动力学基础
不管CGS的根本原因是什么,其病理生理学、血液动力学和心肌能量学都可以通过心室压力-容量图(PV)很容易地解释。这一结构也有助于更好地理解药物和基于设备的治疗对血流动力学和心肌能量学的影响。PV环描述了单个心动周期内发生的事件,并提供了一个框架来直观地表示失代偿性心力衰竭和CGS的紊乱(图3A)。在正常情况下,PV环大致呈梯形,顶部为圆形。环的四个边表示心动周期的四个阶段:(1) 等容收缩期、(2)射血期、(3)等容舒张期和(4)充盈期。环的宽度表示每搏量,而环的高度表示收缩压。
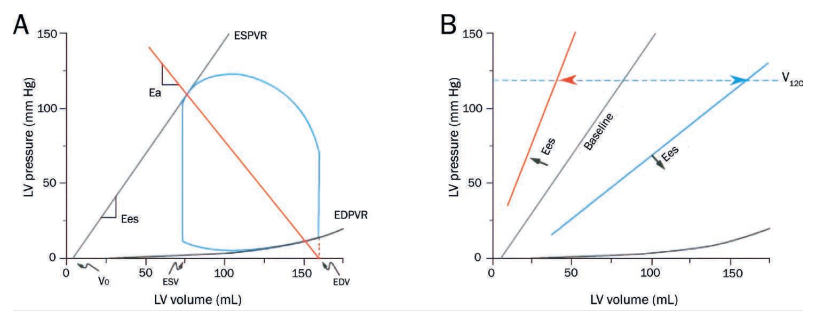
图3 :(A) 正常压力-容量环由收缩压-容量关系(ESPVR)和舒张压-容量关系(EDPVR)界定。ESPVR与斜率Ees和体积轴截距Vo近似线性。有效动脉弹性(Ea)是从容量轴上的舒张末期容积(EDV)点延伸到环的收缩末期压力容量点的线的斜率。(B) ESPVR随着心室收缩力的变化而变化,这可能是Ees和Vo变化的组合。收缩力的变化可以通过V120来指示,V120是ESPVR与120mm Hg相交的容量。
该环位于收缩末期压力-容量关系(ESPVR)和舒张末期压力-容量关系(EDPVR)的边界内。ESPVR对收缩末期压力和容量(分别为Pes和Ves)之间的关系进行建模,并与斜率Ees和体积轴截距Vo(Pes=Ees[Ves-Vo])呈合理线性。Vo是在观察到心室压力升高之前填充心室所需的血液容量(即未受应力容量)。ESPVR的偏移随着心室收缩力的变化而发生(图3B)。收缩力的增加与ESPVR的向上/向左移动有关,理想情况下会导致Ees的增加和Vo的微小变化。因此,Ees被认为是心室收缩力的一个与负荷无关的指标。
EDPVR代表了松弛的程度,并指示了当所有肌动蛋白-肌球蛋白键解偶联且肌细胞完全松弛时的被动心室特性。EDPVR是非线性的,可以用P=β(eα(V-Vo)-1)或P=βVα等方程来描述,其中常数α和β与心室和细胞外基质的机械性能和结构特征有关。EDPVR的移位可发生在病理状态下,如限制性心肌病、肥厚性心肌病和浸润性疾病(向左移位表示舒张功能障碍)或所有形式的扩张型心肌病(向右移位表示重塑)。
有效动脉弹性(Ea)是连接容积轴上舒张末期容积与PV环收缩末期压力容量点的线的斜率(图3A)。Ea与总外周阻力(TPR)和心率(HR)有关:Ea≈TPR×HR。ESPVR和Ea线之间的交点决定了心室和脉管系统中的压力、流量和每搏量之间的平衡点。这种将心室与脉管系统连接起来的概念,被称为心室-血管耦合,是描述每搏量、平均动脉压(MAP)和其他关键心血管参数如何由前负荷、后负荷、收缩性和HR确定的科学基础。
除了提供一个解释心室力学的平台外,PV环图还可以作为理解心肌耗氧量决定因素的一个概念图(MVO2,图4)。循环内的面积是每搏功,估计为每搏量和MAP的乘积。心输出量(CPO)是每搏功和HR的乘积,已被用作CGS严重程度的指标,与住院死亡率呈负相关。CPO的改善也被用于量化CGS疗法的有效性。每搏MVO2与心室压力-容量面积(PVA)呈线性相关;PVA是外部每搏功(SW,PV环内的面积)和势能(PE)的总和(图4)。PE是由ESPVR、EDPVR和PV环的舒张部分限定的区域。它表示在收缩末期储存在肌丝中的未转化为外部功的残余能量。每次搏动的总MVO2包括支持基础代谢所需的氧气、每次搏动的钙循环以及每次搏动期间的肌动蛋白-肌球蛋白解偶联(图4B)。当收缩力增加时,MVO2-PVA线的斜率不变,但截距增加;这是因为收缩性的增加通常是由于钙循环的增加。相反,当收缩性降低时,MVO2-PVA线的截距降低,斜率不变。HR的变化不会显著影响每搏PVA和MVO2之间的关系(图4C)。然而,每分钟MVO2(通过将每搏MVO2乘以HR获得)和PVA之间的关系受到HR的高度影响(图4D)。
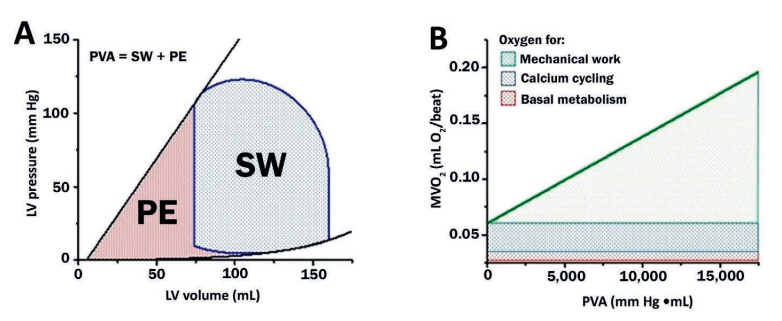
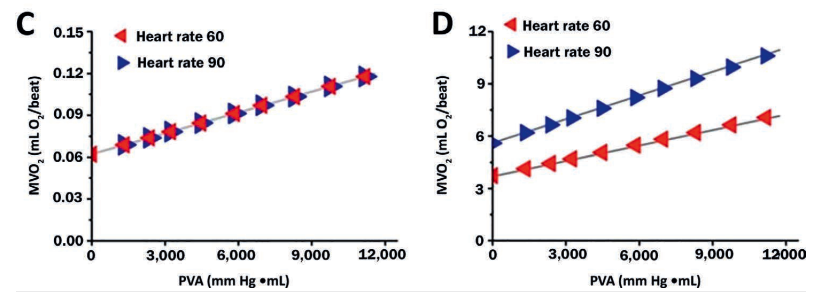
图4 :(A) 压力-容量面积(PVA)是每搏功(SW,PV环内的面积)和势能(PE,收缩压-容量关系和舒张压-容量之间的关系所限定的面积)的总和。(B) 心肌耗氧量(MVO2)与PVA呈线性相关,可分为3个主要成分。(C) 心率对PVA和MVO2之间的逐搏关系的影响最小,(D) 但是当考虑PVA和每分钟MVO2之间的关系时,这些小的差异被放大了。
心源性休克与压力-容量环
PV环特别有助于描述失代偿性心力衰竭的病理生理学(图5A)。例如,在MI发生后不久,ESPVR向下和向右移动,表明心室收缩力突然降低(图5B)。这种下降伴随着血压(以PV环的高度为指标)、SV和心输出量的显著下降,同时左心室舒张末期压和PCWP也可能出现小幅升高。
对心室收缩力降低(神经激素激活)的第一阶段代偿反应试图维持MAP(图5C)。当大血管中的压力感受器识别MAP的减少,并(1)激活指向心脏和血管结构的传出自主神经纤维,以及(2)刺激肾上腺释放儿茶酚胺时,该过程开始。心率和收缩性在较小程度上因自主神经张力增强而增加,而TPR则因儿茶酚胺诱导的血管收缩而增加。这些因素也会导致静脉收缩,使血液从内脏循环中未受压力的高容量储器功能性地转移到低容量血管。这增加了功能性循环血容量,并提高了中心静脉和肺静脉压力。总的来说,这些影响会增加血压,但代价是导致PV环进一步向右移动,向更高的舒张末期容积和压力移动。
代偿反应的下一阶段取决于是否存在伴随的炎症过程。炎性细胞因子也能降低TPR,抵消上述许多神经激素紊乱(图5D)。因此,CGS对PV环的净影响(基于患有严重MI的患者)是ESPVR更平坦,PV环更窄、更短并向右移动。这些发现解释了MI后CGS的临床表现,患者收缩力降低,SV较小,BP较低,左心室(LV)舒张末期容积升高。TPR可能正常、升高或降低,这取决于自主神经介导的血管收缩和炎症介导的舒张之间的平衡。
随着时间的推移,这些机制驱动心室重构。这反过来又使EDPVR向更大的容量转移,因为存活的肌细胞肥大(伸长和加宽)和细胞外基质转运增加,从而允许肌细胞重组(图5E)。EDPVR移位也导致伴随的ESPVR向右移位,进一步恶化左心室功能。只要启动重塑的条件通过药物或机械干预持续不减,重塑的过程就是渐进的。
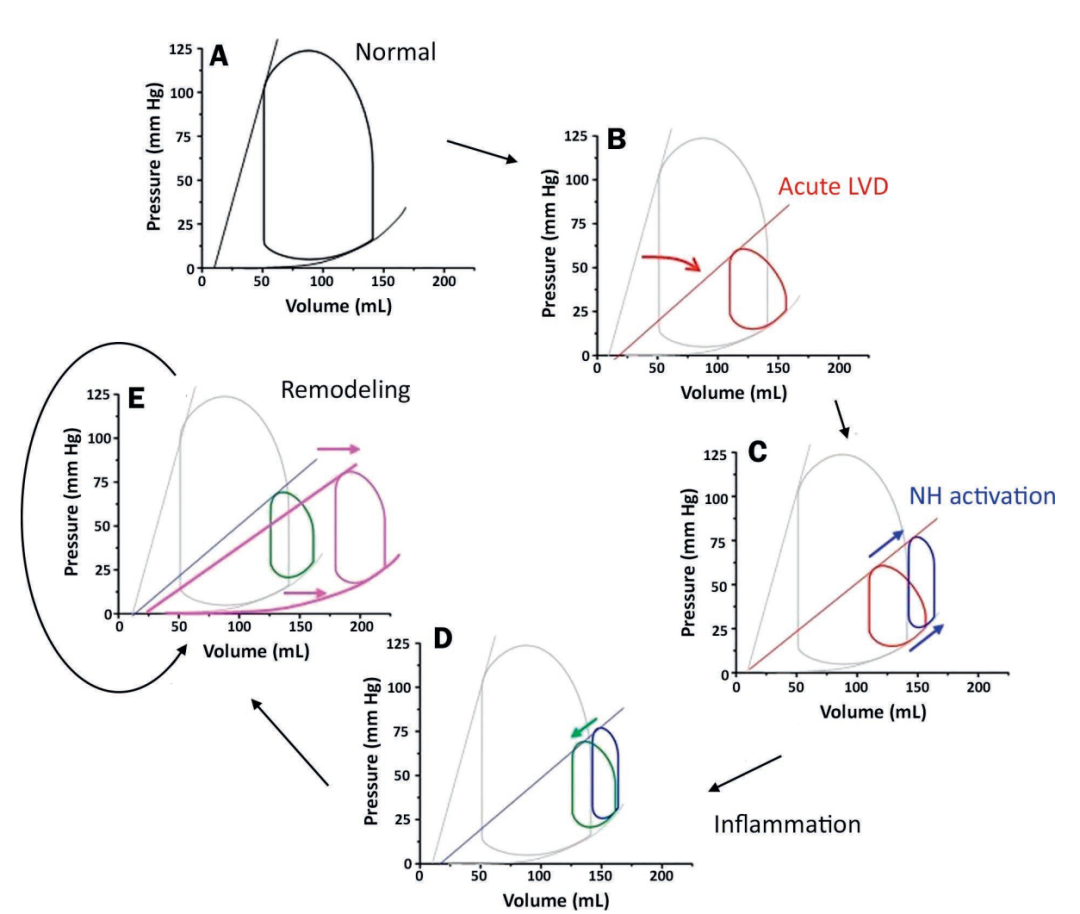
图5 :心源性休克的病理生理学表现为压力-容量(PV)循环。(A) 正常PV环;(B) PV环反映急性心肌梗死后的变化(红色);(C) 收缩力下降引起的自主反应引起的变化(蓝色);(D) 炎症介质释放引起的变化(绿色);(E) PV环反映了心脏重塑的表现(粉红色),收缩末期和舒张末期的压力-容量关系都发生了变化。
右心室功能与心源性休克
右心室(RV)功能障碍可在三个关键方面对CGS的生理学产生影响:(1)在没有LV功能障碍的情况下,如右冠状动脉近端阻塞引起的RV梗死;(2) 在PCWP和/或肺血管阻力增加的情况下引起肺血管后负荷增加;和(3)在原发性左心室功能障碍的情况下,室间隔对右心室功能的影响减少。当RV功能障碍使左心室功能障碍复杂化时,临床医生需要考虑支持RV,使左心室有足够的前负荷来维持足够的心输出量。右心室功能障碍是死亡率的有力预测指标,突出了它在CGS中的关键作用。
右心室功能障碍也可以使用PV环框架来描述,但正常的RV PV环与LV PV环在许多重要方面存在不同(图6)。首先,RV有自己的ESPVR和EDPVR,为环提供边界。重要的是,RV ESPVR(Ees)的斜率通常是LV的五分之一到七分之一。然而,EDPVR相似,因为两个腔室的大小相似。其次,RV PV环没有表现出显著的等容期,因为舒张压几乎可以衰减到RV舒张末期压。第三,RV PV环具有更圆顶形状的顶部,并且环的左上部区域不形成尖角。随着CGS的RV功能障碍,RV PV环开始类似于CGS中的LV PV环,向右移动并变得越来越窄。
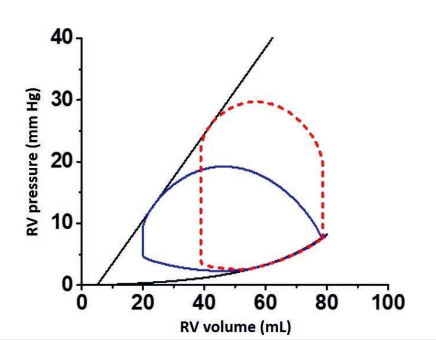
图6 :正常右心室(RV)压力-容量(PV)环(蓝色实线)与正常左心室(LV)PV环(红色虚线)相比。RV收缩末期压力-容量关系的斜率较浅,收缩压小于LV PV环中的收缩压。右心室和左心室舒张末期压力-容量关系相似。
总结
心源性休克是一种复杂的异质性疾病,其特征是心输出量不足或为帮助恢复正常心输出量而进行的代偿调整是有害的。谨慎的临床评估,通过详细的体检和肺动脉导管来评估心内充盈压力,对于促进风险分层和指导这一弱势人群的治疗选择和优化至关重要。评估也有助于根据CGS的程度对患者按照SCAI ABCDE分类法进行分类。此外,尽管在没有有创性测试的情况下无法在临床实践中评估PV环,但临床医生和研究人员可以参考PV环框架作为一种补充工具,以了解CGS背后的生理紊乱,并确定哪些血流动力学参数(即收缩性、舒张性、前负荷和后负荷)可以作为解决CGS的目标。
KEY POINTS
1、心源性休克(CGS)是指心输出量不足以满足末端器官灌注要求的一种力学状态。当通过激活有害和不可持续的代偿机制在短期内满足灌注要求时,也可能发生这种情况。
2、尽管急性心肌梗死是CGS最常见的原因,但越来越多的CGS病例归因于慢性心力衰竭的急性失代偿。
3、CGS患者的风险分层至关重要。CardShock和IABP-SHOCK II评分是根据冠状动脉造影和介入学会的心源性休克分期对患者进行分类的有用辅助指标。
4、正常压力容量在逐搏的基础上直观地描述了心室力学和心室-血管的相互作用。该循环由两条基本曲线围绕——收缩末期压力-容量关系和舒张末期压力-容量关系——这两条曲线代表了收缩性、舒张性、前负荷和后负荷等特性。
5、无论病因如何,CGS过程中的压力-容量还在正常情况下都会变窄并相对于回路向下和向右移动,反映出每搏量和收缩力的下降以及左心室舒张末期容量的增加。
原文地址:
Methodist Debakey Cardiovasc J. 2020 Jan-Mar;16(1):7-15. Doi: 10.14797/mdcj-16-1-7.
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫 



![[JAMA述评] 迈向个体化治疗:评估随机临床试验中疗效的异质性](https://www.icu.cn/wp-content/uploads/2023/05/2023-05-09_112937-480x300.gif)
