第二百四十四期 2
本期文献回顾
李媛
中国医学科学院阜外医院
王赫
中国医学科学院阜外医院
VA ECMO中左室减压:适用人群、使用时机以及具体实施策略
Unloading the Left Ventricle in Venoarterial ECMO: In Whom, When, and How?
Saad M. Ezad, et al. Circulation. April 18, 2023. DOI: 10.1161/CIRCULATIONAHA.122.062371.

研究背景
VA-ECMO可为心源性休克患者提供心肺支持,但是在外周置管的VA-ECMO中(图1),血液在主动脉逆流,这将增加左室的后负荷,从而引起左室扩张、冠脉灌注及每搏量的减低,并可能进一步导致心脏血栓、心律失常和肺水肿(图2)等并发症的发生。可以通过使用额外的循环辅助装置来进行心脏减压,以减轻后负荷过高带来的不利影响,但关于这些装置的使用缺乏明确的证据,并且这些装置本身可能也会产生不良影响,因此需要综合考虑使用这些装置的获益以及与其相关的并发症。
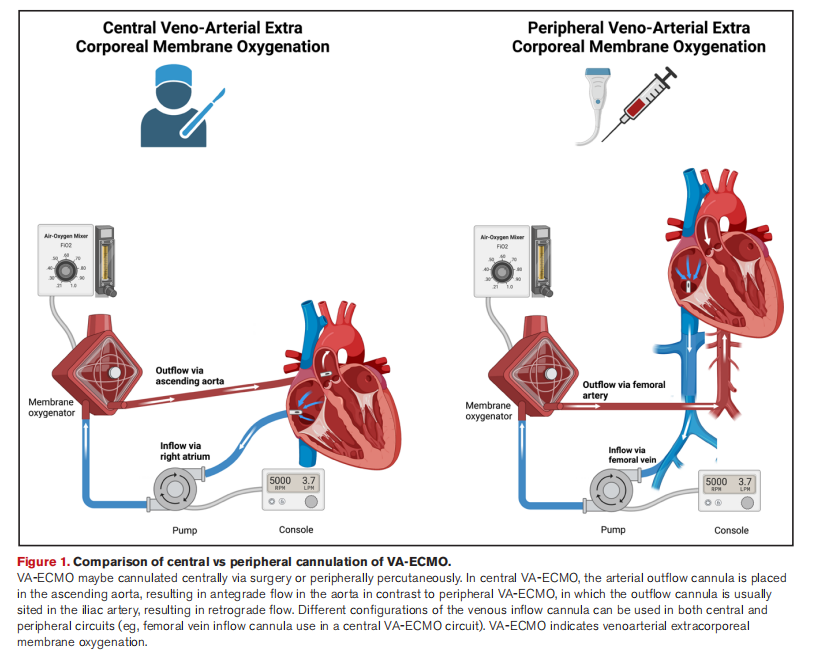
图1 VA-ECMO中心插管与外周插管比较
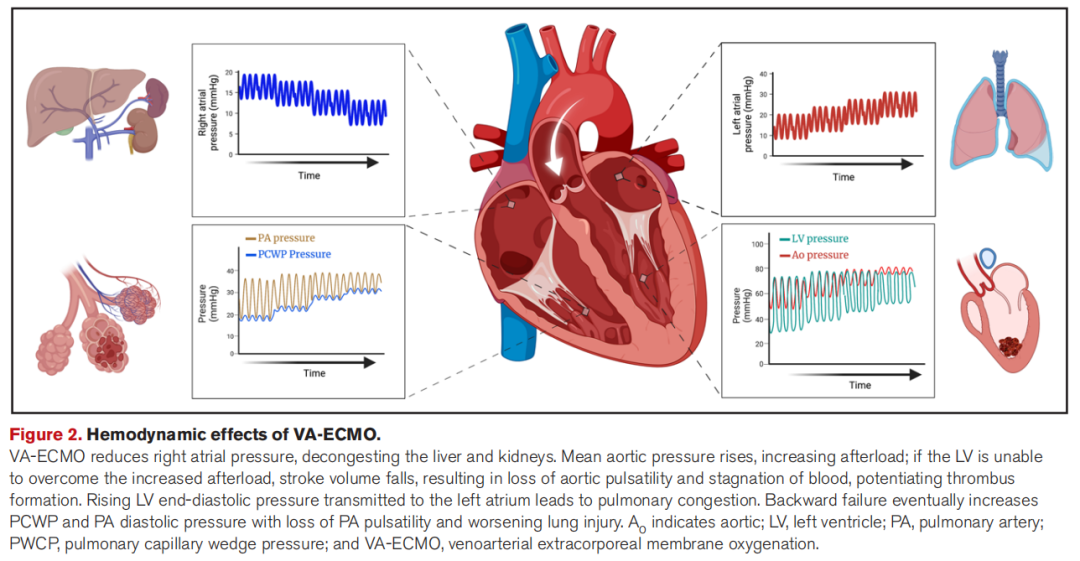
图2 VA-ECMO血流动力学影响
左室减压的生理学基础
左心室后负荷是收缩期施加在心肌上的机械负荷的间接体现。心脏机械负荷也可以称之为心室壁应力,左室壁负荷是整个心动周期的连续测量值,与左心室腔内压成正比,与心室壁厚度成反比。连续的左心室腔内压力和体积读数可用于生成左心室压力-体积 (PV) 环,可以通过动脉弹性等指标来评估后负荷。收缩末期的心室收缩压与每搏输出量的比值等于动脉弹性,可以反映动脉的负荷(图3A)。动脉负荷与心脏后负荷密切相关,如果动脉负荷增加,即使心肌收缩力和舒张末期容积(EDV)保持不变,其也会通过减少每搏输出量从而降低心输出量(图3C)。
在病理情况下,后负荷显著增加常伴有静脉淤血和较高的前负荷。较高的前负荷可能会增加左室舒张末容积(LVEDV),根据Frank-Starling机制,每搏输出量也会增加(图3D),这称之为前负荷储备,收缩力增加是左室维持每搏输出量的一种代偿机制,但它是以增加PV环的面积增大和增加心肌耗氧量为代价的,这可能会对心肌恢复产生潜在的不利影响。在心源性休克期间,左心室通常缺乏前负荷和收缩储备以克服与VA-ECMO相关的后负荷增加,这将会增加心肌耗氧量。
左室减压的目的是减少PV面积,从而减少心肌耗氧量(图3B)。最近有证据表明,左室减压还有可能减少炎性细胞因子表达。在急性心肌梗死的猪的模型中,左心减压减少了梗死面积,基因组研究确定了基因表达层面的心脏保护机制,因其保持了线粒体的完整性。
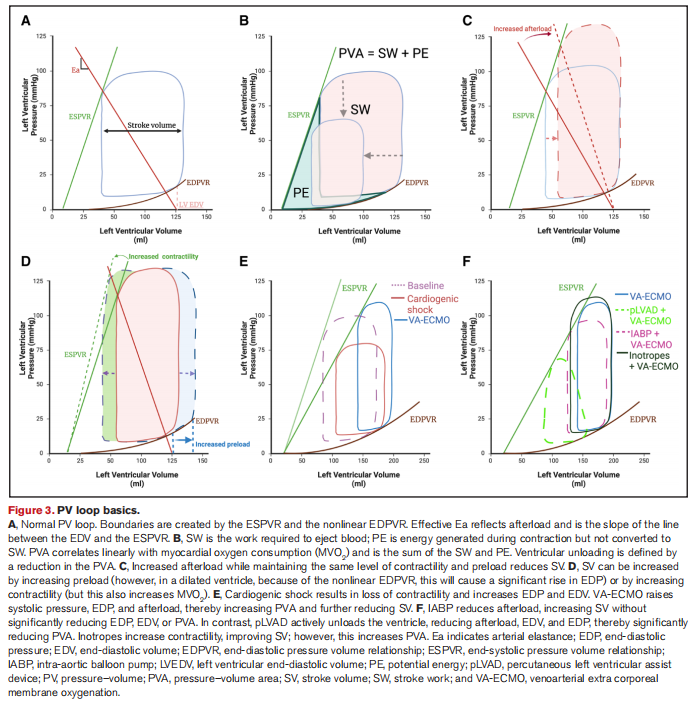
图3 PV环基础知识
适用人群
左室后负荷所导致的并发症持续进展是进行左室减压的相对明确的指征(表1)。但是如果没有明确的并发症,我们就需要平衡使用左室减压装置所带来的获益及风险,因为其有可能会导致严重的出血、血管并发症以及凝血功能紊乱。是否使用左室减压装置以及其使用的时机和使用何种装置,是由病人个体化的治疗目标来决定的。血流动力学、超声心动图和临床特征可能有助于识别有发生并发症风险的患者。
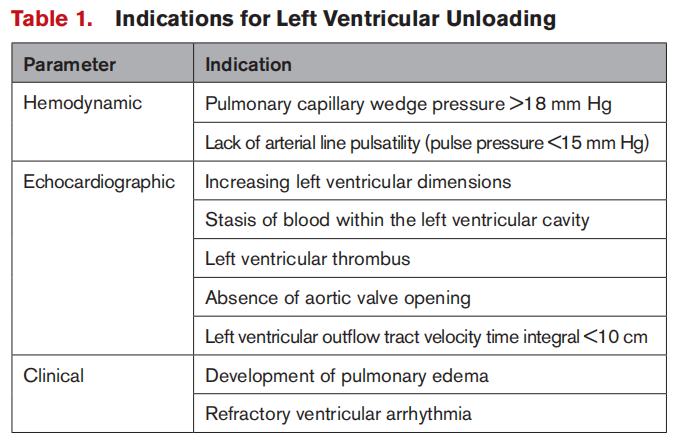
表1 LV减压指征
血流动力学预测指标
动脉搏动减弱是VA-ECMO患者后负荷增加的指标,脉压<15 mm Hg与自体心输出量<1 L/min密切相关,脉压<20 mm Hg与患者生存率的降低有关。
左室舒张末压(LVEDP)也可以作为一项预测指标,通常通过测量肺毛细血管楔压(PCWP)来估计其数值的大小。在使用VA-ECMO之前PCWP就较高的病人因为其前负荷储备已耗竭,这就使其不易耐受增加的后负荷。如果在VA-ECMO启动时PCWP>15mmHg提示可以使用IABP进行左室减压,但是也有人建议阈值为18mm Hg.使用左室减压装置时LVEDP为 12-18 mmHg提示充分的左室卸负荷。左右室的相互作用是一个重要的考虑因素,特别是对于右心室功能保留的患者,由于肺血流量增加会导致左心室充盈压升高,因此并发症发生的风险也会随之增加。
超声心动图预测指标
经胸超声心动图可以对左室的形状及功能状态进行无创的监测,并且建议进行连续评估。在超声心动图评估有限的情况下,重点评估主动脉瓣开放情况和左心室流出道 (LVOT) 速度时间积分可提供最客观的指标。经胸超声心动图成像窗有限的患者可考虑经食管超声心动图。
在实施 VA-ECMO 之前测得的左心室射血分数可预测后负荷敏感性:较低的左心室射血分数与 PCWP 增加和每搏输出量减少有关。左室形状与后负荷和收缩力有较强的相关性,尽管ECMO流速固定,但发现左室增大时可以考虑进行左室减压。左室流出道速度时间积分可用于估计每搏输出量和心输出量;左室流出道速度时间积分<10 cm 反映了自体心输出量不足,从而预测 VA-ECMO 撤机失败以及对后负荷增加的敏感性。
超声心动图也可用于检测血液淤滞、左心室血栓或主动脉瓣开放不全等并发症。不断加重的二尖瓣关闭不全可能反映左心室压力升高,是发生肺水肿的早期标志。
临床预测指标
对于合并心肌梗死的休克病人,左心室压升高会导致心内膜下灌注减少,从而加剧心肌缺血并进一步损害心室功能。一项针对 62 项研究(共 7581 名患者)的荟萃分析数据显示,当休克继发于急性心梗时进行左室减压可以达到最大死亡率获益,并可使其风险降低 6.65%。
慢性心力衰竭患者通常在基线PCWP升高,使其更容易受到后负荷增加的影响,因为他们的前负荷储备即将耗尽。在慢性心衰急性发作引起的休克中使用IABP可显着降低全身血管阻力,并将心输出量增加 23%,而在急性心梗患者中增加10%。由于这类病人易受后负荷增加的影响,预防性减压可能是有益的,通过减轻后负荷和减少肺水肿的发生率可明显改善心输出量。
减压方式
每种方法都有自己的禁忌症、风险、成本和潜在优势。
非侵入性和药物方法
在考虑侵入性左心室减压策略之前,应尽力采用保守措施减少前后负荷。VA-ECMO的流量应足够提供全身灌注,同时最小化后负荷,较低的流量(
左心引流
导管
经皮导管可插入LV腔、左心房或肺动脉,并连接到VA-ECMO回路的引流导管。使用经食管超声引导的猪尾形导管(7F)插入LV,可实现经主动脉减压,减小LV尺寸和容积。报道显示减小LV尺寸会增加平均动脉压和脉压。但是,经皮导管的尺寸限制了最大流量,因为存在更高的溶血风险,因此不建议常规使用这种方法。
左心减压
经皮房间隔造口术
经皮房间隔造口术是一种在透视或经食管超声引导下进行的手术,用于缓解左心房压力降低、左室扩张和肺水肿等症状。但是,这种手术可能会左室射血不足和潜在的LV或主动脉根部血栓的风险,因为没有经过主动脉瓣的前向流动。同时,残余的房间隔缺损可能会增加撤除静脉导管后中风的风险。左心房VA-ECMO则可以通过经房间隔穿刺将多级静脉引流导管置于左心房内,从而对右心室和左心室进行减压,并显示降低PCWP。这种方法可能特别适用于具有左室血栓或单侧周围血管疾病的患者,在这些患者中,一般无法进行第二次大口径股动脉入路操作。另一种实现左心房引流的方法是使用TandemHeart,该方法是一种基于离心泵的系统,使用21F经房间隔穿刺放置的导管位于左心房,流出管路位于股动脉。
肺动脉引流
将ECMO的引流导管置入肺动脉中可以通过减少前负荷间接降低左心室压力和容积。单级或多级导管可以用于此目的。ProTek Duo(CardiacAssist Inc,美国)是一种双腔导管,当两个腔道被拼接在一起开口作为引流口时,也可用于同时引流右心房和肺动脉。ProTek Duo有29F或31F导管尺寸可用,经颈静脉插入,使流量可达4.5升。它通常用作右心室支持的右心房到肺动脉旁路管路
主动脉球囊反搏
主动脉球囊反搏(IABP)是最常用的左心室减负辅助心脏机械支持设备。IABP放置在降主动脉的标准位置,通过舒张期膨胀降低左心室射血时的后负荷,促进经主动脉瓣的前向流,收缩期缩小,增加冠状动脉血流。与pLVAD相比,IABP提供的减压量较少。使用IABP可以改善心源性休克患者的脑血流。目前没有随机数据支持使用IABP进行减压,观察性研究数据存在争议。在AMI休克期间,使用IABP减压可以改善短期死亡率,但会增加严重出血的风险。涉及术后休克患者的荟萃分析发现,使用VA-ECMO和IABP的联合治疗与仅使用VA-ECMO相比死亡率类似。涉及4653名患者的更大规模的荟萃分析发现,在AMI休克亚组中使用IABP的死亡率较低。这些结果表明IABP的作用因休克病因不同而异,在缺血患者中可以获得额外的益处。需要更强有力的随机研究来证实这一点。
经皮左心室辅助装置(pLVAD)
pLVAD是一种经瓣膜微型轴流泵,可以将血液从左室中排出到主动脉根部,从而降低搏动功和PVA,减少MVO2。Impella CP是用于LV减压的常见设备,与ECMO流出导管组合使用,称为ECMELLA或ECPELLA。通常通过对侧股动脉经皮插入到ECMO流出导管中插入pLVAD,但也可以考虑通过腋动脉的外科植入和经皮跨心腔植入。pLVAD使用的禁忌症包括主动脉瓣机械瓣置换、严重主动脉瓣反流、LV血栓和外周血管疾病。Impella CP设备需要大口径动脉通路(14F)和直接通过设备管路应用的抗凝剂。ECPELLA可以降低PCWP、改善肺血流和降低LV尺寸,但需要考虑出血和肢体缺血的风险。一项包括510个倾向性评分匹配的患者的登记注册研究发现,与单独使用VA-ECMO相比,ECPELLA在30天内死亡率降低了21%,尽管出现了严重出血(分别为38.4%和17.9%)和溶血(分别为33.6%和22.4%)。平衡VA-ECMO管路和pLVAD设备的流量,以实现全身灌注和左心减压非常重要。对于伴有低氧血症的呼吸衰竭患者,需要注意高pLVAD流量可能会导致未氧合的血液进入系统和造成“小丑综合征”或“南北综合征”的现象。在这种情况下,最好将pLVAD流量设置为较低水平,直到呼吸功能得到改善,允许调整pLVAD和减少ECMO流量。同样的现象也常常伴随着左室恢复和持续性肺水肿。为确保足够的LV前负荷,还需要仔细地平衡pLVAD的入口压力,以防增加溶血的风险的情况。
Impella设备的一个大口径型号(Impella 5.5)可以提供高达6L/min的顺向流量,足以支持大多数情况下的独立全身灌注。该设备通过腋动脉进行外科手术植入,可以长时间留置(例如,已报道的持续时间长达83天)。这一发展具有潜在优势,可以使患者行走并减少溶血和血栓形成,因此在ECMO拔管后作为移植或长期LVAD植入的潜在桥梁。
外科方式
在心脏手术后休克或心脏移植后移植物功能衰竭时,常采用中心VA-ECMO治疗。虽然经升主动脉插管避免了外周VA-ECMO所伴随的逆行血流,但仍可能发生心室扩张和通过LVOT和主动脉根部的前向血流流量降低,加剧心肌下端灌注和心室功能损伤。因此,一些中心常规对所有接受外周或中心VA-ECMO治疗的心脏外科术后患者行左心减压,一项对2324名患者的荟萃分析发现死亡率降低的风险比(RR)为0.93(95% CI,0.85-1.01;P = 0.09),但ECMO脱机率显著增加。
将植入在LV心尖、肺静脉或肺动脉位置的手术排气导管通过Y型连接器插入到VA-ECMO回流管路中的静脉引流端肢体,可提供有效的双心室减压,但这些方法的结果数据有限:一项回顾性研究比较了23名接受外科减压和22名接受pLVAD治疗的患者,发现两组30天死亡率相似。
减压策略的选择
每种减压策略的作用机制可能是不同的,需要根据患者具体情况选择。HERACLES 试验将是首个比较减压策略的随机试验。虽然急需随机数据以对减压方法的选择做出明确的建议,但当前的决策应该以实用为主,基于特定的多学科团队根据的本中心专业知识和策略确定(见图4)。
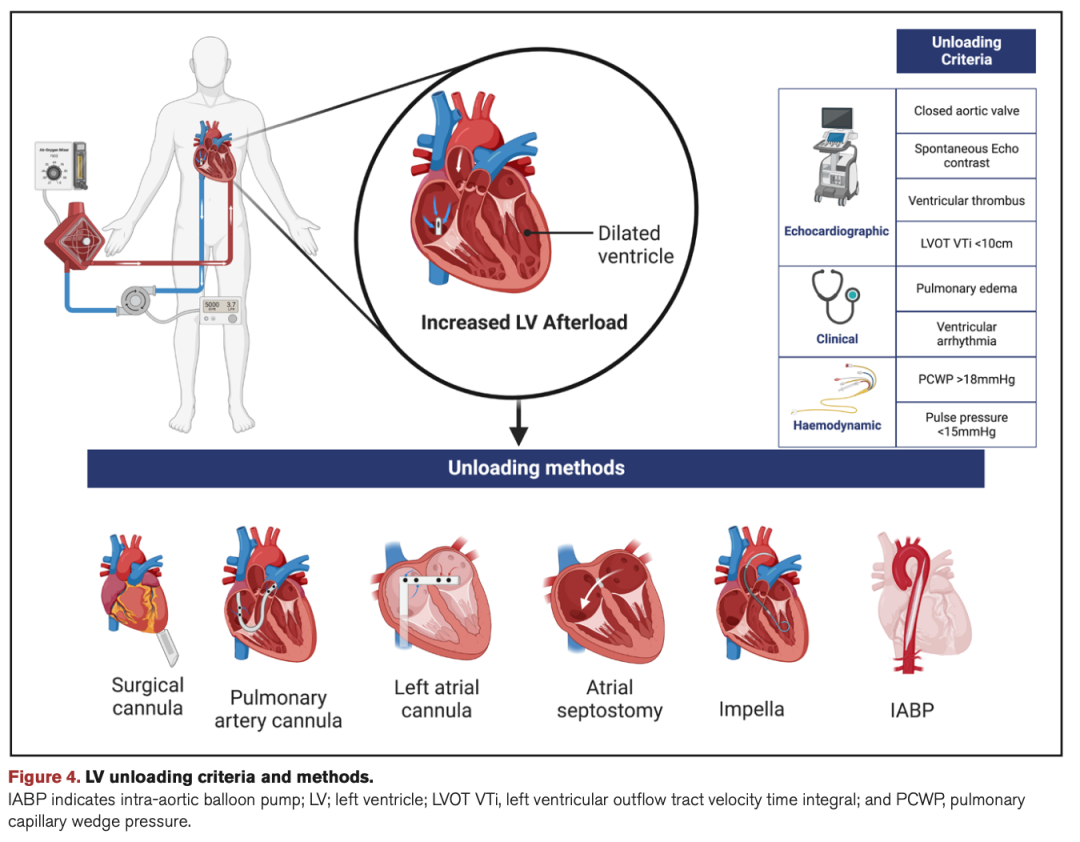
图4 LV减压指征与方式
减压时机
减压装置可以在VA-ECMO启动之前、同时或之后植入。这种预防性方法可以帮助保护脆弱的心室,并通过避免暴露于增加的后负荷来促进心肌康复,这应该与增加的并发症和成本的潜在风险相权衡。另一方面,如果仅在发现增加的后负荷的不良血流动力学、临床或超声心动图表现时才采取减压,可以减少减压装置本身的并发症风险,但可能会影响心肌康复。
虽然目前的数据表明,在VA-ECMO启动后最多2小时进行预防性减压似乎是有益的,但需要进行随机试验以确定治疗的有效性(表2)。
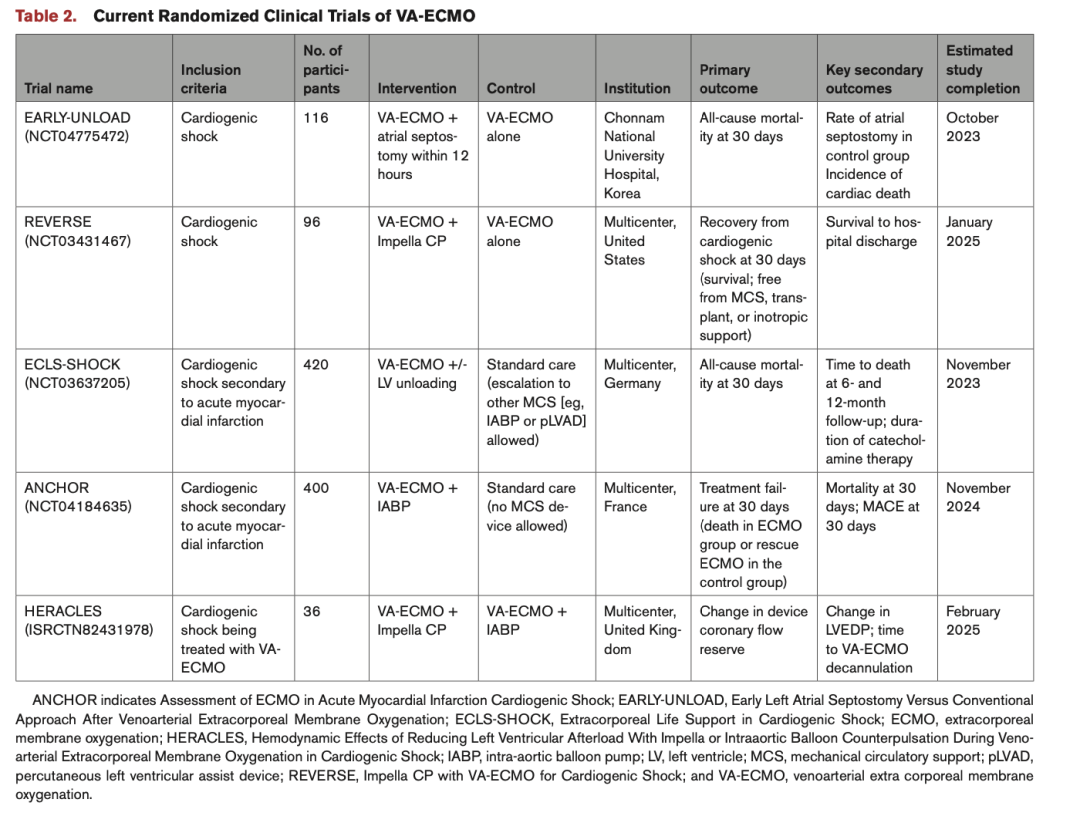
表2 现有VA-ECMO相关RCT
减压目标
在减压开始后,继续密切监测患者非常重要,以确保任何肺水肿等临床并发症缓解,ECMO流量和减压设备参数应持续优化,以达到足以提供全身灌注的平均动脉压,PCWP
研究结论
VA-ECMO是一种有效的MCS,能够支持全身灌注、提供机体氧合,但对心衰患者施加额外的血液动力负荷可能导致并发症并影响心肌恢复。心肌收缩功能不良或前负荷减少的患者容易发生后负荷增加所带来的并发症,这类患者应用预防性的左心室减压可能是有益的。对于没有左心室后负荷并发症的患者,预防性减压是否能改善心肌恢复和降低死亡率尚不清楚;潜在的益处必须与增加MCS设备的风险相比较。最后,减压方法的选择取决于当地医疗中心的个体化选择,缺乏指导某种方法的数据。更加详尽的生理学研究可能有助于个性化决策。我们提出了一种左心室减压的参考流程(图5),供VA-ECMO患者使用,以确定最佳的左心室减压方案。
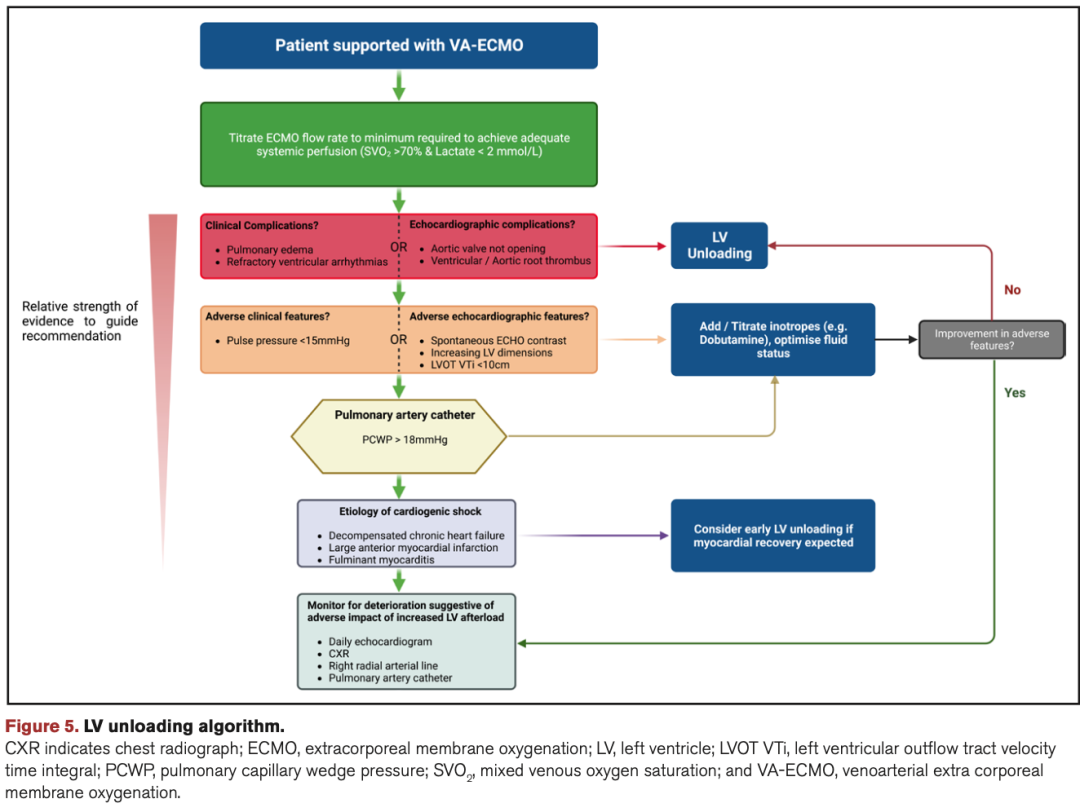
表1 左室减压临床策略流程参考
END
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。



 微信扫一扫
微信扫一扫