摘要:VA-ECMO是心源性休克患者短期机械支持方法之一,但会增加左心室压力(LV)。本文分析了这种症状的生理基础及治疗方法。这是一项对现有VA ECMO出现左心室扩张患者回顾性调查研究。我们研究了PubMed上对所有VA-ECMO、LV扩张和LV减压的相关论文,并回顾这些论文并加入我们的想法。我们还将讨论在哥伦比亚大学使用的各种LV减压策略。VA-ECMO患者左心室扩张受到日益重视。有文献表明,未能预见、认识和治疗左心室扩张的后果是严重的,并会进一步影响膨胀和收缩功能不全的左心室功能。心肌恢复受阻,左室血栓形成可能性增加。早期认识和积极治疗左心室扩张是帮助治疗这个危重病人的首要因素。
静脉动脉体外膜氧合(VA-ECMO)是目前公认的治疗重度难治性心源性休克的短期机械支持方法。接受VA-ECMO治疗的患者数量显著增加,来自体外生命支持组织(ELSO)的最新数据显示,2017年全年约有10,000名患者在那里行ECMO治疗,而10年前仅约2 500名。随着我们对ECMO治疗的经验的增长,我们更关注VA-ECMO支持之前未评估的细微差别,包括左心室(LV)扩张。VA-ECMO会在主动脉内产生更多的后负荷,而受损的LV不得不对抗这额外产生的后负荷导致的生理变化。鉴于左心室功能减弱的状态,左心室可能无法产生足够的心排出量,而主动脉瓣(AV)在整个心脏周期仍然关闭。左室扩张可能导致肺动脉压力升高,肺水肿,并影响左室恢复。
在这篇综述中,我们将分析VA-ECMO期间左室扩张的生理基础和危重病人的左室减压指征。我们还将讨论LV减压的各种方法以及我们在哥伦比亚大学使用的减压策略。
01
VA ECMO左室扩张的生理基础及临床表现
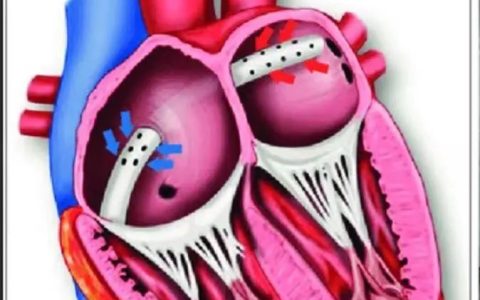
在VA-ECMO期间,动脉导管产生朝向AV的逆行血流,导致心脏上的后负荷升高并高于正常生理状态的原因。这明显增加的后负荷导致左室扩张,增加左室壁应力,并增加心肌氧需求(见图1)。持续高左室舒张末期压(LVEDP)会导致心肌内膜缺血,阻碍左室恢复。这会进一步损害左室功能,使左室恢复更加困难,特别是心肌梗死所致急性心源性休克及心肌炎患者。急性心源性休克患者左室顺应性差,可能二尖瓣功能尚存,合并左心室扩张风险大。与急性失代偿性慢性心力衰竭患者相比,心室在基线水平扩张,二尖瓣可能因这种环状扩张而丧失功能。二尖瓣反流可能肺水肿的主要原因。因此,左心室扩张的发生率在不同的人群中可能有所不同。
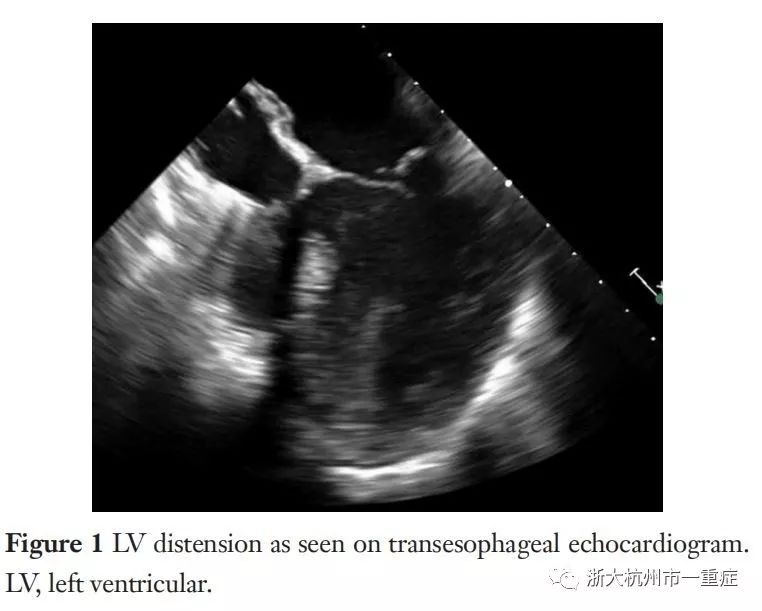
左心室扩张是由血液充盈心脏引起的,但是为什么在VA-ECMO期间左心室会充满血液,血液的来源于哪里?这必须满足两个条件:(1)必须有血液填满左心室;(2)心脏不能完全排出血液。对于后者,如上文所述,ECMO患者的后负荷增加及急性心脏损伤所致左室收缩能力下降,AV可能无法完全打开;而跨瓣膜梯度较高,也就是说主动脉压力明显高于LVEDP,房室不能开放和排出血液,血液停留在左室内,这是第一个条件的答案。就左心室的血液来源而言,这可能包括任何原因所致主动脉瓣反流,来自心脏最小静脉以及支气管血液回流,最重要的是,那些未在ECMO通路中的全身静脉回流的血液。这种通过二尖瓣顺行进入左室系统静脉回流是VA-ECMO期间进入左室的最重要的血源。这种情况与体外循环(CPB)的情况不同,CPB的储蓄装置和更短、直径更大的典型中心插管管路,在CPB上,LV是完全减压的。由于VA-ECMO缺乏储蓄装置,外周静脉导管较长,较薄,阻抗较高,临床医生必须选择其他方法来管理容量,包括利尿或中心静脉血液透析(CVVH)。
如果瓣膜梯度过大,AV在整个心脏周期内保持关闭状态,会导致主动脉根部的血液瘀滞和潜在血栓形成,尤其是在VA-ECMO插管处(图2)。这种情况在中心置管患者中发生的可能性要小一些,因为在中央主动脉的流出管或移植物的位置上,主动脉根部血瘀会减少。主动脉根部血栓会导致冠状动脉、脑部血管及身体发生致命性的栓塞事件。左心室扩张和左室压力升高会导致左心房和肺动脉压力升高,从而导致肺水肿,甚至肺出血,以及随后的全身、脑和心肌缺氧。综上,VA-ECMO期间重要的是适当的降低左心室压力。
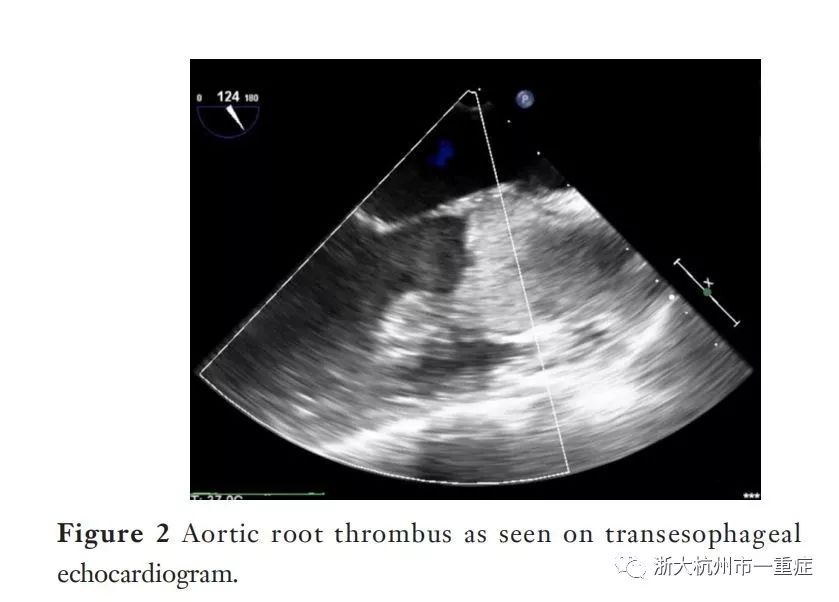
MarcDickstein及同事利用Starling曲线的计算机建模研究了VA-ECMO支持对LV扩张的影响。Starling曲线描绘了左室舒张末期压与卒中容积的关系,并解释了心输出量与容量状态的关系。他发现,在使用VA-ECMO来支持急性心源性休克患者,Starling曲线有相当大的偏移,特别是由于LV对VA-ECMO电路产生的后负载效应。他的结论是,随着后负荷的增加,LV扩张的肺毛细血管楔压(PCWP)将显著升高。进行VA-ECMO支持后,其Starling关系基本不变,但左室扩张程度和PCWP值将取决于患者左室收缩力和后负荷变化。对于急性心源性休克患者,VA-ECMO及其随之增加的后负荷将导致PCWP和LV扩张显著增加。
02
左室减压指征
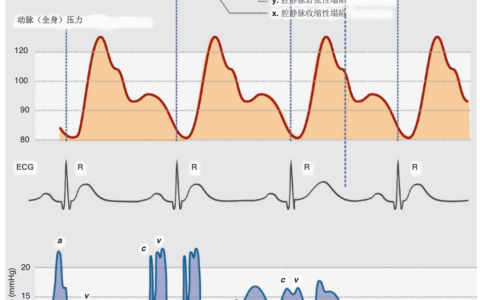
当使用VA-ECMO时,如果病人的心脏能够在心动周期内有一定射血,每一次心搏时房室开放,收缩期和舒张期之间脉压差大于10 mmHg,PCWP值保持在较低水平,这一临床现象表明左室可能有充分的减压作用。正性肌力药物、缩血管药物、利尿剂或CVVH都可以通过精细评估以达到这个目的。此外,ECMO流量可能被滴定到最低可接受的水平,从而产生足够的血压,有助于更好地将血液从心脏排出,同时减少后负荷。这种“部分流”策略以前曾被认为是用于治疗心脏切开术后休克患者的一种成功方法。心肌炎或心肌缺血所致急性心源性休克患者可能比局部血流策略需要更多的支持,这些患者的左室恢复应借助左室辅助减压装置。
然而,目前没有左心室扩张的评估标准,所以必须进行有效的临床调查。超声心动图可以准确地诊断左心室扩张,其表现为左室扩张和收缩功能下降,伴有或不伴有严重的二尖瓣关闭不全。如超声见血液在左心室内的停滞。使用SwanGanz导管非常重要,可以提供肺动脉舒张压和PCWP。PCWP是直接测量LVEDP最好的替代。肺动脉舒张压大于25 mmHg和PCWP升高表明左室尚未实现减压。扩张的左室也可增强心律失常发生率,因此,室性心律失常的出现是左室需要减压的另一个标志。总之,我们放置LV减压装置的指标包括以下任一项:(I)PCWP的升高;(II)如超声提示左室扩张、收缩不足或血液停滞;(III)在整个心脏循环周期中AV保持关闭;(IV)胸部X线可见持续性肺水肿;(V)难治性室性心律失常。
左心室减压的重要性已得到很好的证明。在20世纪80年代末和90年代初的儿科ECMO。文献中,首次详细描述了左室高压,它阻碍了VA-ECMO在新生儿呼吸衰竭患者和小儿心脏手术心脏术后心力衰竭的应用。左室减压最初应用在VA-ECMO上机流量稳定后出现肺水肿和持续高压导致肺出血的患者。随后包括通过球囊或导管制造等与各种外科和导管技术相关的迅速发展。这种左房减压的使用虽然它只减少左心室的前负荷但也是有益的。因为LA引流通常会连接到ECMO通路的静脉置管,这会使更多的血液回流入管路中,并经由动脉置管将回到患者体内,因此这可能不会降低左室后负荷,事实上有可能反到会增加。因此,随着技术的发展减压方法现在包括经过放置经皮左室辅助装置来实现。
随着时间的推移,随着ECMO在成人人群中的使用增加,重新建立LV减压装置的是有必要的。在最近的一项研究中,我们发现在正在进行中的VA-ECMO患者中,需要立即减压的左心室扩张发生率为7%,“亚临床”(不需要立即减压)心室扩张发生率为22%。在同一研究中,我们注意到了左心室扩张程度越大,越需要左室减压,心肌恢复的可能性也越小。特别是,我们研究了所有难治性心源性休克(RCS)的ECMO患者以及存活至出院的RCS患者,左心室扩张程度增加减少了心肌恢复的可能性。我们认为这是首次明确显示左心室扩张对心肌恢复的负面影响的研究。
03
左心室扩张的治疗
3.1 医学管理
传统的左心室减压方法包括医疗管理,透视下手术的经皮左心室减压方法。
从医疗管理开始,在这个病人群体中使用正性肌力药物是必不可少的。多巴酚丁胺和米力农是我们在实践中常用使用,但只考虑到它们能适度增加的心输出量和降低左心室扩张,我们需要快速寻找机械循环支持。其他医学辅助手段包括使用利尿剂和CVVH来控制容量和血压。
3.2 主动脉内球囊反搏
在机械循环支持方面,一种可用的经皮穿刺方法是IABP,它有助于左室减压。IABP具有众所周知的优点:在舒张期增加冠状动脉血流量,并降低后负荷。动物研究表明,动物研究表明VA-ECMO模型中LV后负荷显著降低。此外,一些中心通常会在所有VA-ECMO患者上放置IABP,并确定它能显著降低肺动脉楔压。一项欧洲研究显示,与单独使用ECMO支持的患者相比较,IABP联合ECMO治疗组的X线肺水肿征象明显减少,机械通气时间延长。但最近有一项超过对1500名样本进行的大规模汇总分析显示,VA-ECMO联合IABP没有生存益处。此外,本研究的阴性结果符合最近对心肌梗死和心源性休克患者的IABP的观察和随机研究。考虑到其不直接减少左心室压力,我们通常不会放置IABP用于左心室减压。
3.3 经皮左心房减压
在透视检查的帮助下,除了IABP,还有无数其他经皮穿刺的选择。病例报告和病例系列可追溯到20世纪80年代末和90年代初,记录了ECMO患者(18-20岁)非手术性左心减压的可行性。这些包括经间隔穿刺和左心房引流;经间隔球囊和叶片造口术;经皮插入肺动脉或逆行经主动脉导管。在儿科中,跨间隔气囊和叶片造口术仍然是一种常见的做法,但在成人中通常不常见。
3.4 坦德曼心脏
坦德姆心脏(LivaNova,Inc.,伦敦,英格兰)是ECMO循环支持间接左室减压的另一种方法。坦德姆心脏通过一个连续离心泵装置提供多达5 L/MIN的支持。股静脉通路建立后,左房经隔穿刺进入。氧合血从左心房抽吸,并可连接到ECMO电路的静脉通路。这可以使左室前负荷减少,但实际上并不是直接左室引流。此外,坦德姆心脏系统需要较大的循环套管,而房间隔穿刺会导致左向右分流。
3.5 左室减压开放手术放置
伴随的开胸手术发展,我们有可能对左心室进行手术减压。例如,在未能脱离CPB并转变为VA-ECMO的患者中,通过Y-连接器引流肢体静脉血经由右上肺静脉可并入ECMO通路中。术中经胸超声心动图(TTE)可帮助评估左室扩张和减压的需要,并指导管路放置。管路放置在左心室尖端部位是最直接的减压方法,但必须采用精细的手术技术和充分的止血。非开腹后患者,仍可通过左前外侧开胸术将手术减压装置置入左室。
3.6 脉冲泵(Impella)
脉冲泵(Abied Danvers,MA,美国)是一种微型轴流泵。由带有流入套管的电动机驱动泵穿过房室进入左室,从左室腔抽血,并将血液排出升主动脉。因此,它减少了左心室射血做功,而不增加后负荷。心输出量的大小取决于泵的速度和生理后负荷,而装置的位置对优化功能至关重要。Impella有一个内置的压力信号,可以知道泵放置的正确位置,且超声心动图可以确认这一点。它可以通过经皮股动脉入路放置,通过这个途径,在透视引导下,泵通过一系列逐步的导线进入左室。水泵开机后逐渐增加转速。引流血源自左室,流入升主动脉,是连续的通过心脏周期,且不依赖于心电。我们认为这是Impella的主要优势:它会直接排出左心室。必须保持正确的定位,以确保足够的低压减压。因支持过程需要全身抗凝治疗,有导致溶血和出血的风险。
Impella的次要和尚未评估的优势是考虑到其进入主动脉根部的装置,它可以防止主动脉根部停滞和血栓形成,也可能导致冠状动脉栓塞、中风或其他血管破坏性并发症的原因。这在动脉无脉动的患者中尤其重要,因为这意味着没有自主心脏有效射血,也没有血液从心房流出。由于它的瓣膜位置,脉冲也将保持持续的冠状动脉灌注。
3.7 ECpella
对于急性心源性休克患者,尤其是急性心肌梗死后合并出现左心室扩张的患者,我们选择的复苏策略是同时放置VA-ECMO和Impella CP或“ECpella”(图3)。这可以在导管实验室或手术室指导完成。如果患者正在进行紧急床边体心脏复苏术(ECPR),我们通常进行经皮ECMO插管,然后在观察到左心室扩张的证据后,前往导管实验室进行Impella置入。再股动脉较小或有基础疾病的病人中,无论是在Impella置管侧还是在ECMO置管侧,我们都应该关注腿部灌注是否充足,我们可以通过股浅动脉置管放置远端灌注导管。
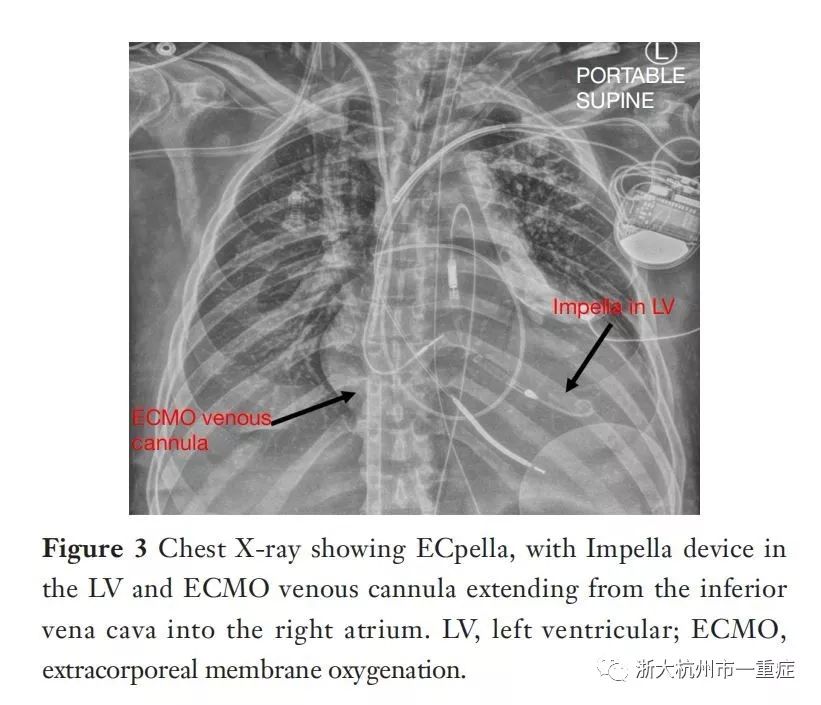
通常,在ECpella的支持下,我们预计Impella会产生1.5到2L/MIN的流量,实现辅助心排这一目标。在可行的情况下,我们使用部分流量VA-ECMO支持维持在3-4L/MIN,在保证末端器官灌注的目标前提下以保持固有心肌收缩性。可通过中心静脉置管、Swan-Ganz导管,用于检查混合静脉饱和度、PCWP和肺动脉压力。当然,每日胸部X线检查应有助于评估肺水肿程度、Impella脉管位置和ECMO置管位置。经食管超声心动图(TEE)或TTE也可用于确保脉冲保持在正确的位置,并确保左心室得到充分的减压。
一旦支持流量调节到低水平,ECpella系统就可能开始撤机。我们通常在1.5-2L/MIN的时候留逐渐降低ECMO的流量。收缩功能的恢复通常表现为动脉波形的搏动性增加,脉压稳定增加。此时,ECMO首先被移除,将Impella保留。如果患者需要额外的支持,Impella可以被提升到更高的流量,Impella CP可以产生大约4L/MIN的流量。
我们在这一战略上取得了成功。我们最近证明,联合应用Impella,VA-ECMO支持,我们的病人有更高的降低肺动脉压的比率。单独使用VA-ECMO支持的患者与联合ECpella支持的患者的生存率相似,但是应用联合支持的患者的病情更严重。各组间并发症少且基本相当,但有例外,ECpella组溶血率较高。
其他团体也报告了类似的结果。Patel和他的同事报告表示,联合Impella,VA-ECMO支持可以显著降低患者30天到1年的全因死亡率。除了在VA ECMO支持中更多地使用正性肌力药物外,在继发结果上没有差异。通过统计分析,作者认为Impella装置直接进行LV减压可以提高患者的生存率。同样,圣路易斯华盛顿大学医学院的Tpper和Associates对VA-ECMO患者的外科减压和Impella左心室减压进行了比较。他们得出结论认为,使用Impella是一种有效的左室减压手段,可以防止肺水肿的恶化,其结果和并发症类似于外科左室减压。且欧洲的Pappalardo等人的报告说,VA-ECMO和Impella组患者的住院死亡率明显低于仅使用ECMO的患者。更重要的是,VA-ECMO和Impella患者的桥接成功率更高,无论是进一步的康复还是其他治疗。正如预期的,ECPella组的溶血率较高,可能归因于Impella。
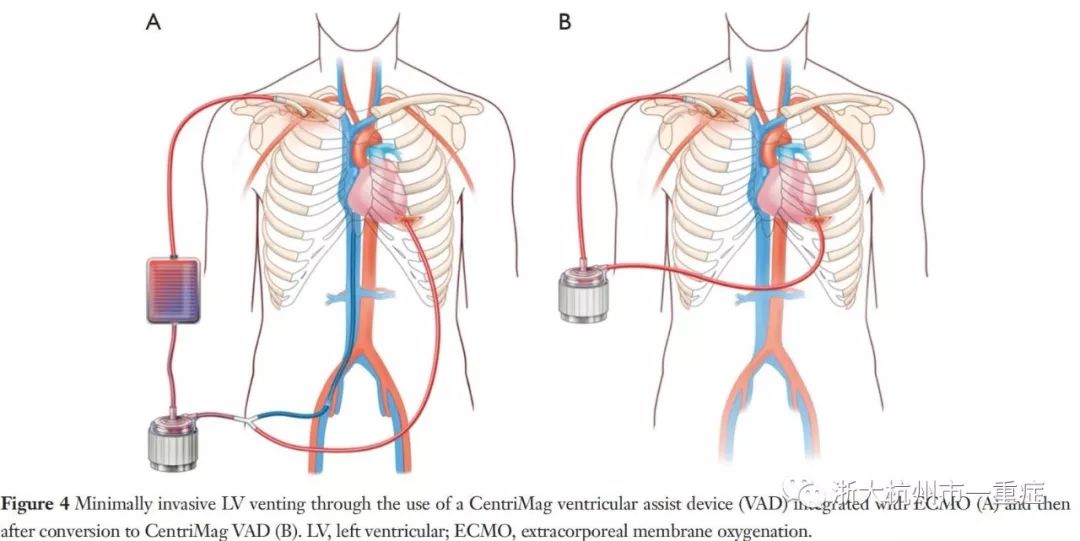
3.8 微创LV减压以及中央型左心辅助装置(LVAD)联合ECMO应用
我们开发了一种微创途径,通过使用心室辅助装置(LVAD)和ECMO(图4)。简言之,这结合了从股静脉或颈静脉的静脉血流和左室前端的血流,将它们是汇入一起流入循环。在循环通路中也有一个氧合器,并使用一个可调节的管夹来滴定两个流入患者(静脉和左室心尖)的流量(图4A)。此方法除ECpella外,有多项优势:(I)增高上身含氧血液的灌注;(II)有效地对右心室及左心室减压;(III)通过摘除循环通路中的氧合器来调动病人的自身新功能(图4B);(IV)潜在地避免胸骨切开术,从而避免再次手术对胸骨的损伤,以及随后的长期VAD植入或心脏移植做准备。
结论
左室扩张是在VA-ECMO支持中一个日益被重视的并发症。无法预测、识别和治疗左心室扩张会导致严重后果,并且可能使已经扩张和收缩减低的左心室功能进一步恶化,使心肌恢复更加困难,增加肺水肿和左心室血栓形成可能。我们认为直接减压是治疗左室扩张的最佳方法,因为它减少了左室的预负荷和后负荷。我们预计,在未来,将会有更小的LV减压装置应在VA ECMO支持过程中,特别是在急性心脏支持的患者应尽早采用。早期识别和对LV扩张的积极管理对于帮助重症患者人群是至关重要的。
原文链接:https://pan.baidu.com/s/1FaUuCmI-nwov5CavxmRYjw
提取码:hbxt
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫