癫痫是最为常见的慢性神经系统疾病之一,影响了全球范围约6 900万患者 [ 1 ] 。即使在规范使用抗癫痫发作药物(anti-seizure medications,ASM)的前提下,仍有约30%患者的癫痫发作控制不理想。对癫痫疾病强调在病因层次进行管理,而“免疫性”因素已经被列入癫痫病因之一 [ 2 ] 。“自身免疫性癫痫(autoimmune epilepsy)”的概念于2002年的国际自身免疫大会上首次提出,表明自身免疫因素在部分癫痫患者中的重要性 [ 3 ] 。2017年,国际抗癫痫联盟(International League Against Epilepsy,ILAE)出版的癫痫定义和分类指南中,正式将“免疫性”列为癫痫的六大病因(结构性、遗传性、感染性、代谢性、免疫性、未知)之一;“免疫性”病因的患者可能受益于免疫治疗,与其他病因的癫痫患者在治疗方式上存在不同,从而成为研究热点 [ 4 ] 。近年来,“自身免疫性癫痫”这一概念被大量应用,有很多学者对于在自身免疫性脑炎的背景下使用“癫痫”一词提出质疑 [ 5 , 6 ] 。针对这一问题的存在,ILAE自身免疫和炎症特别工作组于2020年提出了两个新概念定义:继发于自身免疫性脑炎的急性症状性痫性发作(acute symptomatic seizures secondary to autoimmune encephalitis,ASSAE)和自身免疫相关癫痫(autoimmune-associated epilepsy,AAE) [ 7 ] 。2023年在 Epilepsia上发表的一篇专家述评,对神经抗体相关癫痫的专业术语进一步澄清,将AAE修改为自身免疫性脑炎相关癫痫(autoimmune encephalitis-associated epilepsy,AEAE),有助于明确此类癫痫发作和脑炎之间的关系 [ 8 ] 。
我们通过检索文献,对ASSAE和AEAE这两个诊断实体的定义、流行病学、病因、临床表现、诊断、治疗和预后进行综述,以期能为神经科医生在临床上处理和应对自身免疫性病因有关的癫痫提供参考。检索条件:以“epilepsy”“seizure”“epilepsy/immunology”“autoimmune epilepsy”“autoimmune-associated epilepsy”“acute symptomatic seizures secondary to autoimmune encephalitis”“treatment”“outcome”作为检索关键词在PubMed、Web of Science数据库进行检索,选择在近10年内发表的文献。
三、临床表现
AE的癫痫发作特点为急性或亚急性起病、频繁发作。病毒前驱感染的病史很常见。频繁的、多灶性、对ASM耐药的痫性发作,尤其是发生在既往无癫痫病史或无任何危险因素的患者时,神经科医生应怀疑ASSAE或者AEAE的存在。某些类型的癫痫发作可能提示潜在的免疫学病因,如面-臂肌张力障碍发作(faciobrachial dystonic seizures,FBDS)常提示抗LGI1抗体的存在 [ 10 ] 。一些患者可能表现为新发难治性癫痫持续状态(new-onset refractory status epilepticus,NORSE)或发热感染相关性癫痫综合征(febrile infection-related epilepsy syndrome) [ 30 ] 。约37%的NORSE病因诊断是AE,而隐源性NORSE(cryptogenic NORSE)占所有NORSE患者的50% [ 31 ] 。 表1 总结了疑似ASSAE的临床症状线索 [ 2 ] 。
四、诊断
在采集疑似ASSAE或者AEAE的病史时,除了需要详细记录癫痫发作的情况外,还需要关注其他有关的神经系统症状,包括精神症状、记忆损害、运动障碍、自主神经功能受损等,这些均有助于建立ASSAE或者AEAE的诊断 [ 2 ] 。此外,一些重要的辅助检查手段也能为ASSAE或AEAE的诊断确立提供重要依据。
1.脑电图和头部MRI:脑电图是癫痫疾病诊断的重要辅助检查手段之一。AE患者常有异常脑电图表现,但是脑电图结果无异常也不能完全排除AE的诊断。脑电图可呈现多种结果,包括正常、局灶或广泛性慢波发放、痫样放电等。广泛节律性δ波发放,可伴或者不伴β波发放(称为“极端δ刷”),是抗NMDAR脑炎的特征脑电图表现 [ 32 ] ,但是伴FBDS的抗LGI1脑炎患者常呈现为正常脑电图 [ 33 ] 。推测有可能是由于致痫灶位置太深或是涉及到的神经元聚集团太小 [ 2 ] ,而导致头皮电极无法接收到同步脑电活动。总的来说,脑电图在AE诊断上的特异度不高。
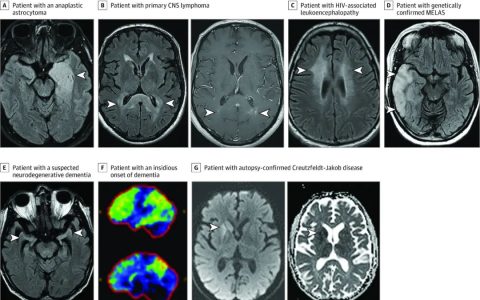
在起病初期,约30%~50%的头部MRI是正常的,但是到疾病后期,可能出现一些提示AE的影像学表现,包括典型的内侧颞叶的FLAIR高信号、多灶性灰质和(或)白质异常FLAIR信号等 [ 34 ] 。有研究尝试将AE急性期某些MRI异常结果与不良预后或者慢性癫痫的演变趋势进行关联,如抗NMDAR脑炎中出现弥漫性小脑萎缩预示着预后不良 [ 35 ] ,急性期AE头部MRI上出现不可逆的额颞叶病变、海马硬化是演变为慢性、难治性AEAE的危险因素之一 [ 36 ] 。
2.自身免疫性抗体检查:在脑脊液和(或)血液中检测到自身免疫性抗体的存在对于ASSAE或者AEAE的诊断确立有着关键性的作用。然而,抗体的检测过程往往需要花费数天乃至数周,这极大地延长了最终诊断确立的时间 [ 37 ] 。于是Graus等 [ 38 ] 提出了一套在抗体检测结果未回报前的AE早期诊断标准:(1)亚急性起病,3个月内出现工作记忆下降、意识状态改变或精神症状;(2)至少有下述1项神经系统症状:新发的局灶性CNS改变、无法用既往疾病解释的痫性发作、脑脊液白细胞增多、与脑炎有关的头部MRI改变;(3)合理排除其他疾病。对符合早期诊断标准的患者,建议尽快完善抗体检测并请神经免疫医生协助诊疗。
行自身免疫性抗体检测时推荐同步对血清和脑脊液样本进行多种抗体筛查,而不是仅在血清或脑脊液中检测单一抗体。比如抗LGI1抗体更多在血清中检测到,而有15%的NMDAR-IgG仅能在脑脊液中检测到 [ 38 ] 。此外,不同的抗体检测方法对抗体检测结果也有影响。不鼓励单独使用无组织免疫荧光的基于细胞底物的实验(cell-based assays,CBA)方法,反之亦然。因为有研究证实分别使用活细胞CBA法和固定细胞CBA法检测抗体,在敏感度和特异度方面会导致不同的结果 [ 39 ] 。在未来研究方法学部分,鼓励联合使用验证性检测(如CBA法结合免疫荧光检测法)以及通过实验室检测进行外部验证来确保结果的严谨性和可重复性。
3.正确解读自身免疫性抗体检测结果:抗体检测对于临床治疗以及预后评估的意义有多大?这需要神经科医生能正确解读抗体检测结果。对于大多数抗体而言,现存的很少数据能证实抗体的滴度与临床症状的严重程度或者免疫治疗效果有关联。一些非特异性的自身免疫系统疾病抗体的出现,一般不被认为是ASSAE或AEAE的病因,如抗核抗体和抗甲状腺过氧化物酶抗体(anti-thyroid peroxidase antibody,TPO-ab) [ 40 ] 。然而,值得注意的是,系统性自身免疫疾病的存在常提示CNS免疫易感性 [ 41 ] 。电压门控钾离子(voltage-gated potassium channel,VGKC)抗体是与VGKC复合物结合的非特异性神经元抗体,之前被认为是致病性抗体,而最近在正常人群中也能检测到。针对VGKC复合物抗体的放射免疫分析发现了2种类型抗体:一类致病性抗体是结合到LGI1和CASPR2的表面暴露结构域,另一类非致病性抗体则是结合到VGKC复合物的细胞内结构域 [ 2 ] 。因此,当疑似ASSAE或AEAE诊断时,仅检测抗LGI1抗体和抗CASPR2抗体即可 [ 42 ] 。也有研究质疑仅在血清样本中出现抗体阳性结果的价值,如血清中低滴度的GAD65抗体可以在正常人群和1型糖尿病患者中发现 [ 43 ] 。临床医生不能仅依据抗体阳性结果就草率得出ASSAE或AEAE的诊断。
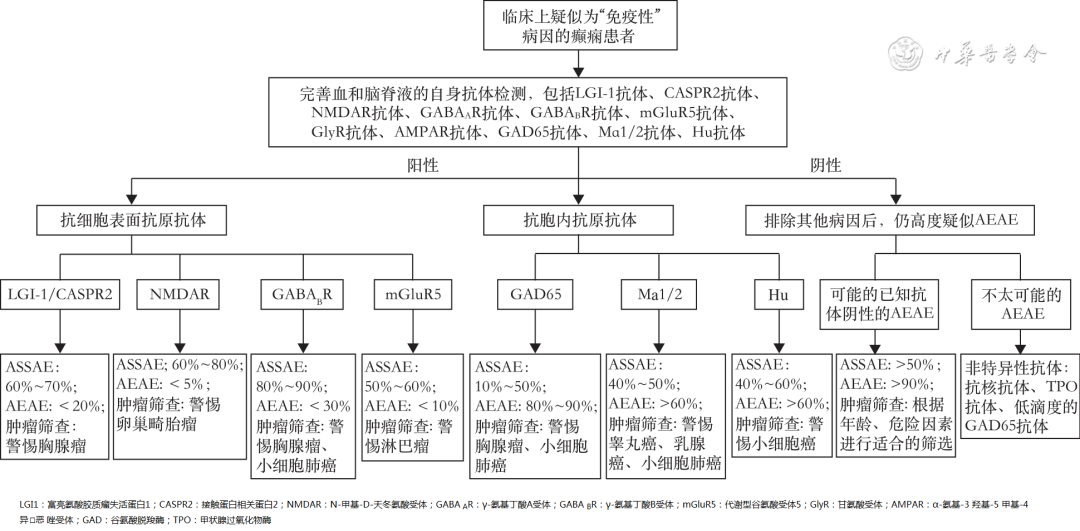
虽然很多与AE有关的抗体正在逐步被认识和了解,但是还是存在大量的未知抗体。如果没有检测到已知抗体,但仍高度疑似ASSAE或AEAE的诊断,这些患者被称为“抗体阴性ASSAE或AEAE” [ 44 ] 。抗体阴性ASSAE或AEAE患者很少能接受到及时的免疫治疗,导致出现较长时间的癫痫持续状态(status epilepticus)和死亡。美国梅奥诊所的相关指南建议在排除感染性病因后,可以开始考虑对这些患者使用免疫治疗。虽然抗体检查对于ASSAE或AEAE的诊断有着极大的辅助价值,但它绝不会取代临床症状的核心意义。 图1 是美国梅奥诊所推荐的ASSAE和AEAE的诊断流程 [ 2 ] 。
图1 美国梅奥诊所推荐的继发于自身免疫性脑炎的急性症状性痫性发作(ASSAE)和自身免疫性脑炎相关癫痫(AEAE)的诊断流程(2021年;在参考文献[ 2 ]中推荐诊断流程的基础上绘制)
Figure 1 The diagnostic algorithm of acute symptomatic seizures secondary to autoimmune encephalitis (ASSAE) and autoimmune encephalitis-associated epilepsy (AEAE) recommended by the Mayo Clinic in the United States (2021; drawn on the basis of the diagnostic process recommended in reference [ 2 ])
4. 不明原因癫痫和脑病的自身抗体流行率评分(Antibody Prevalence in Epilepsy and Encephalopathy score,APE)和自身抗体致局灶性癫痫症状和体征评分(Antibodies Contributing to Focal Epilepsy Signs and Symptoms Score,ACES):近年来,很多研究都总结了自身免疫性病因介导的癫痫发作和癫痫患者的共同特征,并形成了系统性评分量表用于协助诊断。APE以及ACES就是这类评分量表的2个典型代表。
APE是一份10项、总分15分的评分量表,目的是试图依据临床表现和初步的神经病学评估结果来筛选出可能需要完善抗体检测的不明原因癫痫患者。在387例符合癫痫诊断并且完善抗体检测的患者队列中,对APE进行内部验证。其中有44例(11.4%)患者检测到特异性CNS抗体,抗体阳性的患者中APE评分≥4分的比例明显较高(97.7%比21.6%)。有研究结果证实当APE评分≥4分时,预测抗体存在的敏感度和特异度分别为87.5%和83.8% [ 45 ] 。2019年,Dubey等 [ 46 ] 在2017年提出的原有APE的基础上,提高FBDS的权重,同时头部MRI影像异常的定义由之前的“单侧/双侧内侧颞叶T 2FLAIR高信号”拓展至包括“多灶性T 2FLAIR高信号”,从而提出癫痫和脑病患者的自身抗体流行率评分 2(Antibody Prevalence in Epilepsy and Encephalopathy score 2,APE 2),APE 2评分≥4分的诊断特异度提高至85%。APE 2的细则详见 表2 。Liu等 [ 47 ] 亦提出了APE 2评分表的中国患者版本(APE 2-CHN),研究纳入了191例不明原因的中国癫痫患者,发现APE 2-CHN评分≥5分时,在预测特异性自身抗体存在的敏感度和特异度分别为85.5%和58.9%。虽然大多数临床医生可以很容易地使用这个评分量表筛选出需要进行抗体检测的目标患者群体,但值得注意的是,APE 2量表可能更适用于筛选ASSAE患者,而对AEAE的诊断敏感度不够。
de Bruijn等 [ 23 ] 制定的ACES能很好地弥补APE对AEAE敏感度不高的缺点。ACES量表是包含6项(认知症状、行为改变、自主症状、言语障碍、自身免疫性疾病、MRI上颞叶高信号),每项赋值1分的评分量表。de Bruijn等 [ 23 ] 在128例颞叶癫痫患者组成的队列中对ACES进行外部验证,发现当评分截断值≥2分时,特异性神经抗体阳性的局灶性癫痫患者的敏感度和特异度为100%和84.9%;该研究发现对于病程超过1年的局灶性癫痫患者,ACES量表比APE 2量表有更好的预测能力 [ 23 ] 。在实际临床工作中,ACES量表较APE 2量表在使用上更为简单,且在无明显脑炎症状的局灶性癫痫患者的筛查中更具有优势。然而现有的评分量表仍然不太完善,未来需要结合更为详细的癫痫发作症状学描述,以及在临床实践中大规模使用。
五、治疗及预后
关于AEAE和无明显脑炎症状的ASSAE的治疗目前尚无标准化治疗方案,现有的治疗方案基本来源于AE的相关研究。被广泛认可的治疗手段主要包括免疫治疗、ASMs和其他治疗。
一项观察性研究证实,早期免疫治疗能有效缩短癫痫发作时间、改善认知预后 [ 48 ] 。目前推荐的一线免疫治疗方案包括:静脉注射甲泼尼龙(1 g/d,持续3~5 d),静脉注射免疫球蛋白(0.4 g·kg -1·d -1,持续5 d)和血浆置换(建议进行5次,隔日1次)。如果一线治疗无效或收效甚微(癫痫发作频率降低[ 2 ] 。McGinty等 [ 24 ] 发现免疫治疗对于在脑炎背景下的癫痫发作控制效果好,但是对于AE相关癫痫的疗效不理想。
目前没有足够数据明确不同的免疫治疗药物之间的疗效优劣,也没有足够的数据表明如果患者在第一轮免疫治疗后没有改善,尝试第二轮或第三轮免疫治疗是否给患者带来好处。尽管有研究结果表明在起病之初尽早使用二线免疫抑制药物是有效的,但是免疫抑制剂的维持时间和药物类型选择仍有待商榷 [ 2 ] 。最近的研究发现,血清和脑脊液细胞因子白细胞介素1(interleukin 1,IL-1)和IL-6升高的患者,对针对性的细胞因子调节剂可能有用,如阿那真素(针对IL-1)和托珠单抗(针对IL-6) [ 2 ] 。
ASM作为联合治疗手段,应与免疫治疗同步进行。Vogrig等 [ 49 ] 认为与免疫病因有关的癫痫发作其治疗应该个体化,要依托抗体类型、脑电图表现、影像学结果综合分析,但仍缺乏大样本的临床研究证据。至于是否要根据不同抗体类型选择不同类型的ASM或者哪种类型的ASM疗效更好,目前尚无定论。总的来说,ASM总体疗效相对较低。有证据表明钠离子通道阻滞类型的ASM(如卡马西平和拉考沙胺)在这类患者中更有效 [ 50 ] 。虽然AEAE患者可能需要终身服用ASM,但是ASSAE患者,尤其是神经细胞表面抗体(如抗NMDAR抗体和抗LGI1抗体)阳性的患者,可能只需要短期的ASM治疗 [ 51 ] ,但关于在脑炎急性期后ASM的确切持续治疗时间尚不清楚 [ 2 ] 。
其他治疗方式包括癫痫外科手术、性激素替代治疗、合并的副肿瘤病灶切除和治疗等。事实上,由于其癫痫发作的多灶性起源,很多难治性AEAE患者的癫痫外科手术效果不甚理想。在一项多中心的回顾性研究中,研究者对8例抗GAD65抗体阳性的难治性癫痫患者进行术后随访,仅2例患者处于恩格尔等级(Engel′s classes)Ⅰ或Ⅱ级,与颞叶癫痫伴海马硬化患者颞叶切除术后70%~80%的有效率相比,难治性AAE的术后癫痫发作可能性更高 [ 52 ] 。此外,一些神经调控疗法,包括反应性神经刺激疗法已被批准用于治疗,但还需要前瞻性多中心的研究来验证神经调控疗法的效果 [ 53 ] 。Heiry等 [ 54 ] 使用外源性睾酮替代治疗了1例47岁抗GAD65抗体阳性的难治性男性癫痫患者,患者的癫痫发作频率从每天发作15~20次降低到每天发作1~4次,这为难治性AAE的癫痫治疗提供了新的思路。对于合并的副肿瘤进行切除或者治疗,对于延长患者的生存期、改善预后是必要的。
此外,一些靶向性的单克隆抗体药物正在被批准用于ASSAE和AEAE的治疗 [ 26 ] 。比如,已经被用作AE二线免疫治疗药物的利妥昔单抗(rituximab),就是一种针对B细胞表面CD20抗原的B细胞耗竭剂。此外,同样是靶向CD20的单克隆抗体奥美珠单抗(ocrelizumab)和奥法木单抗(ofatumumab)也开始尝试用于AE的临床治疗。靶向CD19和CD38的B细胞耗竭剂伊奈利珠单抗(inebilizumab)和达雷妥尤单抗(daratumumab)也有正在进行的前瞻性药物临床试验(ExTINGUISH和NCT04372615)。鉴于细胞因子IL-6参与免疫稳态和多种自身免疫性疾病的发病机制,靶向或针对IL-6的药物也获批用于治疗自身免疫性疾病 [ 55 ] 。托珠单抗(tocilizumab)作为IL-6的阻滞剂,已被用于治疗利妥昔单抗难治性的AE患者,且与其他免疫治疗策略相比,显示出较好的临床反应 [ 56 ] 。
新型ASMs的推出也为难治性AEAE的药物选择提供了更多的可能。Serrano-Castro等 [ 57 ] 从5家癫痫中心共收集8例难治性的GAD65阳性的癫痫患者,联合引入新型ASM苯巴那酯(cenobamate)和氯巴占治疗,使癫痫发作次数中位数减少了92.22%。苯巴那酯作为突触和突触外GABA AR的正变构调节剂,主要是通过增加大脑中的抑制性神经传递而抑制癫痫发作。基于脑机接口的反应性神经刺激(responsive neurostimulation system,RNS)也被批准用于难治性癫痫的治疗,有研究人员试图在AEAE患者中使用RNS系统进行治疗,发现9例AEAE患者中有4例在植入RNS系统后癫痫发作频率出现下降,证实RNS系统的辅助治疗可能是难治性AEAE患者的治疗选择之一 [ 58 ] ,但仍需要进行更多的多中心前瞻性随机性研究。
六、小结与展望
总的来说,ILAE提出的新术语将自身免疫性病因介导的癫痫发作和癫痫分为ASSAE和AEAE两大类。ASSAE强调在脑炎急性期背景下继发的症状性癫痫发作,以抗神经元表面的抗原的自身抗体阳性为主,对免疫治疗效果好,只需要持续短期的ASM治疗;AEAE指由自身免疫因素介导的癫痫持续易感状态,免疫因素、脑炎后结构损伤或其组合等多种因素导致其演变成难治性癫痫,免疫治疗和ASM治疗效果均欠佳。自身免疫性抗体检查对于ASSAE或AEAE的诊断是必要的,但应结合临床表现,慎重解读抗体检测结果,并留意抗体阴性ASSAE或AEAE的存在。APE和ACES能协助筛选出需要完善抗体检查的不明原因的癫痫目标群体,但需要在大规模的临床实践中更多地使用。被广泛认可的治疗手段主要包括免疫治疗、ASM和其他治疗,但标准的治疗方案尚无共识和定论,未来需要更多前瞻性的研究以确定免疫抑制治疗的持续时间、ASM的种类选择以及其他治疗方式的效果。随着对自身免疫病因介导的癫痫和癫痫发作的认识不断深入以及新抗体不断被发现,自身免疫性病因在癫痫中的占比逐步升高。临床医生需更早地识别癫痫的自身免疫病因,及早地针对免疫病因进行干预,才能更快更好地控制癫痫发作,改善患者的长期预后。
参考文献略
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。




 微信扫一扫
微信扫一扫