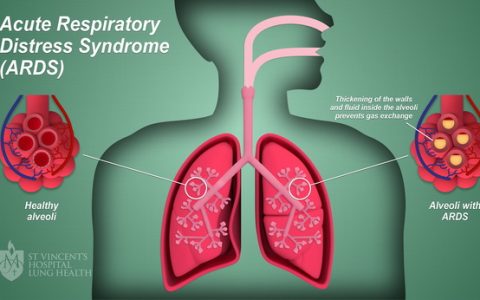
脓毒性休克患者组织灌注压的评估:超越平均动脉压

目的:
优化大循环血流动力学仅是脓毒性休克患者循环管理的起点。本文旨在阐述影响动脉压和组织灌注的多种因素之间的相互作用,如何优化这些因素,并在床边如何评估它们。本文是一篇简明而权威的综述,重点探讨在脓毒性休克患者中超越平均动脉压(MAP)的组织灌注压(TPP)评估。
数据来源:
通过PubMed和MEDLINE数据库检索与脓毒性休克、动脉血压、临界闭合压(Pcc)、平均系统充盈压(Pmsf)和TPP相关的原始文献。必要时也通过上述数据库补充支持性证据。
研究选择:
纳入英文发表的系统评价、叙述性综述、Meta分析、随机对照试验和观察性研究。
数据提取与综合:
作者对相关文献中的数据进行审阅、筛选和总结,并在适当情况下应用于本研究。
结论:
在脓毒性休克中,动脉压与临床结局之间的关系复杂且具有异质性。关注关键参数(如TPP、血管瀑布效应及个体化治疗反应)有助于实现以灌注为核心的个体化治疗策略,而不仅仅是关注血压数值。当微循环灌注不足在大循环目标已达标的情况下持续存在,提示需及时评估微循环状态,以避免潜在的液体或升压药物治疗过度。床边测量收缩压、MAP、舒张压、Pcc与Pmsf等指标,为监测与个体化治疗提供了实用工具。未来临床试验仍需验证这些参数的有效性,并进一步优化脓毒性休克的复苏策略。
要点
问题: 在脓毒性休克患者中,除了平均动脉压(MAP),我们是否可以评估组织灌注压(TPP)和血管张力?
研究发现: MAP 相对于临界闭合压(Pcc)定义了 TPP,而 Pcc 与平均系统充盈压(Pmsf)之间的压力梯度则定义了“血管瀑布”,这是实现局部血流自动调节的关键。低血管张力表现为舒张压的降低。值得注意的是,心动过速通过缩短舒张期回流时间,虽然在一定程度上减轻了低血压,这是有利的,但也掩盖了血管张力减弱(血管麻痹)的表现。在脓毒状态下,若血流动力学因素导致组织灌注不足,那么复苏策略应当旨在同时恢复 TPP 和局部血管瀑布,从而改善宏循环参数(如 MAP 和心输出量)与微循环灌注之间的联系。这种对脓毒症诱发的组织低灌注机制更广泛的理解,有助于更为细致地调整液体、血管活性药物及正性肌力药物的使用。
意义: 动脉血压及其衍生的组织灌注参数可在床边进行估算,可能为临床决策提供指导,超越传统仅以 MAP 为依据的做法,优化脓毒性休克患者的管理策略。
引言
脓毒性休克是一种危及生命的疾病,其特征为血管扩张性麻痹(vasoplegia),导致组织灌注受损,进而引发器官功能障碍和死亡。动脉低血压的程度与持续时间均会影响死亡率。通过液体复苏和血管活性药将平均动脉压(MAP)和心输出量(CO)恢复至阈值目标,并不一定能够恢复器官功能或改善组织灌注。可测量的大循环参数与微循环灌注之间存在失偶联现象,这提示我们需要更深入地分析动脉压和组织血流的决定因素。
动脉压与器官血流的决定因素
动脉压不是一个单一的数值,也不能单凭其数值来界定病理状态或器官灌注情况。理解其决定因素对于临床决策至关重要。决定动脉压力的四个主要参数包括:收缩压(SAP)、舒张压(DAP)、脉压(PP)和平均动脉压(MAP)。如图1所示,SAP为左心室射血所产生的峰值压力,受动脉张力、反射波及动脉的粘弹性特性共同影响;DAP为射血前的最低压力,由中心血容量、血管张力及心率决定;PP为SAP与DAP之差,受搏出量、血管顺应性及SAP/DAP因素影响;MAP是一个代表整个心动周期中动脉压力的算术平均值,计算公式为:DAP + 1/3 × PP。
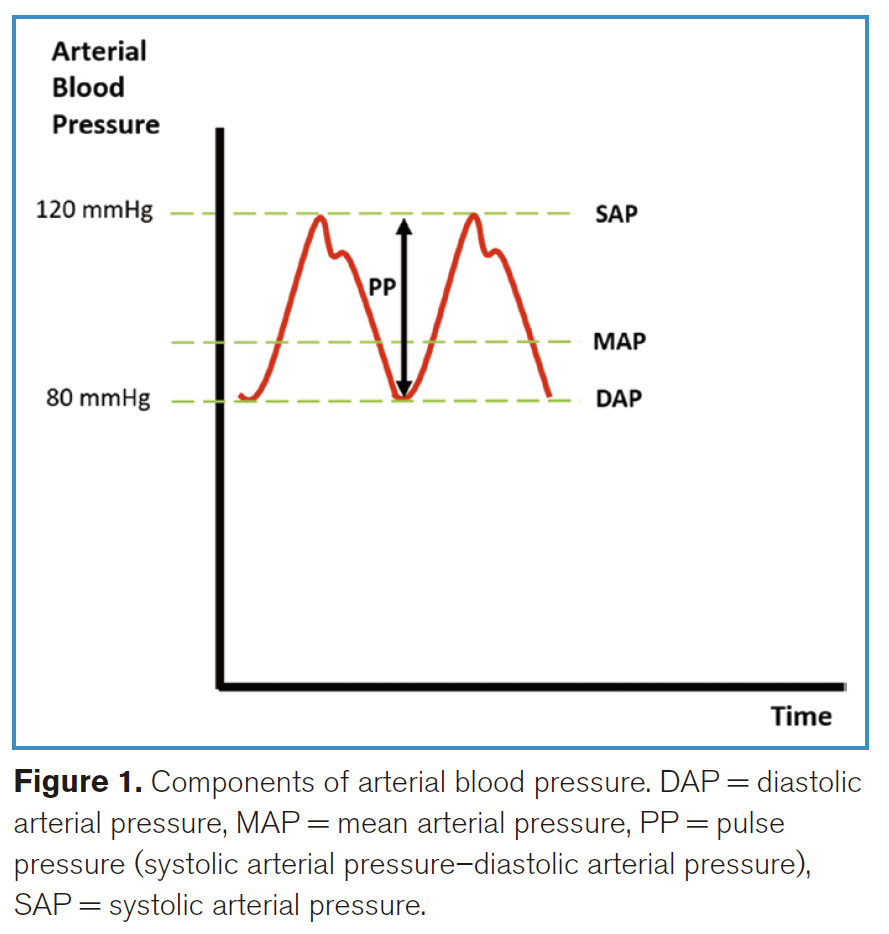
脓毒性休克的共识定义包括低血压(如SAP ≤ 100 mmHg)或为维持MAP而需要使用血管活性药。指南推荐初始MAP应大于或等于65 mmHg,这一目标是合理的,因为SAP在动脉系统中各部位存在差异。如果复苏目标仅依据最低SAP,可能会导致复苏失败。低DAP常反映血管扩张状态;而与SAP不同,MAP在整个动脉树中相对恒定,更能反映平均动脉压力。
MAP在动脉系统向小动脉/小动脉末梢的恒定性反映了大血管在舒张期起到储压器作用,在前向血流极少时仍能维持压力。随着动脉分支至更小的血管,总横截面积增加,血管阻力上升,血压在较短距离内迅速下降。当血管腔内压力低于由平滑肌张力所维持的血管壁张力时,血管发生塌陷,此压力即为动脉临界闭合压(Pcc)。在血管张力减弱(如脓毒症)时,该塌陷点向远端移动;而在血管张力增强(如早期失血性或心源性休克)时,则向近端移动。组织通过调节小供血动脉/小动脉的血管张力来满足代谢需求,从而调控局部血流。
组织灌注压(TPP) 是平均动脉压(MAP)与动脉临界闭合压(Pcc)之间的梯度。血流的变化是通过血管张力的反馈性调节实现的,这一过程依赖于内皮的逆行信号传导。Pcc 的变化若要影响血流,需满足两个条件:(1)TPP 必须足以维持前向血流;(2)Pcc 必须显著高于下游毛细血管压,以推动血流通过。由于毛细血管具有较大的横截面积且血流缓慢,其下游阻力很小,主要来源于静脉端压力。尽管 Pcc 在不同组织中有所不同,但由于引流静脉具有高容积和大横截面积,且血流缓慢,因此静脉回流端的压力相对恒定。
这种回流压力被称为平均系统充盈压(Pmsf),是指血流突然停止并重新分布后系统内的压力,可估算驱动静脉回流的上游压力,亦可反映循环容量的充盈程度。正常情况下,Pmsf 较低(≤10 mmHg),而静息状态下的 Pcc 较高(约 45 mmHg),在代谢需求升高时会下降。这种差异构成了动脉入流端(Pcc)与毛细血管之间的“血管瀑布”现象。
Pmsf 受静脉血管张力、组织间压和血容量的共同影响。临床上已有床旁估算 Pmsf 的方法,智能手机应用 iGuyton 亦可通过人口学参数、心输出量、MAP 及右心房压(Pra)估算 Pmsf 及静脉回流参数。静脉回流的压力梯度为 Pmsf–Pra。图2展示了这些概念及其在循环调控中的作用。
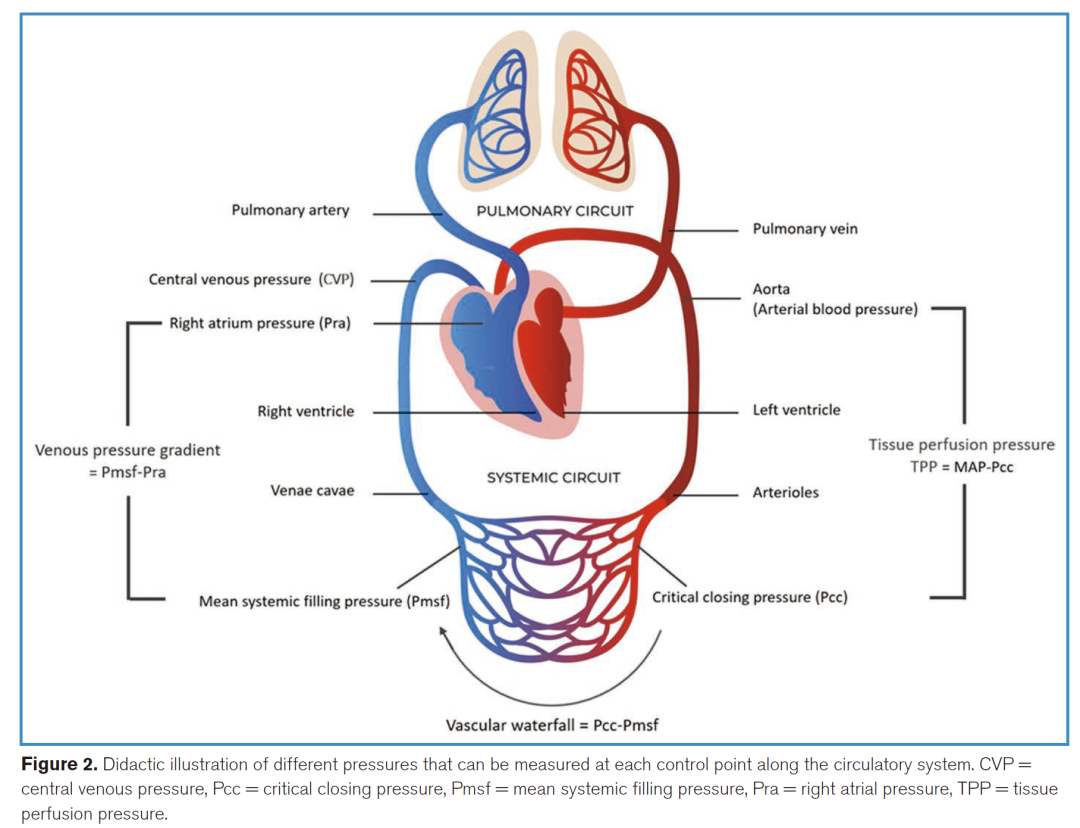
“血管瀑布”有助于保护毛细血管免受高压和水肿影响。然而,当代谢需求升高时,Pcc 降低,毛细血管压力上升,从而促进液体向组织间隙转移。在运动过程中,局部 Pcc 降低,导致组织间水肿,这种“肌肉充盈感”即为表现。虽然不同组织具有各自特异的 Pcc 值,但也可通过呼吸或窦性停搏期间的全身血压变化推测全身性 Pcc 值。MAP、SAP、DAP、Pcc 与 Pmsf 均可通过无创或微创手段在床旁估算,为临床医生提供更准确的血流动力学视角。
脓毒症、动脉压与自我调节
脓毒性休克可通过削弱血管内皮与平滑肌之间的反馈调节,诱发全身性血管麻痹(vasoplegia),导致 Pcc 与 Pmsf 同时下降,但因两者机制不同,Pcc 降幅更显著。临床上,Pcc 可能降至接近 Pmsf 的水平,提示自我调节功能的丧失。尽管复苏措施可提升 MAP 与 CO,但血流分布趋于均匀,反而导致代谢活跃组织灌注不足、代谢不活跃组织灌注过多。
这种状态被称为高动力低血压(hyperdynamic hypotension):表现为低 MAP 与 DAP,但 CO、HR、混合静脉血氧饱和度升高,同时伴有高乳酸血症与器官功能障碍。若 DAP 小于 40 mmHg,通常提示血管麻痹,因为正常 Pcc 值高于此水平。
在脓毒症进展过程中,全身性炎症可能诱导细胞内代谢改变,即使 TPP 与血管瀑布恢复正常,这些代谢紊乱仍可能持续。此时,临床医生可能面对这样一种情形:MAP 与 CO 已恢复正常,但器官功能仍未改善。此时,测量 TPP、Pcc 以及血管瀑布的存在与否,或可为下一步治疗提供指导——若灌注不足,可继续强化复苏;若灌注指标已充分,则应避免进一步使用液体或血管活性药物,以免带来潜在危害。不过,该策略尚未在临床试验中得到验证。
高级动脉压指标
心室-动脉耦合(Ventriculo-Arterial Coupling, VAC)
左心室将搏出量(SV)射入已加压的动脉系统中。SV产生前向血流,但动脉压作为后负荷会限制输出。随着阻抗增加,SV会下降,这取决于终末收缩弹性(反映固有心肌收缩力)与动脉弹性之间的平衡关系。这种关系被称为心室-动脉耦合(VAC),如图3所示。
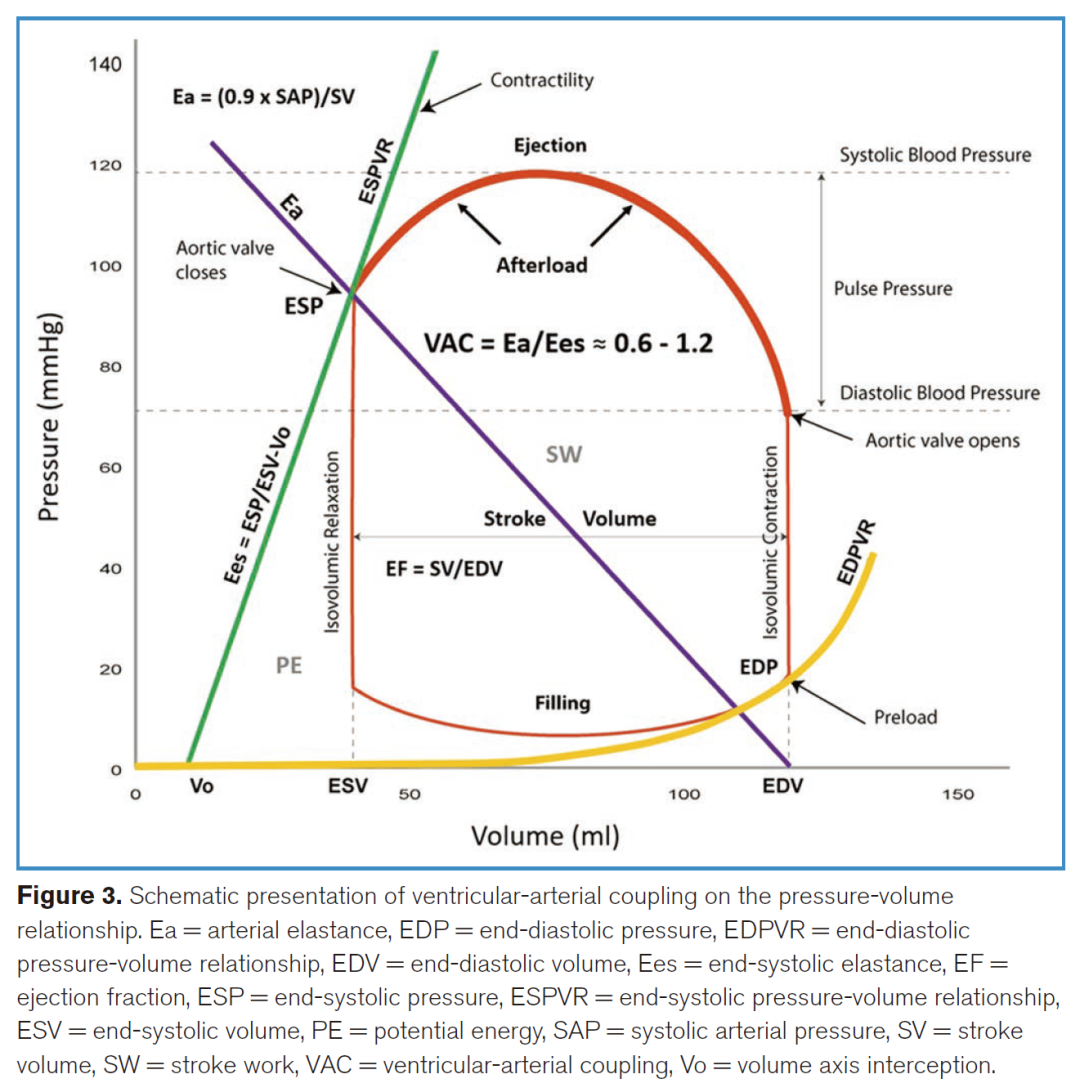
最佳的VAC比值接近1,表示心肌收缩力与动脉负荷匹配,可在低能耗下维持自主调节。动脉弹性可估算为(SAP × 0.9) ÷ SV(假设心率恒定)。
脓毒症通过血管麻痹降低动脉弹性。因此,在相同的收缩力和舒张末期容积条件下,SV会升高,而SAP保持不变或降低。脓毒症亦可能损害收缩力,但在早期高动力性脓毒性休克中,这种收缩力减弱通常不易察觉,因为低动脉弹性掩盖了其表现。此时使用血管活性药物提升动脉弹性可揭示潜在的心功能不全,表现为心输出量下降。
免费手机应用 iElastance 可通过输入SAP、DAP、射血分数(EF)、搏出量(SV)、射血前时间和射血时间,估算终末收缩弹性、动脉弹性和VAC。
动态动脉弹性(Dynamic Arterial Elastance, Eadyn)
左心室搏出量的变化会引起脉压(PP)的成比例变化。此关系依赖于中心动脉顺应性,称为动态动脉弹性(Eadyn)。Eadyn 的计算公式为:脉压变异度(PPV) ÷ 搏出量变异度(SVV),其测量基于自主呼吸或正压通气状态。
Eadyn 与VAC相关,但其主要用于评估当心输出量或使用血管活性药物变化时,MAP 的变化趋势。
在低血压且容量反应性良好的患者中,液体负荷可增加CO,但MAP 可能并不随之上升。这在脓毒性休克中较为常见,因其动脉弹性低。若液体负荷前的Eadyn小于1,则MAP通常仅有轻微提升。此类患者更适合使用血管活性药物,以缩短低血压持续时间并减少液体用量。
相反,对于已使用血管活性药物的血管麻痹患者,临床上常面临是否仍需维持支持的问题。目前的做法是尝试减量观察MAP变化,若MAP下降则判断为对血管活性药物依赖。然而,这种“试探性撤除”可能诱发低血压并加重器官损伤。
研究发现,若Eadyn > 1.1,则停用血管活性药物很少导致低血压,从而使得在病情稳定的患者中能更安全、更迅速地撤除循环支持。
动脉压各组成部分的临床相关性
收缩压(SAP)
左心室收缩将血液射入主动脉,升高中心动脉压。这一升高发生在心脏射血期,因此收缩压是评估左心室功能的指标之一。动脉僵硬性或弹性(即动脉弹性)是影响收缩压的次要决定因素。此外,血管分支点的反向压力波还会进一步升高外周收缩压(pSAP)(图4)。在临床上,收缩压可通过血压计快速测量,是急诊中定义低血压的常用初筛指标。
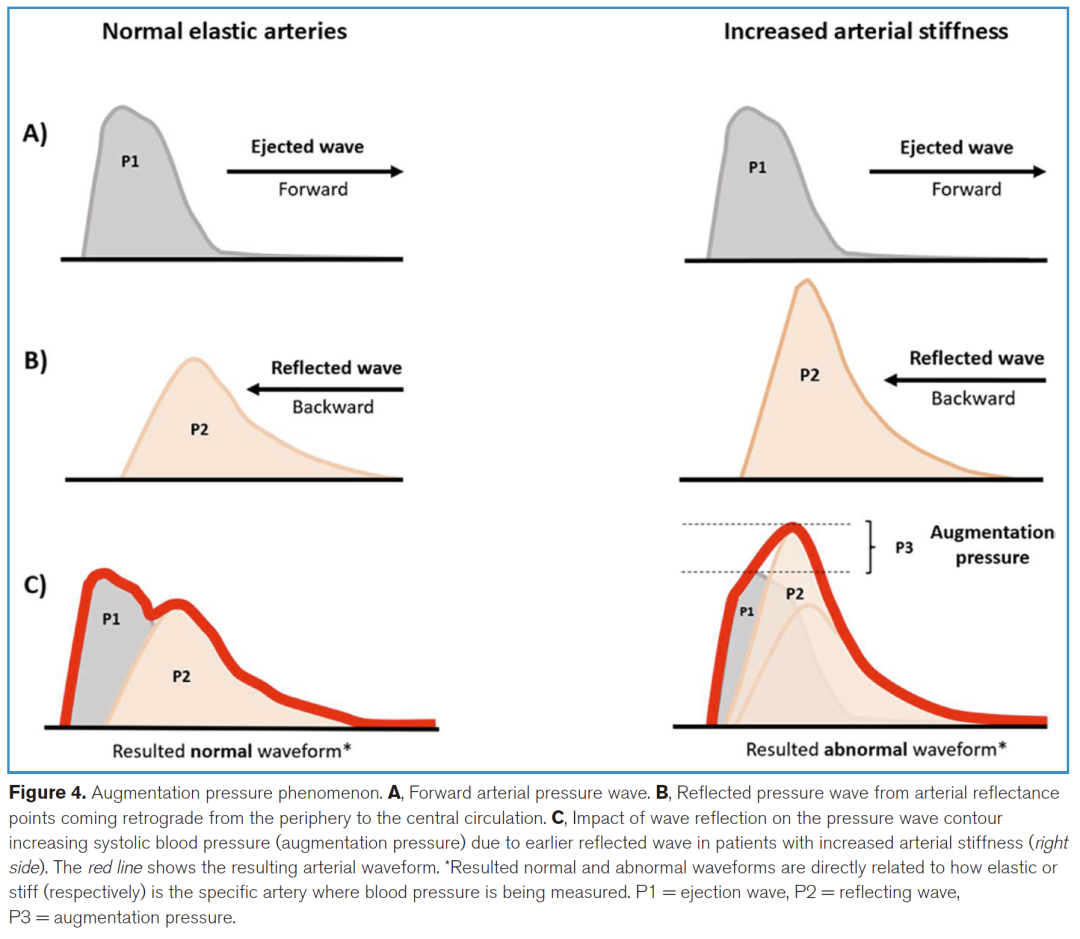
收缩压≤100 mm Hg 是脓毒症的早期体征之一,但同样也见于心源性、低容量性和阻塞性休克。因此,收缩压降低是循环衰竭的非特异性标志。关于收缩压预后价值的研究结果不一,但较高的收缩压通常与更好的结局相关。若收缩压波动显著且不规律,则提示更高的死亡风险,并更可能与容量不足有关,而非单纯需要血管活性药物。
平均动脉压(MAP)
平均动脉压是一个心动周期中动脉压的平均值,通常估算为舒张压加上1/3的脉压。正常MAP范围为70–110 mm Hg。在脓毒性休克中,65 mm Hg被认为是维持终末器官灌注的最低初始目标,或对于慢性高血压患者不低于基线的15%。由于MAP仅代表“输入压”,因此在静脉压或腹内压升高时,可能需要更高的MAP才能维持组织灌注。真正决定组织血流的是组织灌注压(TPP),而非单一MAP。
MAP反映整个心动周期的压力,其中舒张压的影响较大,因为心脏在舒张期所占时间更长。
舒张压(DAP)
舒张压是一个心动周期中最低的动脉压,受舒张末期动脉残余血容量、血管紧张度和临界闭合压(Pcc)共同影响。舒张期时间影响残余血容量,而心动过速会缩短舒张期,在相同搏出量下使舒张压升高。对于脓毒症或合并慢性高血压的患者,维持舒张压在54–62 mm Hg之间可能更有利于器官灌注。
冠状动脉向左心室供血主要发生在舒张期,因为收缩期心肌压迫冠脉。因此,舒张压是左心室灌注的输入压。当DAP低于40 mm Hg时,可能出现心肌缺血。舒张压<40 mm Hg通常与血管张力下降有关,尤其在心动过速时更为明显。有研究指出,脓毒性休克患者的最佳舒张压和心率范围分别为50–70 mm Hg和60–90次/分。若DAP≤40 mm Hg且HR≥100次/分,则预示更高的死亡风险。
研究还显示,DAP<52 mm Hg可预测96小时内脓毒性休克的早期进展。DAP越低,血管麻痹越严重,预后也越差。另有研究发现,在复苏后24小时,若DAP<59 mm Hg,则与28天死亡率升高相关,因此建议在MAP达标(≥65 mm Hg)后,进一步维持DAP≥59 mm Hg可能改善预后。目前该策略正在多中心随机对照试验(ANDROMEDA-SHOCK-2)中进行验证。
即便MAP>65 mm Hg,低DAP仍与90天高死亡率相关。此外,在MAP恢复正常后,微循环功能障碍常常仍然存在。有研究发现,在脓毒症中,DAP是组织氧饱和恢复的唯一独立预测因子。
脉压(Pulse Pressure, PP)
脉压是收缩压与舒张压之间的差值,可无创反映搏出量与血管紧张度的关系。在脓毒症中,低脉压与更高的死亡率相关。脉压受呼吸影响而变化,称为脉压变异度(PPV),在机械通气患者中,PPV≥13%对容量反应性具有较高的敏感性(85–89%)和特异性(88–98%)。
多种呼吸操作可通过PPV评估容量反应性。PPV是床旁评估脓毒症患者血容量扩充效果的简单工具。
心率对动脉压的影响
心率对动脉压有重要影响,主要通过其对舒张期时间的影响体现。心动过速会缩短舒张期,减少动脉排空时间,在相同搏出量下导致舒张压升高。这种升高可掩盖潜在的血管麻痹状态,因为舒张压的升高并非由于血管紧张度增强,而是由于舒张期时间缩短所致(图5)。因此,在重症患者中,反射性心动过速可能造成血管张力正常的假象。
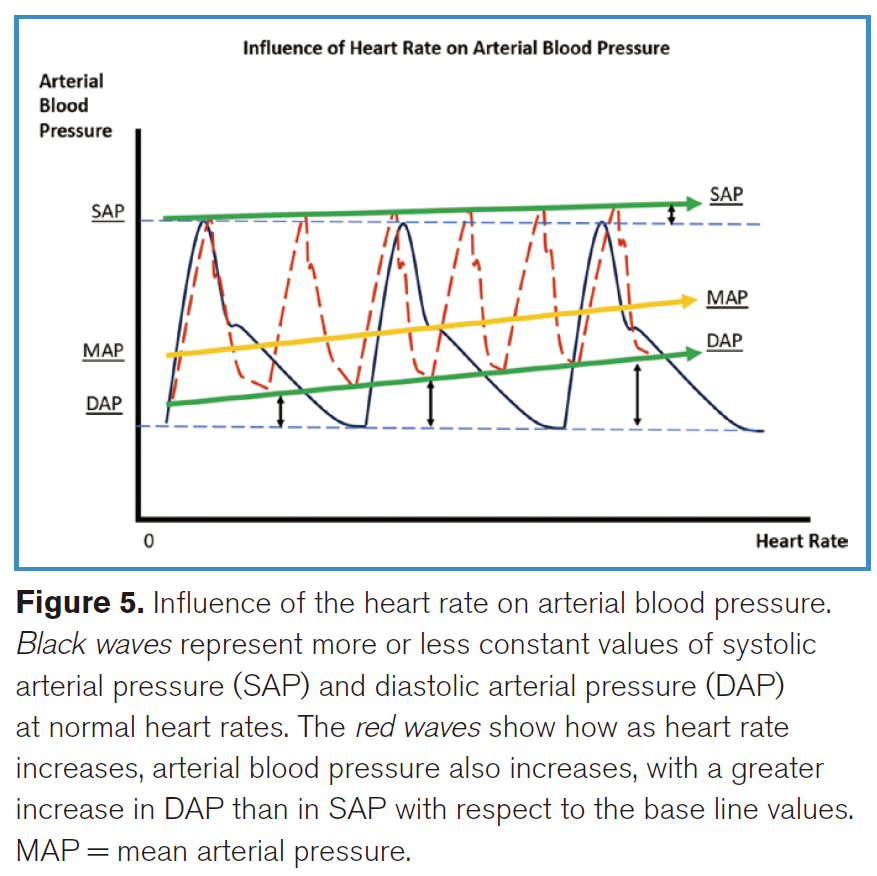
研究发现,在不改变心输出量的情况下,通过人工起搏逐步升高心率会导致搏出量下降,但仍可观察到SAP、DAP与MAP的升高。有趣的是,尽管中心DAP随着心率增加而上升,中心SAP(cSAP)并未表现出相同趋势,可能是由于反射波到达时序不同。这一发现凸显了心率与动脉压各组分之间复杂的相互作用。
一个整合心率与舒张压的临床相关指标是舒张性休克指数(Diastolic Shock Index, DSI),定义为心率除以舒张压。研究表明,DSI>2.2的患者在脓毒性休克中死亡风险显著增加。其关系为:在心率恒定时,DAP越低死亡率越高;在DAP恒定时,HR越高死亡率越高。值得注意的是,在该临床情境下,HR与DAP均为死亡率的独立预测因子。
床旁动脉压监测
尽管在危重症患者中常常使用有创动脉血压(ABP)监测,但目前的证据并不完全支持其常规使用。这主要是因为仅进行血压测量,而未将其用于指导靶向干预,并不能必然改善临床结局。Kaufmann 等人比较了有创与无创方式测得的 SAP、MAP 和 DAP,包括接受去甲肾上腺素输注的患者,结果显示两者之间无显著差异。
然而,Kim 等人进行的一项荟萃分析得出结论:连续无创动脉血压监测在患者出现低血压时,其准确性和精密度往往超出可接受范围。特别是在计算 舒张性休克指数(DSI) 或对低血压患者进行关键决策时,这些偏差尤为重要。因此,根据主流重症医学指南,在血流动力学不稳定的患者中,有创动脉监测仍为推荐的标准方法。
在血管收缩状态下,外周动脉血压读数可能不可靠。Kim 等人研究发现,对于使用去甲肾上腺素≥0.1 μg/kg/min 维持 MAP ≥65 mm Hg 的患者,桡动脉压力有 62.2% 的情况会比股动脉压力低 ≥5 mm Hg。Wisanusattra 和 Khwannimit 的报告也发现了类似的结果。
这种差异的原因在于,由于反射压力波的放大作用,外周收缩压(pSAP)通常高于中心收缩压(cSAP)。因此,pSAP 并不是评估中心血流动力学或心血管风险的可靠替代指标。为此,Chemla 等人提出通过以下公式,用外周 MAP 和 DAP 来估算 cSAP,从而避免依赖可能具有误导性的 pSAP 值:
cSAP = MAP² / DAP
需要特别指出的是,与有创测量相比,无创方法通常高估 DAP 平均约 6 mm Hg,低估 SAP 同样约 6 mm Hg。在血管麻痹状态下,由于反射波减弱,外周测量的动脉压与中心动脉压之间的偏差会更加显著。
组织灌注压(Tissue Perfusion Pressure, TPP)
组织灌注压(TPP)定义为 MAP 与动脉临界闭合压(Pcc)之间的差值,反映了驱动组织血流的压力梯度。由于 Pcc 通常高于平均系统充盈压(Pmsf),因此局部血管扩张(可降低 Pcc)能够增强组织灌注。这正是机体通过自主调节机制,将局部血流与代谢需求相匹配的主要方式。
然而,在血管麻痹状态下,Pcc 可能降至接近 Pmsf 的水平,从而削弱这一自主调节机制。在这种情况下,即使 MAP 增加,灌注也未必改善。
研究显示,TPP>34 mm Hg 与心脏外科患者乳酸清除改善和微循环调节改善相关。Andrei 等人观察到,在术后血管麻痹的患者中,复苏前的 Pcc–Pmsf 梯度小于 5 mm Hg。在使用去甲肾上腺素将 MAP 提高至 80 mm Hg 以上后,只有一半患者 Pcc 出现升高,重新建立了动脉“血管瀑布”现象(即 Pcc ≫ Pmsf)。
而这些 Pcc 升高的患者在灌注方面表现更佳,包括:乳酸清除改善,二氧化碳分压差(ΔPco₂)降低,舌下微循环血流改善,毛细血管再充盈时间(CRT)更快。
PCC 与 PMSF 的床旁测量
目前已开发出多种床旁技术用于估算动脉临界闭合压(Pcc)与平均系统充盈压(Pmsf)。
Pcc
每个血管床都有其特异性的 Pcc,会随代谢需求而变化。然而,可通过快速阻断外周动脉导管的方法在床旁估算总体 Pcc;动脉压力在 10–12 秒内的初始衰减呈对数衰减模式,可近似代表 Pcc。
上臂袖带法测量 Pmsf
通过将上臂袖带快速充气至收缩压以上 50 mm Hg,可瞬间使动脉与静脉压力达到平衡,从而反映 Pmsf。推荐使用快速充气设备(0.3 秒)或气动止血带(1.4 秒)。在许多情况下,仅需测量动脉压至其趋于稳定(约 18–20 秒)即可完成估算。此法适用于清醒患者、接受机械通气的患者或存在心律不齐者。
类比计算法估算 Pmsf
该方法基于 Guyton 模型中的关系式:
心输出量(CO)= 静脉回流(VR) = (Pmsf – 中心静脉压 CVP)/ 静脉回流阻力(RVR)
类比公式为:
Pmsf = a × CVP + b × MAP + c × CO,且 a + b = 1,其中 a = 0.96,b = 0.04。
这些常数源自静脉与动脉顺应性的经验数据。若已知 CO、MAP 与右心房压(Pra),可使用智能手机应用程序 iGuyton 自动完成计算。
吸气平台法测量 Pmsf
该方法最为传统,需进行短暂吸气平台保持(2–10 cm H₂O,持续 6–10 秒),绘制 Pra 与 CO 的关系图。图中零流量交点即代表 Pmsf。此法仅适用于接受机械通气、无自主呼吸或心律不齐的患者。
表1. 临界闭合压与平均系统充盈压的床边测量方法
Pcc(临界闭合压)床边测量
|
|
|
|
| Pcc |
|
|
Pmsf(平均系统充盈压)床边测量
|
|
|
|
| Pmsf臂测法 |
|
自主呼吸或机械通气 窦性或心律失常患者 |
| Pmsf类比法 |
|
自主呼吸或机械通气 窦性或心律失常患者 |
| Pmsf吸气屏气法 |
|
无心律失常 |
动脉血压与宏-微循环耦合
宏-微循环耦合(亦称血流动力学一致性)指的是:当系统性宏循环变量(如 MAP 与 CO)改善时,微循环血流同步改善,从而逆转组织低灌注状态。
然而,在脓毒性休克中,达成宏循环目标并不总能实现足够的组织灌注以满足代谢需求。MAP 升高是否能改善微循环灌注存在较大差异,关键取决于两个因素:
-
1. 系统性组织灌注压(TPP)是否达到最低阈值; -
2. 动脉临界闭合压(Pcc)与平均系统充盈压(Pmsf)之间是否存在“血管瀑布”,即当 Pcc 降低时血流得以增加。
床旁评估微循环血流极具挑战性。研究发现,当低血压脓毒性休克患者的 MAP 被升高至 80–85 mm Hg 时,微循环血流的反应表现出高度异质性:
-
• 微循环灌注初始较差的患者往往在 MAP 升高后出现改善; -
• 基线灌注正常者则无改善,甚至血流减少。
在部分患者中,毛细血管再充盈时间(CRT)作为微循环灌注指标,在升高 MAP 后可增可减,在不同个体中表现不同。此外,若组织已进入“细胞衰竭”状态,即便血流恢复,也可能无法改善功能。
若灌注压正常但器官功能持续障碍,则提示有其他机制参与,单纯提升 MAP 并不能带来功能改善。
ANDROMEDA-SHOCK 研究引入了一项测试方法:通过观察 CRT 对 MAP 改变的反应,评估宏-微循环耦合程度。如果 CRT 在 MAP 升高后改善,提示该 MAP 水平具有治疗意义;相反,如果增加去甲肾上腺素剂量导致组织灌注恶化,表明应重新考虑 MAP 的设定目标。
优化宏循环变量只是脓毒性休克管理的第一步。尽管 MAP 与血流直接相关,但其正常化并不总能改善微循环状况。通常,MAP 超过 65 mm Hg 可提高 TPP,从而可能改善组织灌注,尤其当 Pcc 显著高于 Pmsf 时更是如此。
当患者对液体有反应时,可通过补液升高 MAP。然而,如果补液不能升高 MAP 或改善 Pcc,应及时启动血管活性药物。
若已实现以下目标:
-
• MAP 超过 65 mm Hg; -
• TPP 大于 35 mm Hg; -
• Pcc 与 Pmsf 的差值超过 10 mm Hg,
但仍存在低灌注现象,则进一步补液或使用升压药可能无益,甚至增加并发症风险。
然而,这些假设尚需通过前瞻性临床试验验证后,方可成为标准治疗策略。
结论
动脉血压与脓毒性休克预后的关系复杂且具有异质性。聚焦关键参数——如组织灌注压、血管瀑布效应以及个体化治疗反应——有助于形成以灌注为导向、而非单纯以压力为导向的个体化治疗路径。当宏循环参数达标而组织灌注依然不足时,应转向微循环评估,以指导下一步治疗并避免盲目加重补液或使用升压药。床旁评估收缩压(SAP)、平均动脉压(MAP)、舒张压(DAP)、Pcc 及 Pmsf,可为治疗方案的制定与调整提供实用工具。未来仍需高质量临床研究验证这些参数的可行性与有效性,并优化脓毒性休克的复苏策略。
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫