重症医学中的肺内分流:结合临床情境的实用方法

摘要
背景
肺内分流是指静脉血绕过肺泡—血气交换进入动脉血系统的过程。肺内分流的定义是肺通气与肺灌注生理耦合的下降,这可能会导致呼吸衰竭。
正文
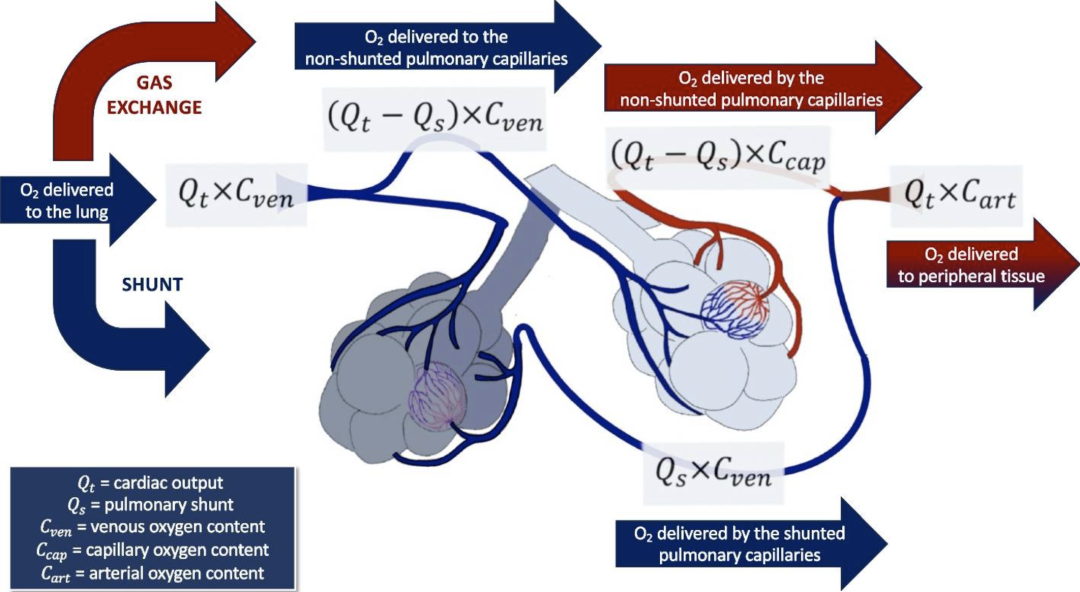
肺内分流的评估常常被忽视。从数学角度看,肺内分流可以通过估算含氧血与缺氧血混合的程度来进行评估。计算肺内分流时需分析三个关键组成部分:气体交换前中心静脉血中的氧含量(O₂)、气体交换后肺毛细血管中计算得到的氧含量,以及分流血与非分流血混合后动脉系统中的氧含量。在接受体外膜肺氧合(ECMO)的患者中,肺内分流计算尤为重要,因为动脉氧水平可能并不能直接反映原生肺的气体交换情况。
结论
本综述通过一个在线分流模拟器,讨论了肺内分流分析及其在不同临床情境中的实际应用。
我眼瞎,在文章里没找到这个所谓的online shunt simulator到底在哪里,其实微信小程序上也有计算工具

背景
肺内分流被定义为去氧血进入动脉血系统,从而在功能上或解剖学上绕过肺泡-毛细血管水平的气体交换。肺内分流的程度与低氧血症的严重程度相关,其变化与疾病的进程密切相关。
气体交换的评估通常局限于动脉血气分析(BGA),而肺内分流的测量并不常被视为标准实践。然而,动脉血氧含量可能会受到中心静脉血氧饱和度变化的显著影响,而这种变化可能出现在特定临床情境中。例如,心输出量下降可显著降低SvO₂,而接受体外膜肺氧合(ECMO)的患者则表现出非常高的静脉血氧含量。肺内分流的定量与解读有助于评估疾病严重程度、持续监测肺损伤进展以及评估治疗反应的演变轨迹。
在本综述中,我们从1802年Gay-Lussac在其题为《气体与蒸汽膨胀的研究》的手稿中所阐述的物理概念出发,回顾了上世纪后半叶West与Riley的生理学研究成果,最终延伸至近期提出的数学模型与计算工具,对肺内分流的计算进行了全面探讨,并逐一解读各公式变量的含义。
此外,我们还提供了一些临床实例,旨在强调该分析在应对不同心肺衰竭情境时对临床医生的潜在价值,并利用先进的在线分流模拟器进行说明。
关于分流对二氧化碳清除复杂效应的讨论超出了本文的范围,因此不作阐述。
定义:分流、通气/血流比失调与死腔
分流、通气/血流比(V/Q)失调和死腔是指肺通气与灌注的特定异常。
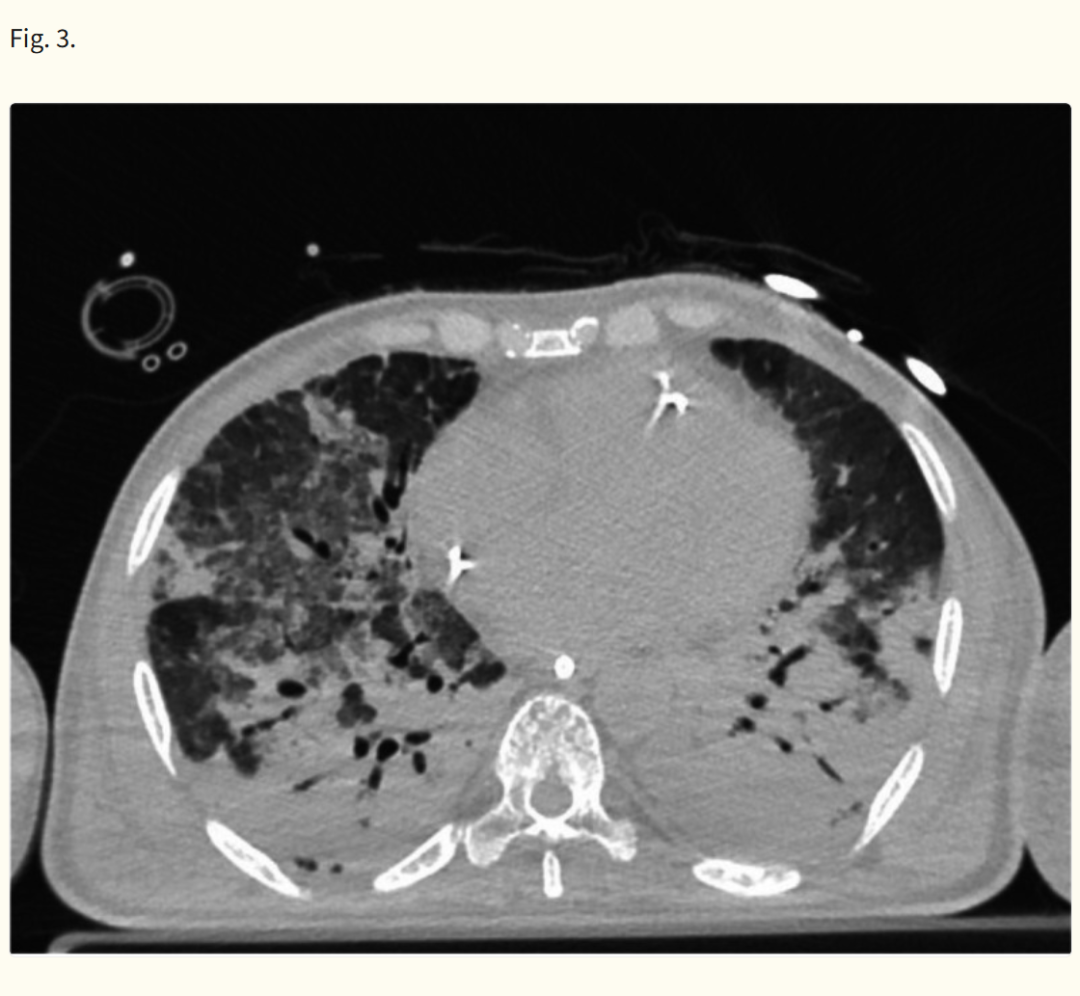
分流,如上所述,指的是肺部某些区域存在血流灌注但无通气,导致血液中的氧含量下降。分流常见于ARDS患者,这类患者在计算机断层扫描(CT)上通常表现为广泛的实变。从病理生理学角度来看,功能残气量(FRC)显著减少;这一减少可通过应用PEEP有效治疗,以恢复呼气末肺容量(EELV)。
V/Q失调是通气与血流之间的不匹配。这一比值可以偏低(类分流型),也可以偏高(类死腔型)。类分流型失调是由于相对于血流灌注通气减少所致,从而导致氧合下降。类死腔型失调发生在通气超过血流灌注时,导致二氧化碳清除不足。
死腔是指呼吸系统中不参与气体交换的区域。总死腔(又称生理性死腔)是气道死腔和肺泡死腔的总和。前者为生理性,而后者则出现在肺泡有通气但无灌注的病理状态下,例如肺栓塞。
总之,分流、V/Q失调和死腔是相互关联的概念,分别描述了肺气体交换受损的不同方面。理解这些原理对于呼吸系统疾病的诊断与治疗至关重要。
本综述主要聚焦于分流计算的应用及其在不同危重症场景中床旁使用的价值。
血氧含量
血氧含量()可定义为每分升血液中所含的氧气体积(以 O₂ mL/dL 表示)。在血液中,氧气主要与血红蛋白结合,仅有一小部分以溶解形式存在。血液中所含氧气的数量与血红蛋白浓度及其氧饱和度(),以及氧分压()成正比,其表达式如下:
其中, 为血红蛋白浓度(g/dL), 为血红蛋白饱和度(以比值表示), 与 分别为每克血红蛋白所结合的氧气量系数和氧气溶解系数。
根据查理定律(等压,即恒压条件下),气体所占体积可计算如下:
其中, 为完全解离 1 g 血红蛋白释放的氧气体积, 为气体物质的量(mol), 为大气压(1 atm), 为绝对温度(37 ℃ = 310.15 K), 为通用气体常数()。
完全结合 O₂ 的血红蛋白 1 mol 可结合 4 mol 氧气;1 g 血红蛋白相当于 mol(分子量 68,000 KDa)。由此可得,1 g 血红蛋白可结合 mol 氧气()。
将这些数值代入公式 2,可计算出 1 g 血红蛋白在完全解离后释放的氧气体积如下:
由于氧气并非理想气体,因此需要一个修正因子()以校正气体的可压缩性。
因此,1 g 血红蛋白解离所释放的实际氧气体积如下:
在海平面时,大气压恒定,但人体温度可在 28 ℃(301.15 K,严重低体温)至 42 ℃(315.15 K,严重高体温)之间变化。为了准确计算氧气体积,必须考虑患者的体温(见表 1)。
表 1.不同体温下 1 g 血红蛋白完全解离所释放的氧气体积
|
|
|
|
|
|---|---|---|---|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
基于公式 1, 最终可以计算为:
根据表 1,在 37 ℃ 时,1 g 血红蛋白完全解离所释放的氧气体积为 1.363 mL。在发热时可升高至 1.385 mL;相反,在严重低体温时可下降至 1.323 mL。举例而言,在一位 、、 的患者中,当温度从 37 ℃ 升高至 40 ℃ 时, 的增加量为 0.2 mL/dL。
需要强调的是,在计算 时必须考虑高铁血红蛋白(MetHb)和碳氧血红蛋白(COHb)的存在。大多数血气分析仪会在修正 MetHb 和 COHb 后,报告血红蛋白氧饱和度,记作 “HbO₂”。在可行的情况下,HbO₂ 应优先于 使用(见公式 5)。
肺内分流(Pulmonary shunt)
肺内分流的计算基于对三个部位 的分析:
静脉氧含量
在每一分钟,特定量的静脉血会从心脏右侧被泵入肺循环(),携带一定量的氧气()。输送至肺部的氧气可按如下公式计算:
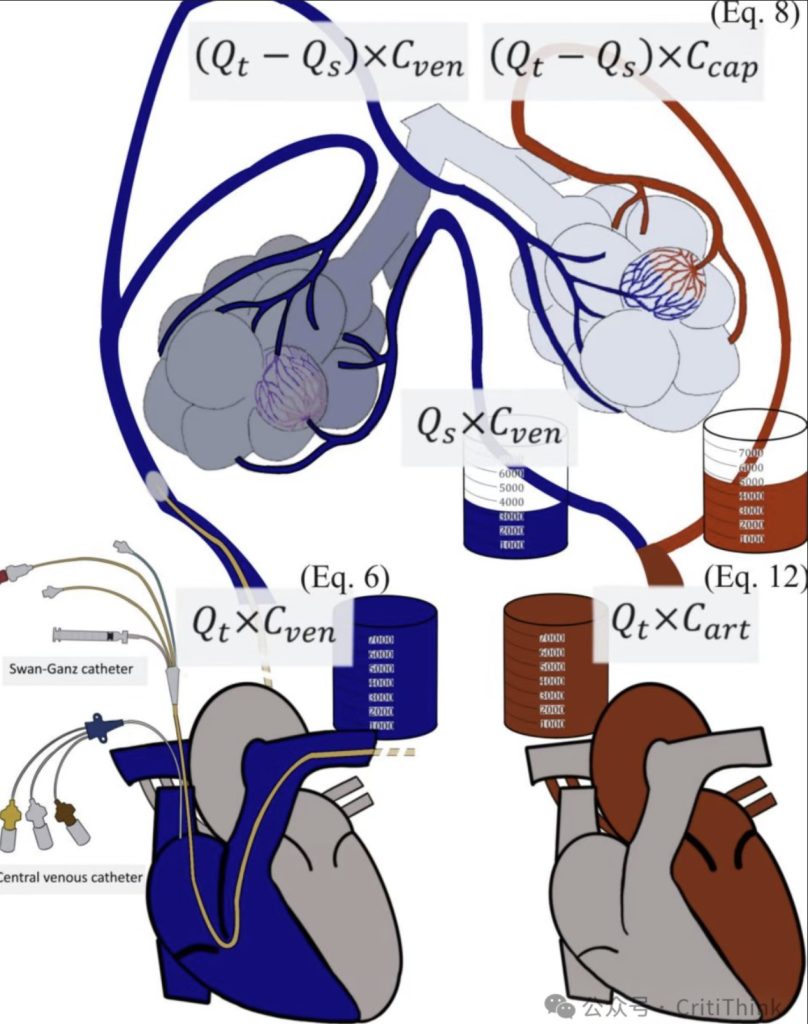
为计算 ,血气分析(BGA)标本可以取自两个部位:通过中心静脉置管采集右心房血,或通过 Swan-Ganz 导管采集肺动脉血(图 1)。这两个部位的氧含量通常相似,但肺动脉中的氧含量往往比右心房稍低。这是由于冠状窦和前心静脉带入心脏的血液含氧量极低。研究表明,混合静脉氧饱和度()可作为估算动脉混合静脉氧饱和度()的一种可靠且风险较低的替代方法,同时仍具有较高的准确性。通过 Swan-Ganz 导管获得的数值可能比中心静脉置管更准确,因为中心静脉标本可能过近(例如来自上腔静脉,氧含量较高)或过远(例如接近冠状窦出口,氧含量较低)。因此,建议在同一患者进行多次采样时,同时使用中心静脉和 Swan-Ganz 导管采样,并参考相同的采样部位。
基于公式 5, 的计算公式为:
其中, 为血红蛋白氧饱和度, 为右心房和/或肺动脉的氧分压。
毛细血管氧含量
非分流血流可通过将心输出量()减去分流分数()来计算。肺毛细血管内的氧输送总量由 与非分流血流的乘积决定(图 1):
其中, 为肺毛细血管在气体交换后、进入左心和体循环之前的氧浓度。
显然,不可能直接在毛细血管中采血。因此,毛细血管氧饱和度()需要通过血红蛋白解离曲线推导,已知毛细血管氧分压()(图 2)。

假设在肺泡-血液氧气梯度为零的平衡状态下,毛细血管中的氧分压()等于肺泡氧分压:
其中, 为大气压(海平面为 760 mmHg), 为水蒸气分压(参考值 47 mmHg), 为吸入氧浓度, 为动脉二氧化碳分压, 为呼吸商。
呼吸商是一个无量纲数值,范围在 0.7 至 1.2 之间,定义为单位时间内产生的二氧化碳体积()与消耗的氧气体积之比。 是呼吸生理学中一个重要参数,用于评估代谢底物类型,并估算肺泡二氧化碳分压。在临床情况下,如果 、 以及相应的 无法直接测得,则可假定 。
基于 的假设,公式 5 可被改写以测定 :
如前所述, 不能直接测量,必须通过以下公式推导:
动脉氧含量
每分钟,左心室将一定量的血液泵送到外周组织,携带一定量的氧气 (见图 1)。输送到外周组织的氧气量可按如下公式计算:
基于公式 5, 的计算可表示为:
肺内分流计算
分流率的计算为未参与气体交换的血流量()与心输出量()的比值:
来源于含氧血与未含氧血(来自分流毛细血管)的混合,需考虑其相对血流量:
展开公式 15:
化简得到分流率的最终公式:
将公式 19 中的氧含量代入,最终得到:
动脉氧含量/饱和度依赖于两个因素。首先,它受灌注肺脏的静脉血氧饱和度影响;其次,它取决于肺脏气体交换的效率(分流率)。在分流率保持恒定的情况下,可以确认动脉血氧饱和度与静脉血氧饱和度呈线性相关。在低心排量综合征时,由于氧提取增加,静脉血氧饱和度下降,从而导致动脉血氧饱和度下降。相反,在接受静脉-静脉(V-V)ECMO 治疗的患者中,由于膜肺氧合对静脉血进行人工氧合,静脉血氧饱和度显著升高,因此即使在存在严重肺损伤的情况下,动脉血氧饱和度也会升高(见图3)。在这两种情况下,动脉血氧饱和度并不能准确反映呼吸衰竭的严重程度。在某些情况下,了解呼吸衰竭的严重程度更多依赖于计算分流率,而非分析动脉血氧饱和度。
肺内分流测量在临床实践中的应用
在本节中,描述了不同的临床情景,其中肺内分流的测量有助于患者的评估。
需要注意的是,任何对肺内分流的解读应仅限于对气体交换障碍类型的评估,而不应推断其具体病因。
病例 1:急性呼吸窘迫综合征(ARDS)
一名 55 岁男性因由 H1N1 流感导致的原发性 ARDS 入住 ICU。患者镇静并在容量控制通气下接受机械通气。
动脉血气分析(BGA)显示严重的低氧性呼吸衰竭(表2)。患者血流动力学稳定,未使用血管活性药物。静脉血气分析显示正常的 SvO₂:68.4%。为了估计呼吸衰竭的严重程度,可使用公式(Eq. 21)计算肺内分流,结果为 0.4(40%)。
表 2. 基线呼吸与血流动力学参数
|
|
|
|---|---|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
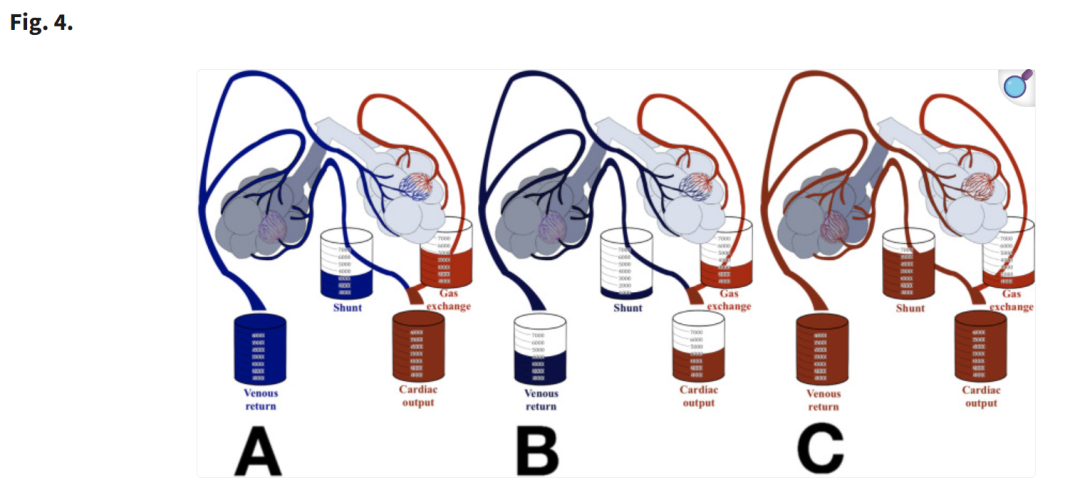
在这个病例,高度的分流伴随低呼吸系统顺应性,这是 ARDS 患者常见的情况 (图 4A)。
病例2:大叶性肺炎
一名75岁男性因大叶性肺炎入住ICU。患者在容量控制通气下进行镇静和机械通气(表3)。
表3.基础呼吸和血流动力学参数
|
|
|
|---|---|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
动脉血气分析(BGA)显示严重低氧血症(表3)。静脉血气分析显示 为46.1%,提示低心输出量状态。为了评估呼吸衰竭的严重程度,测得肺内分流为0.25(25%)。
与第一位患者相比,肺内分流较低,因为疾病仅局限于单个肺叶区域,但由于中心静脉血氧饱和度偏低,导致相同程度的动脉低氧血症(图4B)。
病例3:接受V-V ECMO的ARDS患者
一名45岁女性因H1N1流感导致的原发性ARDS入住ICU,并接受V-V ECMO支持。患者在容量控制通气下进行镇静和机械通气(表4)。
表4.基础呼吸及血流动力学与 ECMO 参数
|
|
|
|---|---|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
动脉血气分析(BGA)显示动脉氧水平较低(表4)。患者血流动力学稳定,无需血管加压药支持。静脉 BGA 显示较高的 SvO₂:86.7%。
为了评估呼吸衰竭的严重程度,计算得出的肺内分流为 0.8(80%)。尽管存在更高的肺内分流,但动脉氧含量与前两个病例相同。这是由于 V-V ECMO 的体外静脉血氧合。被分流的静脉血因此具有较高的氧含量,但确实导致严重的去饱和(图 4C)。需要指出的是,若无 ECMO,分流率达到 0.8(80%)将无法维持生命。
在 V-V ECMO 期间测量肺内分流时,推荐在患者整体通气(膜肺与天然肺)条件下使用相同的氧浓度。在呼吸机和膜肺上调整 FiO₂,以获得更一致的分流测量,尤其是在一段时间内重复检测时。这可能涉及同时重设呼吸机和扫气中的 FiO₂。FiO₂ 改变后必须经过足够时间,以达到新的稳态,再进行分流计算。
天然肺的分时通气量和膜肺的气体流量不会影响肺内分流的测量。高浓度吸入氧被认为适合估算不均一肺泡的“真实分流”比例,因为高 FiO₂ 可以削弱低氧性血管收缩的作用。肺内分流始终会被轻度高估,这是由于生理性分流(如 Thebesian 静脉和支气管循环的右向左分流)有微小的恒定贡献。为了保持一致性并便于在同一患者内比较分流程度,可以将 FiO₂ 统一设定为 1.0。
在详细讨论 V-V ECMO 下的肺内分流测量后,有必要深入探讨静-动脉(V-A)ECMO 下的氧合动力学,从而揭示体外循环与天然循环之间的复杂相互作用。
在 V-A ECMO 期间,患者动脉血氧含量来自两个来源:体外循环和左心室(即通过肺的血液)。因此,在股-股 V-A ECMO 中,来自股动脉的体外循环氧合血流进入主动脉,在此与左心室射出的血液混合。后者的氧合完全依赖于天然肺功能。该混合点的确切位置取决于体外血流量与本身心输出量之间的关系:心输出量越低,混合点越靠近主动脉根部。这解释了在 V-A ECMO 监测中使用右桡动脉动脉血气测量 PaO₂ 的关键作用。虽然可以在 ECMO 回路出口直接检测体外氧合血,但右桡动脉因最靠近心脏、最远离氧合器,其血气值受天然肺功能显著影响,特别是在心输出量较低时。
在原发心功能严重受损的情况下,这种情况常见于 V-A ECMO 运行的初始阶段,体外氧合可能会影响所有主动脉弓以上分支血管(尤其是左侧)的血氧含量。因此,患者常常表现为较高的动脉 PaO₂,反映了来自氧合器的血液氧分压水平升高。由于这种动态,从右桡动脉或左桡动脉采集的血液氧合水平可能并不具有直接可比性。因此,在肺部疾病(如肺炎或 ARDS)存在的情况下,分流可能难以评估,因为动脉 PaO₂ 水平取决于 ECMO 动脉端的氧合程度和本身心输出量血液混合的比例。基于这一原因,即便 V-A ECMO 患者具有充分的心输出量,计算分流依然可能是一个潜在误导性的问题。
局限性
肺内分流计算比起单纯分析氧合(如 PaO₂/FiO₂ 和动脉血氧饱和度)更有价值,可用于评估呼吸衰竭的严重程度。然而,需要强调的是,分流计算模型基于两个假设。首先,由于毛细血管氧含量不可直接测量,其数值被假定等于肺泡中的氧含量。其次,假定毛细血管氧含量等于肺泡氧含量,这意味着认为肺泡-毛细血管膜气体交换效率是完美的。换句话说,整个分流计算是基于所有进入肺泡的氧气都完全通过肺泡-毛细血管膜的假设,而这一假设可能与实际气体交换的情况有所差异。此外,分流计算需要三次不同的动脉血气分析(BGA)以及复杂的计算,需耗费时间和资源。
未来方向
由于分流估算在临床上具有重要意义,并能为评估危重症呼吸衰竭患者的肺损伤严重程度提供关键信息,因此在床旁的未来研究方向可包括以下几个方面:
-
• 探索创伤更小的方法,如使用中线导管,这类方法显示出与更具侵入性的 Swan-Ganz 或中心静脉导管相当的准确性。这些手段未来可更广泛用于血液采样和分流计算。掌握采样部位的知识有助于临床医生正确解读所获得的数值。 -
• 将分流评估及其随治疗时间变化纳入预后算法(例如,机器学习)中,并结合其他气体交换参数(如 PaO₂/FiO₂)和机械通气参数(如驱动压)预测预后或临床结局。 -
• 考虑在日常临床中将分流计算作为肺损伤严重程度的常规评估方法,特别是在处理某些明确的综合征(如 ARDS)时。
结论
-
• 肺内分流是一种能够反映呼吸衰竭严重程度的生理变量。 -
• 肺内分流的计算涉及三个部位氧含量的测定:静脉血(通过 Swan-Ganz 导管采样,或在一定局限下通过中心静脉导管采样)、毛细血管血(基于肺泡气体方程估算)、以及动脉血(通过动脉导管采样)。 -
• 在某些临床情况下,动脉血气分析因静脉氧含量显著改变而产生偏倚,例如低心排状态或 V-V ECMO 支持,此时肺内分流分析尤为有价值。 -
• 本综述旨在向临床医生说明如何准确测量和正确解读分流方程,以及如何通过使用在线分流模拟器,在改变生理变量的同时评估不同的病例情境。
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫