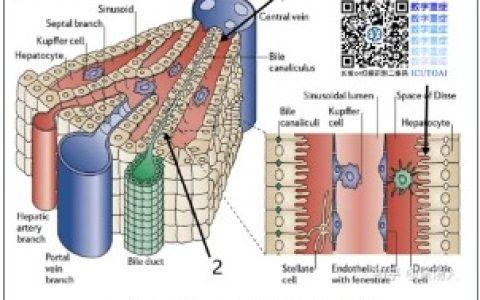
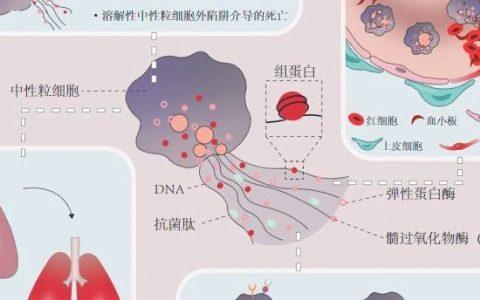
中国急诊社区获得性肺炎临床实践指南2015治疗篇
随着人口老龄化的加剧、免疫损害宿主的增加、病原体的变迁,尤其是病原体耐药率的快速增长和新型有效抗菌药物的研发减缓,急诊CAP的治疗面临众多新挑战。急诊CAP患者病情特点和基础状况等存在诸多差异,因此,需要急诊医师在治疗CAP过程中,针对每个患者给予个体化的综合治疗,这一点在重症感染的治疗中尤为重要。
一、急诊CAP规范治疗的原则
急诊CAP规范治疗的原则是指在了解患者基础条件及感染常见病原体的基础上,选择相应的抗感染治疗,重症患者同时进行免疫支持治疗或器官功能支持治疗。首先,不同基础状况患者对抗感染药物的治疗反应不同,对于急诊流水留观CAP患者,患者免疫功能通常未受到严重损害,因此,可针对常见病原体进行抗菌治疗;对于重症CAP(EICU住院患者),由于重症感染可能会导致机体过度的炎症反应即全身炎症反应综合症(SystemicInflammatory Response Syndrome,SIRS),进而可能引起机体产生代偿性抗炎反应综合征(CompensatoryAnti-inflammatory Response Syndrome, CARS),导致免疫紊乱,因此,除常规抗菌治疗方案外,需要对患者进行相应的免疫支持治疗;对于危重症CAP患者而言,患者可能会存在相关的器官功能障碍,因此,同时需考虑使用器官功能支持治疗。其次,应及时留取病原体培养标本,以便后期对抗菌药物进行调整。最后,在明确诊断CAP的过程中,尽早经验性使用抗菌药物会明显改善患者预后,使患者受益。
1. 早期识别重症CAP 重症CAP是一种严重、病死率高的感染性疾病,起源于肺部,可快速进展、进而出现呼吸衰竭,同时其并发的全身炎症反应综合征、多脏器功衰竭等可严重威胁患者的生命。因此,早期识别重症CAP对于及时治疗、改善预后至关重要。重症CAP的诊断标准见诊断篇。
2. 把握最佳治疗时机 对于急诊医生而言,仅仅正确认识重症CAP的严重程度还远不足,急诊医生治疗重症CAP有苛刻的时间限定。及时治疗可避免患者从局部感染最终走向多器官功能障碍衰竭(Multiple Organ Dysfunction Syndrome,MODS),甚至死亡。因此,要强调在器官功能衰竭/损伤前“抢先治疗”,努力降低器官功能不全的可能性和程度。因此,把握最佳治疗时机,制定合理抗感染治疗方案,是急诊治疗CAP的核心内容。关于急诊治疗社区呼吸道感染的抗菌治疗时间:及时地给予患者正确的起始治疗十分重要,延迟治疗可造成多种危害(病死率增加、住院日延长和总花费显著增高等)。一般推荐尽早给予抗菌治疗,且重症CAP患者需在1h内进行抗菌治疗。如我国成人《社区获得性肺炎诊断和治疗指南》指出:对于危及生命的重症肺炎,建议早期采用广谱强效的抗菌药物治疗,待病情稳定后可根据病原学进行针对性治疗,或降阶梯治疗。抗生素治疗要尽早开始,首剂抗菌药物治疗争取在诊断CAP后4h内使用。再如“挽救严重脓毒症运动“中特别强调,一旦正确诊断严重感染(包括重度CAP),应当在1h内选用广谱而强有力的抗生素治疗方案,依据药动学/药效学(PK/PD)原理,正确使用抗菌药物。但近年来随着细菌耐药问题的日益严峻,过度强调起始时间使医生在明确诊断之前匆忙使用抗菌药物,会造成过度使用,加重耐药发生并使患者承担相应的药物不良反应的风险。因此,对CAP不再界定具体的用药时间窗,强调基于诊断和病情,尽早给予抗菌药物。
3. 建立整体治疗观念 重症CAP治疗时应遵循“整体、平衡、个体化”原则。所谓整体治疗是指根据抗感染治疗的三要素“人-菌-药”制定抗感染治疗方案。患者是一个整体,抗菌治疗不是唯一的治疗方案,患者免疫状况、营养情况、咳痰和引流是否通畅等对于整体治疗均十分重要。另外,不同患者间的个体差异很大,临床医生应该对每一个患者做出最适宜的个体化决策和病情分层,优先处理重症,充分考虑患者自身因素及抗菌药物的自身特点,遵循指南,依据药动学/药效学(PK/PD)原理,正确使用药物(包括足够的剂量、给药次数及静脉滴注持续时间等),优化整体的治疗方案。
4. 根据病情严重程度 选择合适的治疗场所 临床常用PSI,CURB-65和CURB等评分标准对患者病情严重程度进行评估,除上述之外,还要注意初始治疗无反应肺炎患者在正确治疗情况下对治疗的应答情况(具体评分标准见附录-A)。
二、急诊CAP的整体治疗方案
CAP整体治疗方案是良好预后的重要保证。临床治疗过程中一方面强调对病原体的控制或清除,另一方面也需注意调节患者的免疫状态,器官功能支持,营养支持等。
我国《急诊成人社区获得性肺炎诊治专家共识》针对不同患者给予明确用药建议,目前常用的抗菌药物包括:β-内酰胺类、大环内酯类、呼吸喹诺酮类(见附录-B)。
严重感染时,机体处于一种复杂的免疫紊乱和失衡状态。相应的免疫治疗也不应只强调一个方面,而在于重建严重感染患者的免疫平衡稳态。因此,免疫调节主要在于上调或下调患者免疫水平,恢复患者机体免疫功能的平衡:(1)下调患者免疫水平:主要是针对过度炎症介质反应,给予糖皮质激素等治疗。(2)上调患者免疫水平:针对免疫功能低下或缺陷的患者早期给予免疫球蛋白(欧洲已有相应的浓缩免疫球蛋白制剂)、胸腺肽、全血及新鲜血浆等,通过改善机体免疫状态促进重症肺炎对治疗的反应。
同时,器官功能支持治疗亦很重要,包括机械通气、营养和液体支持以及血液净化治疗。正确认识病理生理实质,有针对性地对因和综合调节、支持治疗可以明显提高患者的治疗成功率。
1. 急诊流水留观CAP患者的抗感染治疗方案
1.1 急诊患者,既往有/无基础疾病推荐的抗菌治疗方案
(1)既往健康,无基础疾病的推荐治疗方案包括:青霉素类,如青霉素、阿莫西林1.0g po tid、阿莫西林/克
拉维酸625mg po tid等;大环内酯类,如阿奇霉素:首次给予500mg po,随后250mg/d po 5d;克拉霉素:500mg
po bid ;第一代或第二代头孢菌素类,如头孢拉定或头孢克洛500mg po tid、头孢呋辛或头孢丙烯500mg po tid
等;呼吸喹诺酮类,如莫西沙星400mg po qd、左氧氟沙星750mg po qd连续使用5天,或者500mg po qd连续使
用7~14天等。
(2) 对有基础疾病或近3个月内使用过抗菌药物患者: β-内酰胺类 (青霉素类或头孢菌素类)联合大环内酯
类,如:(大剂量阿莫西林/克拉维酸,头孢地尼100mg po tid,头孢泊肟酯100mg po tid,头孢丙烯500mg po qd)
联合阿奇霉素等;呼吸喹诺酮类单药药物治疗:如莫西沙星、左氧氟沙星等5。初始治疗后48~72h对病情和诊断
进行评价。凡症状明显改善,不一定考虑痰病原学检查结果如何,仍可维持原有治疗。症状显著改善后,胃肠外
给药者可改用同类或抗菌谱相近、或对致病原敏感的制剂口服给药,采用序贯治疗。
1.2 住院非EICU患者推荐的抗菌治疗方案
青霉素类/β-内酰胺酶抑制剂(如大剂量阿莫西林/克拉维酸,氨苄西林/舒巴坦1.5~3g iv q6h等)或头孢菌素类
(如注射头孢曲松1g~2g iv q24h,头孢噻肟,严重感染患者:2g~3g iv q6h-q8h等)联合大环内酯类(如阿奇霉素、
克拉霉素等);呼吸喹诺酮类(如莫西沙星、左氧氟沙星等)。
2. 重症CAP的整体诊治方案(EICU住院患者)
2.1 重症CAP的抗感染方案
目前对于重症肺炎推荐降阶梯抗感染治疗策略,初始采用广谱药物经验性治疗,一旦获得可靠的病原学培养结果,即换用有针对性的窄谱抗感染药物。重症肺炎获得病原学证据较困难,且目前我国缺乏大规模的流行病学研究,缺少重症肺炎病原谱的确切资料,抗感染药物的选择缺少依据,经验性抗感染治疗更为重要,应根据患者基础疾病、住院时间、已使用的抗感染药物等因素进行个体化治疗。美国感染病学会和美国胸科学会成立联合委员会(Infectious Diseases Society of America/AmericanThoracic Society, IDSA/ATS)发布的《成人CAP诊治指南》中根据患者有无铜绿假单胞菌感染危险因素对重症CAP推荐不同治疗方案:
(1)对于无铜绿假单胞菌感染危险因素的患者:可选用β-内酰胺类药物(如头孢噻肟,头孢曲松或氨苄西林/舒巴坦)联合阿奇霉素或上述β-内酰胺类药物联合氟喹诺酮类药物(对青霉素过敏患者,推荐呼吸氟喹诺酮类药物和氨曲南)。
(2)有铜绿假单胞菌感染危险因素的患者目前常用推荐方案为:可选用具有抗假单胞菌活性的β-内酰胺类药物(哌拉西林/他唑巴坦、头孢吡肟、亚胺培南或美罗培南)联合环丙沙星或左氧氟沙星(750mg)或上述β-内酰胺类药物联合氨基糖苷类和阿奇霉素或上述β-内酰胺类药物联合氨基糖苷类和抗肺炎链球菌氟喹诺酮类(对青霉素过敏患者,用氨曲南可替代上述β-内酰胺类药物)。铜绿假单胞菌感染危险因素主要包括:结构性肺病(如支气管扩张、肺囊性纤维化及弥漫性细支气管炎等)、长期气管切开和(或)机械通气及肺炎发病前使用抗生素、皮质激素治疗、营养不良、长期住院、粒细胞缺乏发热合并肺部浸润影等。
(3)对于军团菌感染患者,IDSA/ATS指南推荐首选氟喹诺酮类或阿奇霉素,备选药物为多西环素。目前,重症CAP的最佳治疗疗程尚未明确,一般疗程是7~10天,若是军团菌或铜绿假单胞菌感染,时间可延长至10~21天。另外某些因素也可影响疗程长短,如初始治疗失败、基础疾病、菌血症、肺外疾病、宿主反应等。目前一些数据表明,可根据临床表现相应缩短静脉治疗时间。一项包括302例重症CAP患者的随机试验表明:当患者临床稳定时可早期改为口服用药,也可达到标准的7天静脉用药效果。

2.2 重症CAP的免疫调节治疗方案
重症CAP的患者免疫功能异常可以分为两种类型:一类是过度炎症反应,另一类是免疫功能抑制。重症CAP产生的全身炎症反应及进而导致的MODS是机体防御机制的过度激活而引起自身破坏的结果,而不是细菌、毒素等直接损伤的结果。因此,对重症CAP的治疗不应局限在目前的控制感染和支持治疗方面。免疫调节主要治疗免疫过度或免疫缺陷,调节机体免疫平衡状态。
(1)免疫支持治疗方案:若患者发生严重感染并存在免疫抑制时,可采用相关的免疫支持治疗,可使用干扰素-γ(INF-γ),胸腺肽-α1,粒细胞巨噬细胞集落刺激因子(GM-CSF)等治疗免疫抑制等情况。IFN-γ是在炎性刺激下细胞毒性T细胞和辅助T细胞分泌的细胞因子。IFN-γ的分泌可以通过两条途径促进巨噬细胞的作用。第一条途径是促使细胞生产更多的吞噬蛋白。第二条途径是通过上调组织相容性抗原受体的表达来提高抗原呈递性。使用IFN-γ可以增强肺泡吞噬细胞的免疫作用,对CAP有显著效果。胸腺肽-α1是免疫刺激胸腺组织自然产生的28个氨基酸组成的多肽,通过结合Toll样受体促进T细胞的成熟及发挥作用。研究者发现经过胸腺肽-α1治疗,患者单核细胞HLA-DR表达增高。此外,胸腺肽-α1治疗脓毒血症的机制尚不明确。GM-CSF由白细胞分泌,主要是用来促进干细胞分化为粒细胞和巨噬细胞——体内重要炎性反应。研究表明,在体外GM-CSF可以改善单核细胞人类白细胞抗原测 – DR(HLA-DR)的表达,故被用于辅助治疗。HLA-DR是衡量免疫细胞活性的标志物。在脓毒症免疫抑制阶段,HLA-DR表达降低。脓毒症患者HLA-DR表达降低就意味着二次感染的风险增高及生存率的降低。在这种情况下,增强吞噬功能及抗原呈递可以更有效的清除感染并改善预后。然而,目前用免疫调节剂来改善重症CAP患者的预后仍存在一定争议,需更多设计严谨的大规模临床试验来评价上述药物的有效性、安全性及适应症。
(2)抑制过度免疫反应:临床主要通过应用糖皮质激素治疗严重感染及感染性休克。在重症肺炎中,激素不像在感染性休克中使用那么广泛。目前,临床应用糖皮质激素一直存在争议。近年的研究显示:大剂量、短疗程糖皮质激素冲击治疗并不能改善感染性休克的预后,而低剂量使用激素能够减少肺炎的严重反应和改善疾病进展13,14。但另一方面,糖皮质激素也能抑制机体的炎症防御机制,在感染未受到控制的情况下,可能导致感染加重。同时大剂量使用激素还可引发消化道出血、继发性真菌感染等严重并发症。相关研究证实,糖皮质激素可明显降低行机械通气治疗的肺炎患者的TNF-α、IL-1、IL-6及C-反应蛋白(C- Reactive Protein,CRP)水平。危重脓毒症患者接受糖皮质激素辅助治疗在呼吸生理、免疫及血流动力学方面获益显著,死亡风险明显下降。
临床工作中要注意区分重症CAP患者不同的免疫状态,对于产生过度炎症反应的患者(例如全身炎症反应综合征表现显著者)应早期应用适量的糖皮质激素。但是对于免疫功能缺陷的患者,应禁止或慎用糖皮质激素。对于老年人、有原发性肾上腺皮质功能缺陷的患者应使用小剂量激素,避免使用大剂量激素。目前,仅针对全身感染或合并感染性休克的患者推荐小剂量激素治疗(氢化可的松不超过300mg/d),一般疗程5~7天;当患者能够停用血管活性药物时即可停用皮质激素。
2.3 重症CAP的器官功能支持治疗方案
2.3.1 呼吸支持治疗重症CAP患者常发生呼吸衰竭,其特征为严重的低氧血症,往往需要进行呼吸支持。呼吸支持治疗可有效纠正缺氧和酸中毒。通常低氧血症或呼吸困难患者,可使用无创通气,即使是痰液较多的患者,也可以间断使用无创通气。
(1)常规机械通气:在EICU治疗的重症CAP患者,如伴有严重的呼吸衰竭,则应进行气管插管和指令通气治疗。临床上常用的通气模式为同步间歇强制通气(SIMV)或辅助/控制通气(A/C)模式,给予恰当的呼吸频率。根据低氧血症的严重程度和肺顺应性降低的情况来选择呼气末正压通气(Positive End Expiratory Pressure, PEEP)。对于有创机械通气的患者适当的镇静止痛和肌松治疗会缩短患者的病程,有助于改善预后。但是要注意合适的剂量和时间,因为过度的镇静和肌松会导致撤机困难。
(2)无创伤性通气:对于中等程度低氧血症的CAP患者,可应用面/鼻罩进行无创伤性机械通气(Non-invasivePositive Pressure Ventilation, NPPV),模式有持续气道正压(Continuous Positive Airway Pressure, CPAP)、双水平正压气道(Biphasic Positive Airway Pressure, BiPAP)以纠正低氧血症,其优点是可避免气管插管并减少机械通气的并发症。CPAP或BiPAP可复张塌陷和通气不佳的肺泡,因而能减少肺内分流和改善通气灌注不均。如患者发生呼吸肌群疲劳,面罩通气可为患者提供压力支持通气,使患者的潮气量增加,并增加肺泡内压力以纠正低氧血症。然而NPPV的治疗价值尚存在争论。NPPV治疗肺炎导致的低氧血症的失败率较高,应用需综合考虑患者的临床状况和疾病的进展等问题,权衡NPPV治疗的利弊。对于合适的患者,可以在EICU中密切监护下实施NPPV治疗。虽然应用NPPV在1h后急性呼吸窘迫综合征(Acute Respiratory Distress Syndrom, ARDS)患者的氧合功能明显改善,但并未降低气管插管率、住院病死率和住EICU时间等。目前推荐符合以下条件者可试行治疗:(1)患者清醒合作,病情相对稳定;(2)无痰或痰液清除能力好;(3)多器官功能衰竭;(4)简明急性生理学评分(SAPSⅡ)≤34;(5)NPPV治疗1~2h后Pa O2/FiO2>175 mmHg;(6)基础疾病容易控制和可逆(如手术后,创伤等)。特别注意,NPPV只是一种呼吸支持治疗,而不是病因治疗。开始治疗有改善并不代表最终治疗的有效。并且NPPV有可能增加患者的痰液粘稠度不利于排痰。需要密切监测病情变化,一旦病情恶化并达到气管插管的指标则转为有创通气,避免延误气管插管。
(3)体位变换,改善通气状况:重症肺炎患者中,有时需要特殊的机械通气治疗,尤其当患者出现广泛的单侧肺脏受累时。肺叶实变的患者常可发生严重的低氧血症,多见于肺炎链球菌所致的CAP。这些肺炎患者中,由于肺血管严重低氧性收缩的消除,血管灌注到通气不佳或无通气的肺泡,产生明显的分流,往往加重低氧血症。对于这类单侧肺炎的患者,如要改善氧合,那么患者的体位尤为重要。通常可将患侧的肺部位置朝上,通过调整患者在床上的位置,使重力作用增加健侧肺叶的血流灌注,从而达到通气和灌注的最佳比例,改善氧合作用。而对于单侧肺炎所产生的严重低氧血症,如果应用常规机械通气,有时可造成动态过度充气、肺血管阻力增加、纵膈移位、胸腔内压增加和心脏压塞症状,现能使用一项新的通气治疗技术来治疗单侧肺炎所产生的严重低氧血症,即分侧肺通气。分侧肺通气时,用一个双腔气管代替常规气管插管,这可对每一侧肺分别进行机械通气治疗,通常应用两台呼吸机对两侧肺作独立的机械通气。两肺通气时一般同步进行,有时也可非同步。对每侧肺通气时,通气机的设置可按最佳氧合来选择。病变肺部通常顺应性较差,需要较高的PEEP以复原微小的肺不张和改善肺顺应性。而未受累侧的肺脏可常规机械通气,以防止肺过度扩张。
2.3.2 连续性肾脏替代治疗(Continuous Renal Replacement Therapy, CRRT)
重症肺炎合并休克或MODS的患者体内大量代谢产物堆积,中性粒细胞、白细胞介素、肿瘤坏死因子、黏附分子等细胞因子过度表达。为保持内环境平衡,不仅需要行血液净化,还应彻底纠正代谢紊乱及清除炎症介质。重症感染患者早期CRRT治疗既可以稳定机体内环境,保证液体平衡;亦可在血液净化实施过程中吸附一定的炎性介质,控制病情进展。然而,CRRT在EICU非肾脏疾病中的应用仍有争议。其并非是间歇性血液透析(Intermittent Hemodialysis, IHD)的一种单纯简单的改良,对于危重患者的治疗需要平衡渐进性治疗。同时,CRRT治疗也不应局限于某个阶段,对于具备SIRS、ARDS、MODS、严重感染等疾病,应力求早期治疗,通过调控炎症反应阻断其发展,能有效干预SIRS,可能是防治MODS的关键。目前,急性透析质量指导组认为,对于重症急性肾功能衰竭( Acute Renal Failure, ARF)患者传统透析指征未被纠正,应继续CRRT。同时,有学者认为,对于急性肾功能衰竭ARF合并MODS患者,当炎症反应下调,对机械通气及肠外营养的需求降低,肾清除溶质功能已恢复或部分恢复,机体自我调节容量平衡应停止CRRT。总之,对于危重症患者,CRRT与机械通气和营养支持同样重要,为基本的干预治疗工具。CRRT早期大剂量能维持稳定调整内环境,调整免疫细胞、内皮细胞功能障碍,重建集体免疫内稳态,摆脱病理状态对某些内环境的干扰,为机体的恢复创造条件。同时,在保证重要脏器功能的同时,积极争取治疗原发病的时间,从而可大大提高危重症患者的救治成功率。
2.3.3 重症CAP的营养支持治疗
重症感染患者处于高分解代谢状态,合理的营养支持是机体恢复的物质基础,可提高机体免疫力、纠正电解质紊乱。加强全身支持治疗,尽可能经口摄食,鼻饲饮食,只有完全无法进食的患者,才考虑全胃肠道外营养(Total Parenteral Nutrition,TPN),并尽可能缩短TPN时间,减轻脏器损伤,为进一步治疗争取时机21。早期应用肠道营养及特殊营养底物谷氨酰胺,可预防肠道功能衰竭,改善肝、肾功能,降低EICU危重患者的病死率,这可能与其增加内脏血流、减少肠源性内毒素的转移以及炎症调节因子的释放有关。对高分解代谢患者,宜在内环境稳态进入平衡后进行营养支持治疗,大多数患者在伤后或发病后24~48h内进行此项治疗。与高热量TPN相比,低热量TPN能减轻肺功能损害,改善氮平衡,以及减少尿中3-甲基组氨酸的排出。因此,现代临床营养支持已经超越了以往提供能量、恢复“正氮平衡”的范畴,通过代谢调理和免疫功能调节,使营养支持治疗从结构支持向功能支持发展,发挥着“药理学营养”的重要作用,是现代危重病治疗的重要组成部分。重症患者常伴随应激性高血糖,且血糖水平随病情及治疗变化而波动。应激性高血糖可增加患者的病死率,而强化胰岛素治疗可通过防治高血糖的毒性作用,改善机体能量代谢和高凝状态,降低感染的发生,促进疾病的恢复。
2.3.4 体外膜氧合(Extracorporeal Membrane Oxygenation,ECMO)
重症CAP可导致各系统的严重并发症,例如ARDS、严重心功能不全、感染性休克等,在综合治疗仍然无法使病情得到缓解的情况下,可以考虑在适合的患者实施ECMO。
(1)ECMO适应症:潜在可逆性的严重急性呼吸衰竭或心脏衰竭23,24①各种原因引起的严重心源性休克,如心脏术后、心肌梗死、心肌病、心肌炎、心搏骤停、心脏移植术后等;②各种原因引起的严重急性呼吸衰竭,如严重ARDS、哮喘持续状态、肺移植后原发移植物衰竭、弥漫性肺泡出血、肺动脉高压危象、肺栓塞、严重支气管胸膜瘘等;③各种原因引起的严重循环衰竭,如感染中毒性休克、冻伤、大面积重度烧伤、药物中毒、CO中毒、溺水、严重外伤等
(2)禁忌症:如果患者具有出血风险或凝血功能障碍、不可逆的心脏或呼吸衰竭、不能进行心室辅助装置植入,则不推荐行ECMO23,25,26①有应用肝素的禁忌或相对禁忌,如严重凝血功能障碍、合并有近期颅内出血、对肝素过敏、具有肝素诱导的血小板减少症患者及无法行抗凝治疗的任何疾病的患者;②对于呼吸衰竭的患者,高压通气超过7天(气道平台压>30cmH2O);高氧浓度(FiO2>0.8)使用超过7天;血管通道限制即置管限制;限制ECMO好处的任何情况或者器官功能障碍,比如危重的、不可逆脑损伤或者不可治疗的癌症转移;③对于心脏衰竭的患者,不可进行心室辅助设备植入或心脏移植手术禁忌患者;④另外,对于高龄、肥胖(体重>1kg/cm或BMI>45kg/cm2)、神经功能障碍的患者,ECMO所提供的氧供尚不能满足这类患者的需求
(3)行ECMO的临床指征23,25,26①ARDS:危重低氧血症[高水平呼吸末正压(PEEP=15-20cmH2O)持续至少6h条件下,氧合分数PaO2/FiO2<80,并且呼吸衰竭具有逆转的潜在可能性;通气频率>35次/min时pH值<7.15且平台压>35-45cmH2O;年龄<65岁;机械通气时间<7天;无抗凝禁忌;②重症肺炎所致严重呼吸衰竭可参考上述标准;③支气管哮喘:对于平台<7.1),或血流动力学难以维持者,若无ECMO禁忌,可积极行ECMO或AV-ECMO;④肺栓塞:对于伴有严重血流动力学障碍而又不宜常规溶栓者,或需要手术迅速解除梗阻者,行VA-ECMO以迅速降低右心负荷,稳定血流动力学,并改善氧合;⑤大气道阻塞:由于新生物或异物所致大气道阻塞常需要气管切开或气管镜介入治疗,以ECMO支持可以保证上述操作安全进行;⑥慢性阻塞性肺疾病:AVECMO可使大部分需要有创通气的重症慢阻肺患者避免插管,并维持较好的通气与氧合;⑦另外,肺移植、心脏骤停、难治性心源性休克及心脏外科手术后未能脱离心肺转流术患者可行ECMO。2.3.5 内分泌功能支持重症CAP患者存在一定程度的内分泌功能异常,应根据临床评估患者是否存在内分泌功能异常,给予针对性治疗。
学术交流文章,不做为临床依据,特此声明。发布者:Chu,转转请注明出处:https://www.icu.cn/?p=2379

 微信扫一扫
微信扫一扫 
![[JAMA述评] 迈向个体化治疗:评估随机临床试验中疗效的异质性](https://www.icu.cn/wp-content/uploads/2023/05/2023-05-09_112937-480x300.gif)