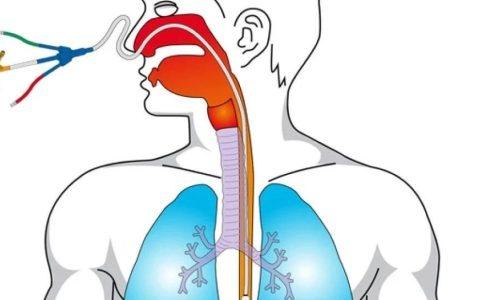
我们小组常规使用食管测压法对急性呼吸窘迫综合征 (ARDS) 患者进行个性化机械通气。食管压力 (Pes) 允许区分胸壁、肺和呼吸系统力学,我们将其用于 PEEP 滴定、监测肺实质压力、限制峰值吸气末跨肺压和监测呼吸机同步性。
我们发现食管测压在大多数患者中是简单的,尽管适当的培训和应用很重要。初始步骤是通过插入与常规胃管相似的独立导管或带有集成食管球囊的饲管来确保正确放置。
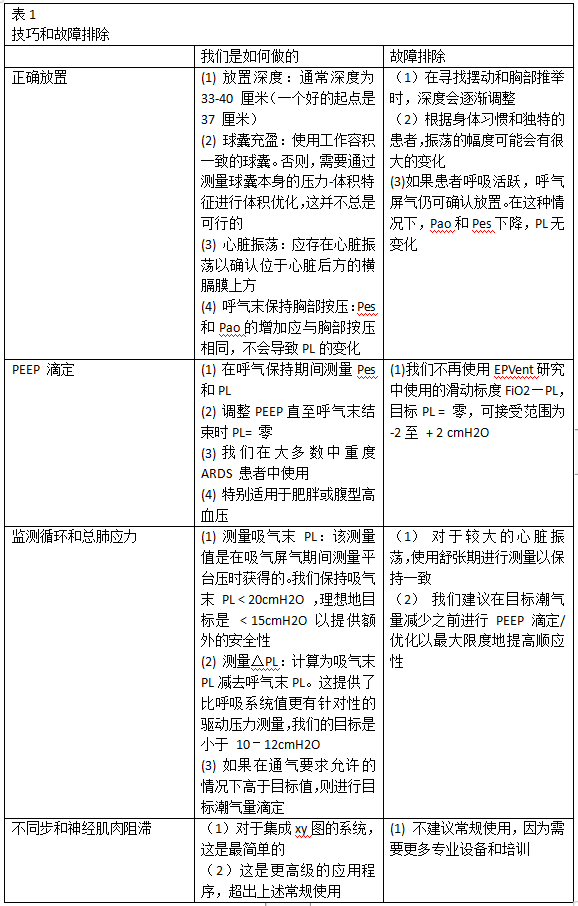
典型的插入深度范围为33至40 cm,取决于体型,我们通过功能性床旁评估确保正确放置。首先,我们寻找心脏振荡的存在,以确保心脏后方的正确位置。如果不存在,这表明球囊过深或过浅,我们在监测这些振荡时逐渐调整。
接下来,我们进行呼气屏气,在轻轻胸部按压期间监测Pes、气道(Pao)和跨肺压(PL = Pao−Pes)的变化。当Pes和Pao等量增加且计算的PL无变化时,确认位置正确。如果 Pao 增加更多 Pes,这表明位置太深,并且通过重复胸部推动来逐步调整气球。这可以通过轻轻的腹部推动来证实(Pes 增加超过 Pao)。(表1)。
使用具有一致工作范围的充气体积的气球有助于获得一致和准确的测量结果。虽然可以根据球囊本身的压力-容积特性来确认最佳充气容积 ,但在使用具有已知可接受范围的球囊时,这非常耗时且在实践中不需要。
由于球囊的顺应性,过度充气会导致测量的压力不准确,而充气不足则会导致波形变化的抑制。呼吸机内的集成压力传感器有利于数据的可视化和解释,或者可以使用独立的设备进行记录,正如我们在EPVent和EPVent2研究中所使用的那样。
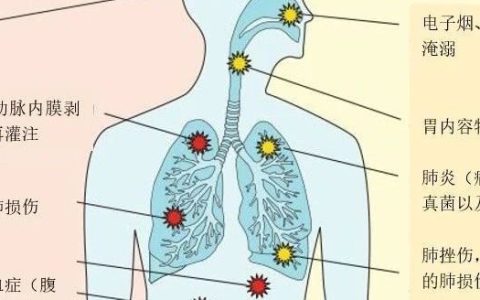
食管测压法的主要应用之一是滴定呼气末正压(PEEP)。危重患者经常表现出胸壁重量增加和基础呼气末胸膜压升高,继发于水肿、胸腔积液、腹压升高和其他原因,这些原因可能导致去复张、肺弹性增加和低氧血症。
我们测量Pes作为胸膜压的替代指标,如果胸膜压大于测量的气道/肺泡压(PL = Pao−Pes),这些塌陷压可以通过应用PEEP来对抗。我们的EPVent和EPvent2研究调查了使用食管测压法来调整PEEP,虽然后者的研究没有显示出与经验性高PEEP相比有明显的好处,但进一步的分析表明,当呼气末PL维持在-2至+2cmH2O的严格生理范围内的PEEP调整时,有好处(出版物正在审查),这也是我们在临床上的做法。
我们的目标是使呼气末PL为零,而不考虑FiO2,这与原始的滑动比例方案不同,并且在一定程度上是次要的,因为纵隔伪影在“实际”PL与测量PL中获得了轻微的益处。
我们发现食管测压法对病态肥胖和 ARDS 特别有用,可以测量升高的胸膜压和安全应用高 PEEP 水平(~20-30cmH2O)以减轻胸壁的重量。相反,食管测压法也可用于确定何时应用的 PEEP 过高,允许有针对性地滴定以降低 PEEP,从而防止过度扩张的有害影响(图 1)。
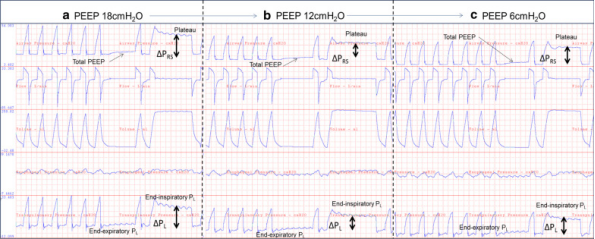
图1
该图代表了1例轻度肥胖女性的呼气末正压(PEEP)滴定,该患者患有继发于腹水和TRALI的中-重度急性呼吸窘迫综合征(ARDS),伴有胸壁僵硬度增加和基础胸膜压轻度升高。患者接受Vt 250 cc(接近5 cc/kg IBW)、RR 34和FiO2 0.6。
该示例说明了PEEP滴定和监测循环和总肺应力水平的用途,以及如何使用食管测压法滴定PEEP,不仅可滴定至高水平,还可用于向下滴定至最佳中间范围。调整PEEP(气道压-Pao),以匹配测量的食管压(Pes),计算跨肺压(PL = Pao–Pes),并将PL目标值设为零。最初对该患者使用的经验PEEP为18 cmH2O(相当于使用经验高PEEP ARDSnet表)。
在这些初始设置下,总PEEP为20 cmH2O,平台压为40 cmH2O,呼吸系统驱动压(∆PRS)为20 cmH2O,呼吸系统顺应性为12.5 mL/cmH2O。呼气末跨肺压(PL)为 + 5 cmH2O,吸气末PL为20 cmH2O,跨肺驱动压(∆PL)为15 cmH2O,肺顺应性为15 mL/cmH2O。这些数字表明 PEEP 应用过高,并可能导致通过循环和总肺应力测量的过度膨胀。
b将PEEP降低至12 cmH2O导致在PEEP为12 cmH2O时发现优化力学。这导致总PEEP为14.5 cmH2O,平台压为29.5 cmH2O,∆PRS为15 cmH2O,呼吸系统顺应性为18 mL/cmH2O,呼气末PL为 + 0.5 cmH2O,吸气末PL为11 cmH2O,∆PL为10.5 mL/cmH2O,肺顺应性为24 mL/cmH2O。c将PEEP进一步降至6 cmH2O导致明显去复张,力学恶化。
PEEP总量8.5 cmH2O,平台压26.5 cmH2O,∆PRS 18 cmH2O,呼吸系统顺应性13.9 mL/cmH2O,呼气末PL为-5.8 cmH2O,吸气末PL为9 cmH2O,∆PL为14.8 cmH2O,肺顺应性16.8 mL/cmH2O
作为一种更具体的肺应力测量方法,我们定期监测肺部的循环扩张压力(跨肺驱动压 [ΔPL])。虽然呼吸系统驱动压力与 ARDS 患者的死亡率相关,但我们认为这是不充分的,因为我们可以使用 Pes 直接测量胸壁的固有变异性和异质性。
由于肺不均匀性和局部压力升高,我们的目标 ΔPL 小于 10–12cmH2O,这可以预防肺损伤 ,并且与我们的回顾性死亡率数据一致。ΔPL 很容易测量为吸气末 PL(平台压力当量)减去呼气末 PL(总 PEEP 当量)。
除了循环肺应力外,我们还使用 Pes 来测量除平台压外的总肺应力(吸气末 PL)。平台压 < 30cmH2O 代表不同程度的肺应力,具体取决于胸壁力学。
虽然尚未明确定义安全水平,但我们已经根据我们对应力、应变和特定弹性之间关系的理解推断出阈值,并且数据显示高∆PL和吸气末PL可使肺达到总肺容量,并导致致命的呼吸机相关性肺损伤因此,我们的做法是将吸气末 PL 限制在小于 20cmH2O(理想情况下甚至更低,小于 15cmH2O),以减少过度扩张并提高安全边际。
如果我们识别出 ΔPL 或总吸气末 PL 升高的患者,则该数据用于促进有针对性的潮气量减少,以将这些值控制在更安全的范围内。我们认识到,有必要对这些限制进行进一步的前瞻性调查,以更好地阐明目标,但我们将这些数据与其他临床数据相结合,以帮助为我们的床边治疗提供信息。重要的是,由于胸壁压力和弹性变化很大,如果不使用食管球囊,我们无法预测我们是否会达到这些循环和总应力的阈值。
我们还在床边评估患者-呼吸机同步性中使用食管测压法,使用胸壁压力容积环来识别被动呼吸机输送的呼吸、自主呼吸、不同步 ,用于神经肌肉阻滞的滴定和直接测量呼吸功、吸气肌用力和肺导向机械功率,以评估何时用力水平可能有害。总之,食管球囊导管易于放置和解释。测量的食管压力和跨肺压的计算在机械通气患者的 PEEP 滴定、肺应力测量和呼吸机同步性评估方面具有广泛的应用。
参考文献:
Baedorf Kassis E, Talmor D. Clinical application of esophageal manometry: how I do it. Crit Care. 2021;25(1):6. Published 2021 Jan 5. doi:10.1186/s13054-020-03453-w
本文荟萃自公众号:知乎小报,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫