本文目的
肝移植仍然是治疗晚期肝病和肝功能衰竭的唯一最终治疗方法。目前用于肝移植的分配方案要求采用“最严重的优先”方法,因此大多数肝移植发生在严重的全身性疾病患者中。对于照顾肝移植受者的重症监护医务人员来说,了解原位肝移植的技术考虑、基本的治疗的考虑和常见并发症的知识基础是必不可少的。这篇综述强调了作者对术后肝移植受者进行重症监护管理的方法,并回顾了在该患者群体中出现的常见问题。
最近的研究发现
全球提供肝移植的中心数量持续增加,接受肝移植的患者数量也在持续增加。晚期肝病患者的数量远远超过了可用的器官数,因此,接受肝移植的患者在移植时病情更严重。由于移植前和移植后的手术技术、免疫抑制管理和肝病重症监护管理的进步,肝移植患者的预后继续改善。
总结
鉴于全球肝移植数量的增加,越来越多的重症监护专业人员可能会照顾这一患者群体。对于这些提供者,学习关于常见并发症和关键管理的基本知识是必要的。
关键词
胆道并发症,肝动脉血栓形成,重症监护,肝移植,原发性移植物无功能
背景
晚期肝病仍然是全球第12大死亡原因,肝癌是全球癌症相关死亡的第三大原因。肝移植仍然是晚期肝功能衰竭的唯一最终治疗方法,也被用于选定的原发性肝癌患者的治疗方法。2021年,美国进行了9236例肝移植,这个总数比前一年增加了4%,比2011年的增加了46%。在全球范围内,脑死亡后对器官捐赠的接受程度的增加和活体肝移植的持续扩大,增加了在以前无法获得的地区进行肝移植的机会,预计还将继续增长。这一趋势需要了解肝移植后患者管理中涉及的常见并发症(见表1)。
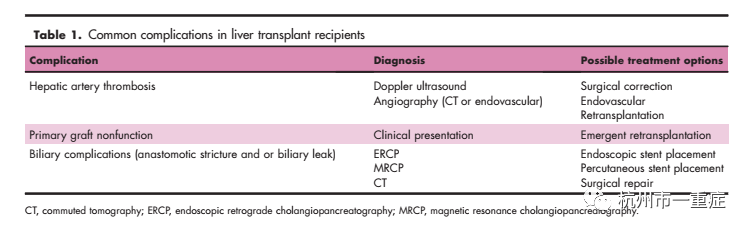
门脉高压(伴静脉曲张出血相关并发症)和显著的血流动力学损害。肝硬化并发症的管理超出了本文的范围,并在其他地方进行了回顾。然而,了解失代偿性肝功能衰竭的生理特征对于那些将照顾肝移植后患者的患者是至关重要的,因为许多这些并发症至少在肝移植后短暂地持续存在,并影响围手术期的管理。
传统肝移植技术是通过切除肝和肝后下腔静脉(IVC),然后插入供体IVC,它(IVC)仍然附着在肝移植物上,通常被称为“常规技术”。这种方法要求IVC在两个位置吻合,通常涉及体外静脉-静脉旁路的使用。该技术与IVC吻合和体外旁路术的并发症相关。
第二种技术称为“背驼技术”已经开发出来,并越来越多地应用于移植中心,50%的欧洲中心使用背驼技术技术,41%使用传统技术作为标准技术。在背驮式技术中,保持IVC的连续性,很少需要使用静脉-静脉旁路。在这个过程中,是通过从IVC解剖肝静脉实施肝切除术,利用供体IVC移植物植入,并与受体的肝静脉吻合。背驼式手术技术与较短的手术时间、较短的无肝期(41 vs. 121 min。;P < 0.001),较短的热缺血时间(35 vs. 45 min;P < 0.001),以及较低的血液制品需求(13 vs. 18个单位;P < 0.001)相关。这进一步导致ICU住院时间减少(60小时vs. 96小时;P < 0.008)和整体住院费用降低(90 412 美元vs.113 838美元;P < 0.002)。虽然背驮式技术有明显的好处,但在某些情况下可能需要使用传统的方法。例如,包括患者特定的解剖考虑,外科研究员的培训要求,以及普通外科经验和专业知识。
除肝静脉吻合外,肝移植还包括肝动脉和门静脉吻合,最后需要进行胆道吻合。根据解剖学和疾病具体方面的考虑,胆道吻合术可以通过多种方法完成。胆总管吻合术(管-管吻合术)是最常见的胆道吻合方法;然而,在受体管病变(如原发性硬化性胆管炎)或解剖结构不合适的情况下,供体导管可以与新形成的输入端吻合或直接至十二指肠(胆总管十二指肠吻合术)。了解胆道吻合术的类型是至关重要的,因为调查胆道并发症受手术解剖的影响;例如,有输入端的患者可能无法进行胆管内镜检查,因此可能需要经皮检查。
对于手术过程中发生的意外并发症,与手术团队进行直接沟通是很重要的,因为这些并发症会增加ICU的并发症发生风险。例如,过度失血、热缺血时间延长或血管损伤,这可能会增加肝动脉血栓形成的风险。了解肝移植过程中的失血量和需求是至关重要的,因为这对术后预后有重要意义。在2017年的一项研究中,接受肝移植的患者接受少于6单位的浓缩红细胞(prbc),中位LOS为7天。当患者接受至少6个单位的prbc时,中位数ICU住院时间从2天到4天增加了一倍(P < 0.0001),总体医院住院时间从7天增加到10天(P < 0.001),中位数住院费用增加了51% 。在同一研究中,至少有12个单位RBC的患者与接受少于12个单位的患者使用呼吸机时间为2天VS1天,有统计学意义的增加。
随着时间的推移,血液产品的输血需求总体有所下降而减少。在一项单中心研究中,评估了两个独立时间队列(1990-1991年与2005-2006年相比),红细胞(16比6单位;P < 0.001),FFP(16比2单位;P < 0.001)、冷沉淀(16比0.001)和血小板(16比4.5个单位;P<0.001)(数据报告为给药单位的中位数)明显下降。
并发症和其他的治疗
血管并发症
肝动脉血栓形成(HAT)是肝移植后发生的最令人担忧的并发症之一,也是肝移植后最常见的血管并发症。肝移植后,肝动脉继续为肝脏贡献50%的含氧血流量。动脉血流受损导致肝实质灌注不足,特别是胆道上皮,因为胆管100%依赖于动脉血流进行氧合。
HAT被分为早期(eHAT)或晚期,在本综述中,eHAT被定义为移植后10天内发生的情况。HAT对移植物功能障碍有重大风险,这可能导致移植物快速衰竭和死亡。在现代肝移植时代,HAT的发病率有所下降,在成人肝移植人群中eHAT的发生率为2.9%,总死亡率为34.3% 。与晚期HAT相比,eHAT与较高的移植物丢失率和死亡率相关,部分原因是随着时间的推移,侧枝循环的发展。eHAT的表现是可变的,从明显的移植物功能障碍和肝生化检查的明显异常、凝血功能障碍、发热、胆道漏和肝性脑病;到生化和临床上无症状。由于eHAT在临床上可能是无症状的,大多数移植项目在移植后早期使用多普勒超声检查,尽管这种筛查的强度在不同中心之间差异很大。我们建议对任何出现不明原因症状或生化症状的患者进行多普勒超声筛查。
目前还没有关于肝移植后HAT管理的循证指南,管理方案包括血运重建(手术或血管内)、再移植和观察。手术血运重建术的成功率不一致,其范围在10-55%之间。介入放射学辅助的血管内尝试进行血管重建和溶栓治疗的成功率在46-68%的之间。在eHAT的情况下,特别是在明显的移植功能障碍的情况下,大多数移植项目将考虑恢复肝移植,大多数分配系统允许在eHAT设置中优先的清单。eHAT的早期再移植(<30天)与改善预后相关。然而,在无症状且无明显移植物功能障碍的患者中,eHAT的血运重建可能与改善预后和避免再移植相关。
门静脉血栓形成(PVT)被报道发生在高达7%的肝移植中,但与移植物功能障碍的严重程度无关,这在HAT中发现,并不是紧急再移植的典型指征。更常见的是,PVT导致门脉高压相关的并发症,如腹水;然而,移植失败的病例报道。与HAT一样,PVT也可以通过移植肝的多普勒超声检测到。PVT可进行保守抗凝治疗、通过手术探查、或介入辅助血管手术。
肝移植术后最可怕的并发症可能是肝移植物的原发性无功能(PNF)。PNF是一个用来描述肝移植物在移植后执行基本代谢功能的失败的术语。虽然PNF没有公认的定义,但其特征包括进行性和严重的转氨酶升高、严重的凝血功能障碍、肝脏不能产生胆汁、乳酸酸中毒、低血糖和多器官衰竭,临床表现类似于急性肝衰竭。在PNF中,肝功能障碍的程度与需要紧急再移植。因此,符合PNF标准的患者在移植等待名单上处于最高优先级,为了紧急等待名单,PNF被美国监管机构定义为移植后7天内符合以下标准的患者:天冬氨酸转氨酶至少3000U/升;国际标准化比率至少2.5;动脉血pH 7.30或以下;静脉血pH 7.25或以下;乳酸至少4 mmol/l,所有结果均来自移植后24小时至7天的同一时抽血。
自20世纪80年代首次引入肝移植以来,PNF的发病率稳步下降,从2010年后的7.4%下降到2.2%。虽然PNF的总体风险有所下降,但PNF的风险因素基本保持不变。了解这些危险因素可能有助于移植团队预测移植物的失败。PNF的危险因素包括供体年龄、供体ICU住院时间、冷缺血时间、肝脂肪变性程度和受体疾病的严重程度。有一种使用容易获得的实验室检查的新的连续得分已经用于移植功能障碍的严重程度分级,也被证明是能够预测短期和长期生存,这被称为早期同种异体移植功能模型MEAF评分,并可在术后前三天内使用。
肾功能不全
急性肾损伤(AKI)是肝硬化的常见并发症,发生在高达50%的住院肝硬化患者。肝硬化中的AKI通常是由于肝肾综合征,并且在肝移植后通常是可逆的。AKI的持续时间相对较短。然而,需要考虑同时进行肝肾移植(SLK)的持续肾功能不全患者的发生率更高。事实上,SLK移植的数量在所有肝移植中的占比从1990年的1.7%增加到2016年的9.9%。对于已存在肾功能不全的患者,围手术期肾功能不全短暂恶化的风险很高。对于接受SLK移植的患者,移植肾功能可能会延迟恢复。预期有肾脏替代治疗的潜在需求,允许在围手术期出现严重酸碱、电解质或容量并发症的患者立即开始透析。
胆道并发症
肝移植术后的胆道并发症相当常见。胆道并发症可能包括狭窄和胆道漏。在移植后早期,狭窄通常是由于手术的技术问题(胆管损伤、小口径胆管和供体-受体胆管大小不匹配)或水肿。胆道狭窄的发生率接近10% 。胆道狭窄的临床表现可能无症状,生化指标异常,如胆红素、碱性磷酸酶和谷氨酰基转移酶升高,有或没有转氨酶升高。然而,患者由于脓毒症也可能伴有胆管炎、发热、腹痛和血流动力学不稳定。对疑似胆道狭窄的初步评估包括多普勒超声来评估肝动脉功能不全或eHAT,当发现血流减少时,这可能提示缺血性胆道狭窄的形成。虽然超声是评估胆管管径变化的一个非常有用的工具,但超声对胆管管径的检测灵敏度较差。
吻合口狭窄的处理可以通过内窥镜、放射学或手术来完成。在技术上可行时,通过ERCP进行的内镜治疗被认为是一线方法。ERCP的选择包括支架植入术或扩张狭窄。介入性放射学干预包括ptc引导下的扩张术和支架植入术。这是由于ptc引导治疗的侵袭性增加,以及相关风险,如出血、胆道漏和感染,被认为是ERCP失败或不可行的二线选择。
胆道漏也是一个肝移植后相对常见的并发症,报道发病率高达25%,他们可能与吻合失败,胆囊管,或从肝脏的活体肝移植。与胆漏发生相关的主要因素包括由于手术技术或并发症导致的胆道吻合口中断、胆道缺血(由于肝动脉并发症、冷缺血和热缺血时间延长),以及使用活体供体移植物。胆漏的发展增加了胆道狭窄的风险,降低了肝移植和患者的生存。小胆漏可以通过简单的观察来处理,对于需要治疗的胆漏,ERCP联合胆道支架加括约肌切开术是治疗的选择,目的是通过转移胆汁流量来降低泄漏部位的压力。对于持续的渗漏,可能需要手术翻修胆道吻合术。
免疫抑制
免疫抑制是肝移植成功的关键组成部分。典型的治疗方案包括类固醇、钙调神经磷酸酶抑制剂(他克莫司和环孢霉素)和抗代谢物(霉酚酸盐)。虽然长期的免疫抑制增加了机会性感染的风险,但这些感染通常在移植后立即出现是非常罕见的。神经系统并发症可能是移植早期最常见的并发症。作为参考,最近有一篇对免疫抑制药物及其并发症的综述,可供参考。
结论
在全球范围内肝移植领域在不断发展。手术技术的改进,以及对肝移植前和肝移植后患者的ICU管理的改进,已经导致了预后的显著改善和资源利用的减少。肝移植为多学科重症治疗管理的方法提供了极好的机会,应该包括肝病学家、移植外科医生和肾病医生、ICU医生。肝移植的成功根植于多学科团队的努力。肝移植患者的管理是一种连续的治疗,从对肝硬化和肝功能衰竭的并发症的全面了解开始。随着对肝硬化的生理学、手术技术和与肝移植相关的常见并发症的深入了解,许多ICU问题可以及时预测和处理,并取得成功的预后。
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫