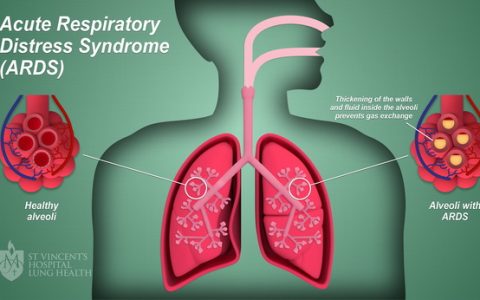
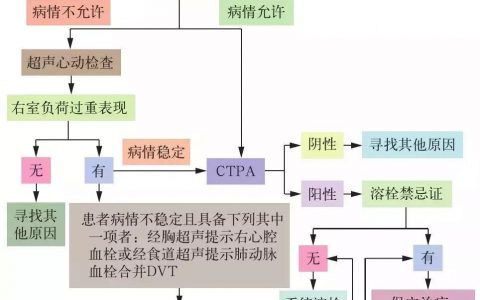
在真菌感染诊疗领域,区分「定植」与「侵袭」始终是横亘于临床医生面前的诊断鸿沟。「定植」被定义为在缺乏明确感染证据时,从患者特定部位反复分离出真菌的共生状态 [1];而「侵袭」则指真菌突破宿主防御屏障,引发组织损伤和系统性感染的病理过程。以曲霉菌(Aspergillus)为例,其作为腐生性霉菌广泛存在于环境中,人类每日吸入 100~1000 个分生孢子,免疫健全者可通过呼吸道上皮屏障、肺泡巨噬细胞吞噬等多重机制有效清除;但在免疫缺陷患者(如粒细胞缺乏、实体器官移植后状态)中,孢子萌发为侵袭性菌丝,启动血管侵袭和组织破坏的致命进程 [1-2]。
误判定植为感染将导致抗真菌药物滥用,加剧药物毒性反应和耐药菌株进化;反之,若延误侵袭性感染的诊断,患者死亡率可因治疗延迟 24 小时上升 33%[3]。重症监护病房(intensive care unit, ICU)患者的临床实践尤其凸显这一困境—约 80% 的疑似侵袭性真菌病(invasive fungal disease, IFD)因缺乏确凿证据被归类为「无法分类(non-classifiable)」[4]。这种灰色地带的广泛存在,本质反映了当前诊断技术在组织侵袭证据获取上的局限性。如何突破这一困境,成为真菌病研究领域的核心命题。
诊断准确率低下:从尸检数据看现实差距
侵袭性肺曲霉病(invasive pulmonary aspergillosis, IPA)是 ICU 患者中最常见的漏诊之一。一项针对 893 例 ICU 患者的尸检研究表明,仅 40% 生前确诊 IPA[1];病毒相关肺曲霉病(如流感或 COVID-19 相关)的拟诊病例中,仅 50%~55% 通过组织病理学验证死前诊断 [4]。此外,对 102 例慢性炎性肉芽肿患者的回顾性分析显示,术前误诊率高达 73%[5]。这些数据揭示了临床诊断的严峻挑战:危重患者因凝血功能障碍或病情危重难以获取组织样本,导致生前确诊率显著低于尸检结果。
临床鉴别决策模型:优化与争议
上述尸解研究以组织病理学确诊标准对存在侵袭而不是定植的研究,肯定低估了临床实践中的正确判断。这些病人存在严重的选择偏倚,与发生侵袭性霉菌感染患者的临床谱难以相符,所以不符合临床实际。
有鉴于此,Blot SI 等提出了被称为 AspICU 的诊断程序(表 1),用于重症病人是侵袭还是种植的鉴别。符合条件者被判断为确诊或推定的诊断(Putative);凡有一项或一项以上不符者判断为种植。该程序的特异性为 61%,灵敏度为 92%。阳性预测值为 61%,阴性预测值为 92%。表明该程序具有良好的可操作特性,可以区分危重患者的曲霉呼吸道定植和侵袭性肺曲霉病 [6]。
表 1 AspICU 诊断程序
 注:BAL = 支气管肺泡灌洗液;CT = 计算机断层扫描;EORTC/MSG = 欧洲癌症研究和治疗组织/真菌病研究小组
注:BAL = 支气管肺泡灌洗液;CT = 计算机断层扫描;EORTC/MSG = 欧洲癌症研究和治疗组织/真菌病研究小组
然而,AspICU 程序没有使用 GM 抗原检测,没有使用 qPCR(quantitative polymerase chain reaction, qPCR)在血液样本或 BAL 中检测曲霉 DNA。为此 Hamam J 等提出了称之为 BM-AspICU 的程序加以改进(图 1)。与 AspICU 程序判定为推定的 IPA ( n = 16) 相比,可以识别出更多符合 BM – AspICU 极似 IPA 者 ( n = 24) 的患者 [7]。
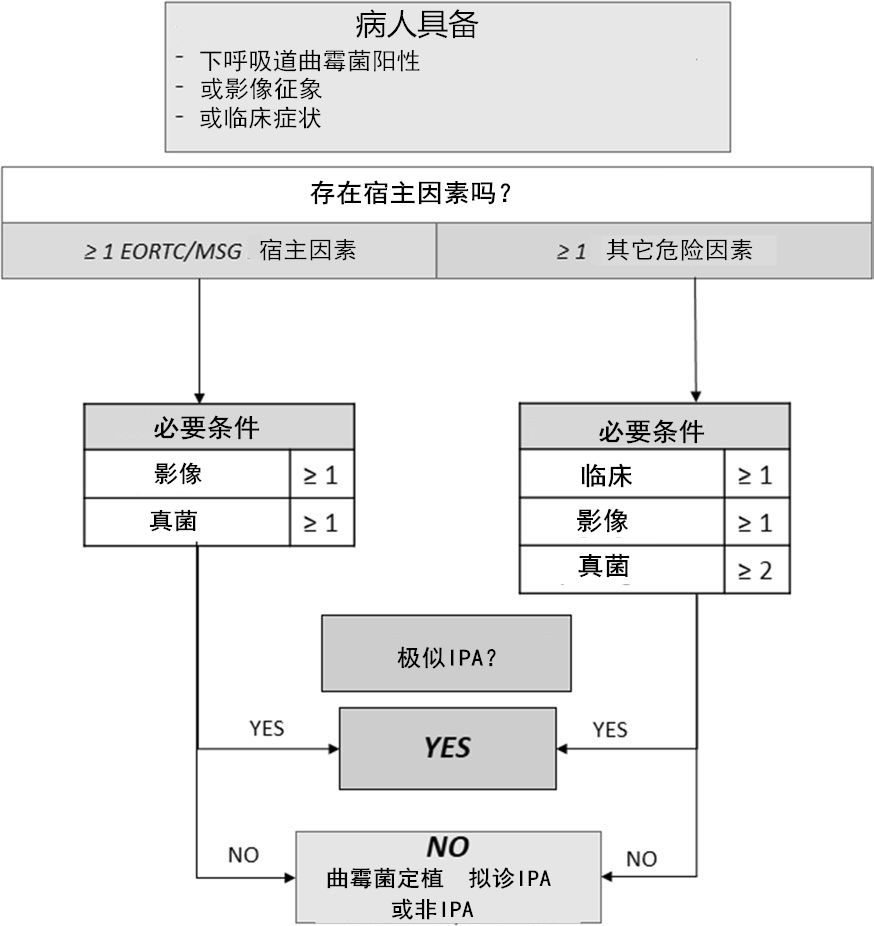 图 1 BM – AspICU 诊断程序
图 1 BM – AspICU 诊断程序
Vandewoude KH 等对定植与侵袭专门进行了长达 7 年的研究。那些符合条件者判断为极似 IPA(标准基本等同 AspICU),不符合确诊或极似 IPA 诊断标准者判断为定植。其后以组织病理学为金标准,发现该程序对定植或侵袭鉴别的敏感性、特异性均达到 100%[8]。
上述各研究的目的略有不同:AspICU、Vandewoude 程序目的明确:符合条件者为侵袭,否则为定植;而 BM-AspICU 不符合诊断条件者既有可能为定植,还有可能是其它。究竟谁对区分定植、侵袭的效力更好,尚需进一步研究。
该方法把病情(症状和体征)的变化纳入程序判断依据,而不是仅用客观指标(如 EORTC/MSG)作为标准,无疑更符合临床实际。
念珠菌指数:校正定植指数(corrected colonization index, CCI ≥ 0.4)与念珠菌评分(Candida score, CS > 2.5)可辅助区分定植与侵袭,敏感性 81%,特异性 74%[9]。
由定植到侵袭:界点难明
理论与实验室研究已使我们清楚辨别何为定植,何为侵袭。然而实验室研究发现的播散性疾病期间内皮内的定植和渗透(endothelial colonization and penetration during disseminated disease)似乎也模糊了二者间的一般概念(图 2)[9]。更重要的是,临床实际中真菌由定植到侵袭的初始发生难以及时识别(图 3)[1]。
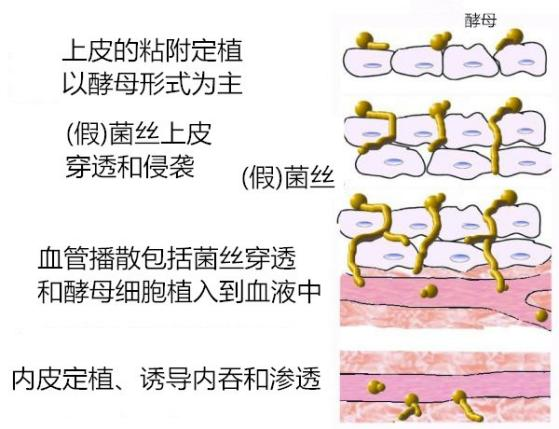 图 2 白色念珠菌组织侵入。图中显示了白假丝酵母侵入组织细胞表面的几个步骤:与上皮的粘附;通过菌丝进行上皮穿透和侵袭;血管播散,包括菌丝穿透和酵母细胞播种到血液中;最后在播散性疾病期间内皮定植和渗透。
图 2 白色念珠菌组织侵入。图中显示了白假丝酵母侵入组织细胞表面的几个步骤:与上皮的粘附;通过菌丝进行上皮穿透和侵袭;血管播散,包括菌丝穿透和酵母细胞播种到血液中;最后在播散性疾病期间内皮定植和渗透。
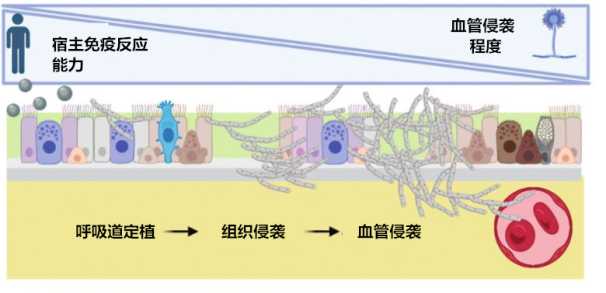 图 3 临床实际中由种植到侵袭。急性侵袭性肺曲霉病:侵袭谱。急性肺曲霉病可以看做是一个连续体,从呼吸道定植到菌丝侵入支气管和细支气管,最后血管侵入(随后传播到其他器官)。
图 3 临床实际中由种植到侵袭。急性侵袭性肺曲霉病:侵袭谱。急性肺曲霉病可以看做是一个连续体,从呼吸道定植到菌丝侵入支气管和细支气管,最后血管侵入(随后传播到其他器官)。即使能发现细胞学水平的侵袭是否就是临床意义上的 IFD 尚不得而知。一般认为,宿主具备酵母-菌丝转化的逆转化能力;而且白念珠菌的数量存在宿主耐受的阈值。宿主必须将真菌负担保持在这一阈值以下,并将非致病性白念珠菌细胞与侵袭性和潜在威胁生命的同一真菌细胞区分开来,以维持内环境稳定。病原体载量低时维持种植,载量高时发生侵袭(图 4、5)[10]。
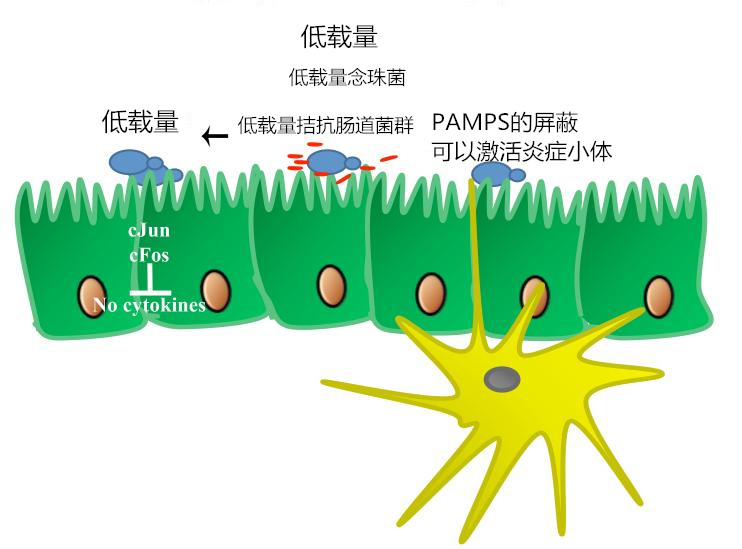 图 4 定植的维持
图 4 定植的维持
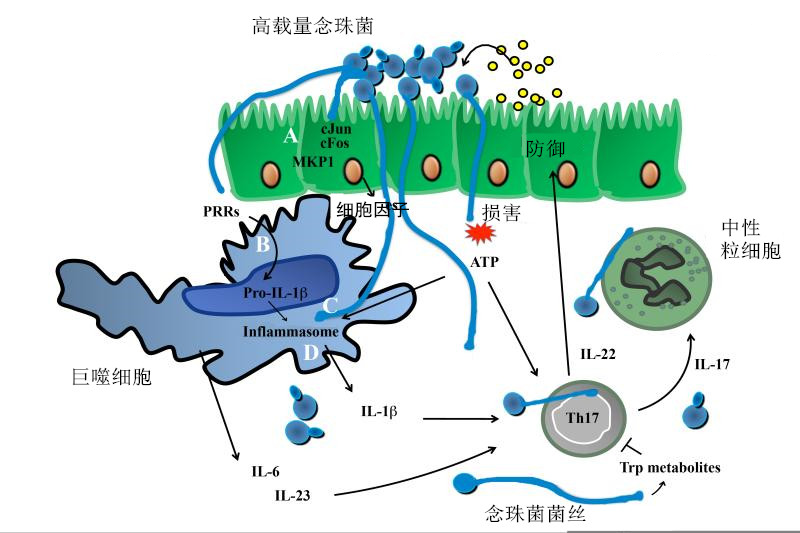 图 5 侵袭的发生
图 5 侵袭的发生微生物学诊断:pros and cons
IPA 的诊断仍然经常被漏诊,显示了我们诊断试验和方法的持续局限性。另外,曲霉菌抗原检测阳性可能会妨碍临床医生进一步寻找其他霉菌病原体的参与。
真菌生物标志物在侵袭性曲霉病 ( IA ) 的诊断中起着至关重要的作用,因此,了解诊断的可能性,特别是它们的局限性 (表 2 和表 3),对于面对风险患者的每一位临床医生都十分必要 [11]。
最重要的是,截值以上或其它阳性发现固然为我们判断侵袭提供了依据,但截值以下(或阴性)就一定不是侵袭,或者说就可以判断为定植,恐怕不是这样。微生物检测结果如果不与临床表现正确适配,则毫无意义。
表 2 侵袭性肺曲霉病最常用诊断试验的敏感性
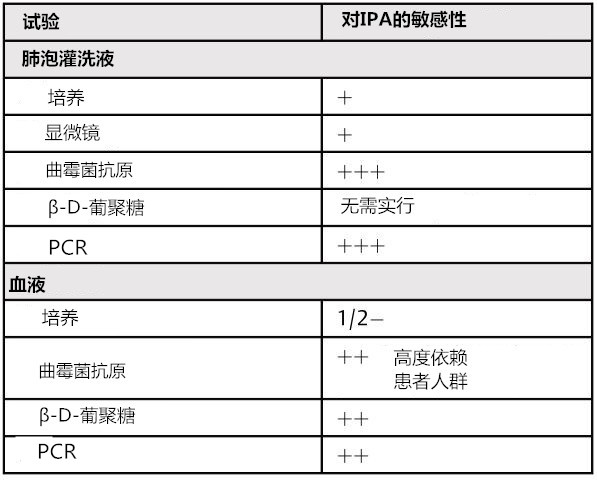 注:—,+,++,+++代表敏感性的一般分级
注:—,+,++,+++代表敏感性的一般分级
表 3 曲霉菌感染微生物学诊断试验的优(Pros)缺(Cons)点
 注:EIA,酶免疫测定;LFT:侧流试验包括侧流层析试验 ( LFAs ) 和侧流装置;NGS cfDNA:下一代无细胞 DNA 测序;PCR,聚合酶链式反应
注:EIA,酶免疫测定;LFT:侧流试验包括侧流层析试验 ( LFAs ) 和侧流装置;NGS cfDNA:下一代无细胞 DNA 测序;PCR,聚合酶链式反应
发现真菌:疑罪从有 OR 疑罪从无?
许多研究结果的不一致,使得判断真菌究竟是种植还是侵袭变得相当困难:
涂片镜检检出真菌孢子或菌丝可明确表示样本中有真菌存在,但阴性并不能排除真菌感染 [12],但国外的指南似乎认为其没有价值。
在非中性粒细胞减少患者的纤维支气管镜采样中分离到念珠菌,即使是高浓度的,都被确定为污染或可能污染而被认定没有临床意义 [7],但我们却在临床实际中怀疑肺曲霉菌病者当日痰液涂片镜检少量菌丝,次日标本即见大量菌丝,随之临床确诊肺曲霉菌病的病人。
业已证实,患有过敏性支气管肺曲霉病患者的大体肺标本通常显示气道内充满了厚厚的粘稠痰液和可能由真菌菌丝组成的纤维物质 [13],但即使这类病人痰涂片镜检的价值尚未见研究。
血清 GM 阳性对侵袭性曲霉菌病的指示性较高,但在曲霉菌定植的患者中,BAL GM 可呈阳性。因此,它并不绝对区分定植性和侵袭性疾病,只是提示侵袭性曲霉菌病的可能性更大 [15]。
连续两次 BDG 水平 ≥ 80 pg/mL 可以区分侵袭性念珠菌病和高级别定植(high-grade colonization)[16]。
尽管对侵袭性患者的特征进行了临床定义,但如何基于临床对定植进行确切定义尚是一个难题:
有学者对呼吸道标本中分离出曲霉菌,符合下列条件者定义为定植 [15]:
1. 病理研究符合其他病因;
2. 没有半乳甘露聚糖阳性的证据,也没有符合 IPA 影像;
3. 患者未经抗真菌治疗存活至少 30 d。
另有学者曲霉菌定植的定义为:至少两次下呼吸道样本培养 (良好的痰液质量) 曲霉菌阳性,而无呼吸困难加重、支气管痉挛、新的肺部浸润或在先前的研究中归因于曲霉菌的症状 [17]。
然而,诡吊的是,尽管定植不同于感染,但多部位定植者却与感染患者的病死率相近 [9]。而且定植随时都会发展成为侵袭 [18]。因此,我们有理由相信,那些正在 ICU 治疗的重症患者,尤其是正在走向死亡的患者,更有可能由定植发展成为侵袭。
我们是否终于克服了定植与感染的争论?
Werner C 等认为,我们应该结束这种争论了。因为现有研究表明,大量的曲霉菌病例 (以阳性的真菌学标准) 实际中已经存在。ICU 中具有严重病毒感染的高危患者中,至少应先发制人地及时启动抗真菌治疗 [19]。
Eggimann 等认为具有多个侵袭性念珠菌感染高危因素且 CCI ≥ 0.4 的脓毒症患者更早给予抗念珠菌治疗,可降低外科重症患者侵袭性念珠菌感染确诊病例的发生率和病死率。2008 年亚太危重病论坛也指出,重症高危患者如同时具有高度念珠菌定植应予以抗念珠菌治疗 [9]。
我国指南推荐:低危和中危 IFD 患者经广谱抗生素治疗 3~5 天无效,出现持续发热等临床症状,应再次评估;同时,低风险和中风险 IFD 患者应给予治疗 [20]。
尽管组织学、微生物学水平上我们对定植和侵袭已有清晰的概念,但二者的临床判断实非易事:不同于侵袭性真菌感染可以用阳性指标判断,定植的临床判断大都是阴性指标作为判断。这种非侵袭即种植的判断存在很大的不确定性,无疑会高估定植的可能性。
自然规律中,人死后真菌繁殖,将我们化作尘埃,这是真菌称为腐生菌的积极意义。很难想象 ICU 中的大量正在走向死亡的病人,体内出现真菌不会发生这种作用;很难想象此种情况下这些真菌还会处于定植状态而不发生侵袭。
那些正在走向死亡的重症患者,即使不符合 IFD 的确诊、极似(临床)诊断、推定诊断、拟似诊断者,很多都可以诊断为未确定类,开始诊断驱动治疗 [21]。
参考文献:
1、Heylen J,etal, Acute Invasive Pulmonar y Aspergillosis: Clinical Presentation and Treatment.Semin Respir Crit Care Med 2024;45:69–87.
2、Ledoux MP, etal .Invasive Pulmonary Aspergillosis.J. Fungi 2023, 9,131
3、 Wickes BL,etal. Diagnostic Mycology: Xtreme Challenges .J Clin Microbiol. 2020 Mar 25;58(4):e01345-19.
4、Werner C,etal.Viral-associated Pulmonary Aspergillosis: Have We Finally Overcome the Debate of Colonization versus Infection? Am J Respir Crit Care Med 2023; 208: 230-231.
5、Zhang R,etal .Misdiagnosis of invasive pulmonary aspergillosis:a clinical analysis of 26 immunocompetent patients.Int J Clin Exp Med 2014;7(12):5075-5082.
6、 Blot SI,et al.A clinical algorithm to diagnose invasive pulmonary aspergillosis in critically ill patients. Am J Respir Crit Care Med. 2012 ;186(1):56-64.
7、Hamam J,et al.New clinical algorithm including fungal biomarkers to better diagnose probable invasive pulmonary aspergillosis in ICU. Ann Intensive Care .2021 ;11:41.
8、 Vandewoude KH,et al. Clinical relevance of Aspergillus isolation from respiratory tract samples in critically ill patients.Crit Care. 2006 ;10(1):R31.
9、陆国平等。呼吸道真菌定植与侵袭性真菌感染的识别。中国小儿急救医学, 2016,23(9) : 585-588,594.
10、Neil A.R, etal. Candida albicans morphogenesis and host defence:discriminating invasion from colonization .Nat Rev Microbiol. ; 2011;10(2): 112–122.
11、Aerts R,Microbiological Diagnosis of Pulmonary Aspergillus Infections. Semin Respir Crit Care Med 2024;45:21–31.
12、侵袭性真菌病真菌学检查指南. 中华检验医学杂志 2023 年 6 月第 46 卷第 6 期。541-557.
13、Brent P. et al.No n i n v a s i v e P u l m o n a r y As p e r g i l l u s In f e c t i o n s. Clin Chest Med 30 (2009) 315–335.
14、Verweij PE,etal. Review of influenza-associated pulmonary aspergillosis in ICU patients and proposal for a case definition: an expert opinion . Intensive Care Med. 2020 22;46(8):1524–1535.
15、Soontrapa P,et al .Characteristics and Outcomes of Patients with Invasive Pulmonary Aspergillosis and Respiratory Tract Aspergillus Colonization from a Tertiary University Hospital in Thailand . J Fungi (Basel). 2022 ;8(4):344.
16、Martín-Mazuelos E,et al. beta-D-Glucan and Candida albicans germ tube antibody in ICU patients with invasive candidiasis. Intensive Care Med . 2015 Aug;41(8):1424-32.
17、Barberán J,et al.Development of Aspergillosis in a cohort of non-neutropenic, non-transplant patients colonised by Aspergillus spp.BMC Infect Dis. 2017 ;17:34.
18、Barberán J,etal.Development of Aspergillosis in a cohort of non-neutropenic, non-transplant patients colonised by Aspergillus spp.BMC Infect Dis. 2017 ;17:34.
19、Werner C et al.Viral-associated Pulmonary Aspergillosis: Have We Finally Overcome the Debate of Colonization versus Infection? Am J Respir Crit Care Med 2023; 208: 230-231.
20、中国抗真菌管理共识(2024 年版)。胸腔疾病杂志》。2024;16:4016-4026.
21、中国医师协会血液科医师分会 中国侵袭性真菌感染工作组。血液病/恶性肿瘤患者侵袭性真菌病的诊断标准与治疗原则(第六次修订版)。中华内科杂志。2020;59:10):754-763.
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫