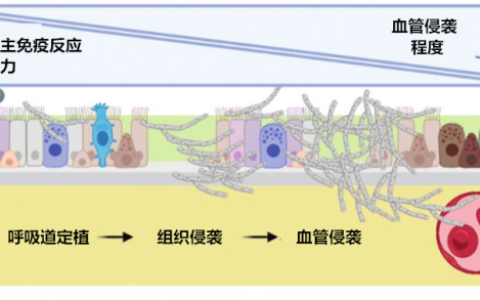
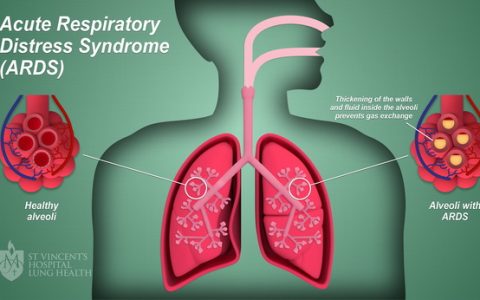
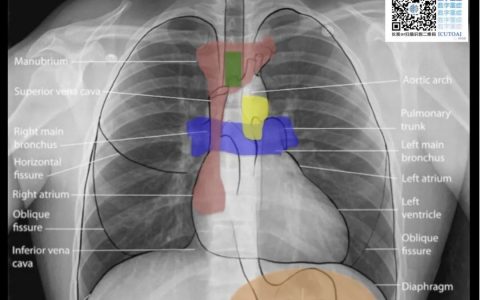
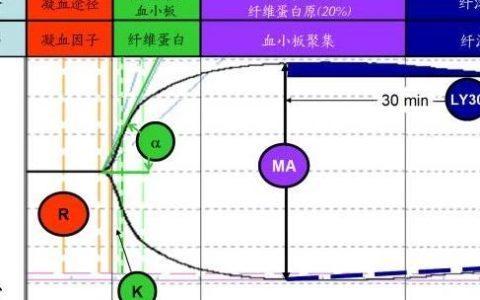
侵袭性肺曲霉病(IPA)常发生于粒细胞缺乏症等严重免疫缺陷患者[1],在入住重症加强治疗病房(ICU)的非严重免疫缺陷患者中,IPA 病例也在不断增加[2]。发生 IPA 的高危人群也在不断扩大,已从“传统因素”(如接受同种异体干细胞移植,血液系统恶性肿瘤等)扩展到“非特异因素”(如慢性阻塞性肺疾病、PTX3 基因突变等)[3-5]。重症流感被证实为 IPA 的独立危险因素之一[6-8]。44%~65% 的重症流感合并侵袭性肺曲霉病(IAPA)患者不具备任何既往诊断标准中列举的 IPA 典型宿主因素[6, 9-12],给临床早期诊断带来困扰。ICU 中 IAPA 的总病死率可高达 45%~61%[8-9, 13]。亚组分析表明无传统危险因素 IAPA 患者的病死率与具有传统风险因素的患者相当;在既往无基础疾病的“免疫正常人群”中也观察到 IAPA 病死率高达 33%~71%[8-9]。非中性粒细胞减少 IPA 患者缺乏特异性临床特征和诊断困难,其病死率甚至高于中性粒细胞减少患者(89% 比 60%)[14]。此外,气道侵袭性肺曲霉病(ITBA)的早期诊断率较低[15]。因此,IAPA 早期诊断具有迫切临床需求,诊断与治疗的延迟是导致高病死率的重要原因[9]。ICU 患者中 IPA 早期诊断一直是临床难点。在本文中,我们对多个 IPA 诊断标准进行了横向比较(表 1),对真菌学诊断新进展进行了阐述,并对 IAPA 诊断标准提出了建议。
表1 IPA 不同诊断标准的对比
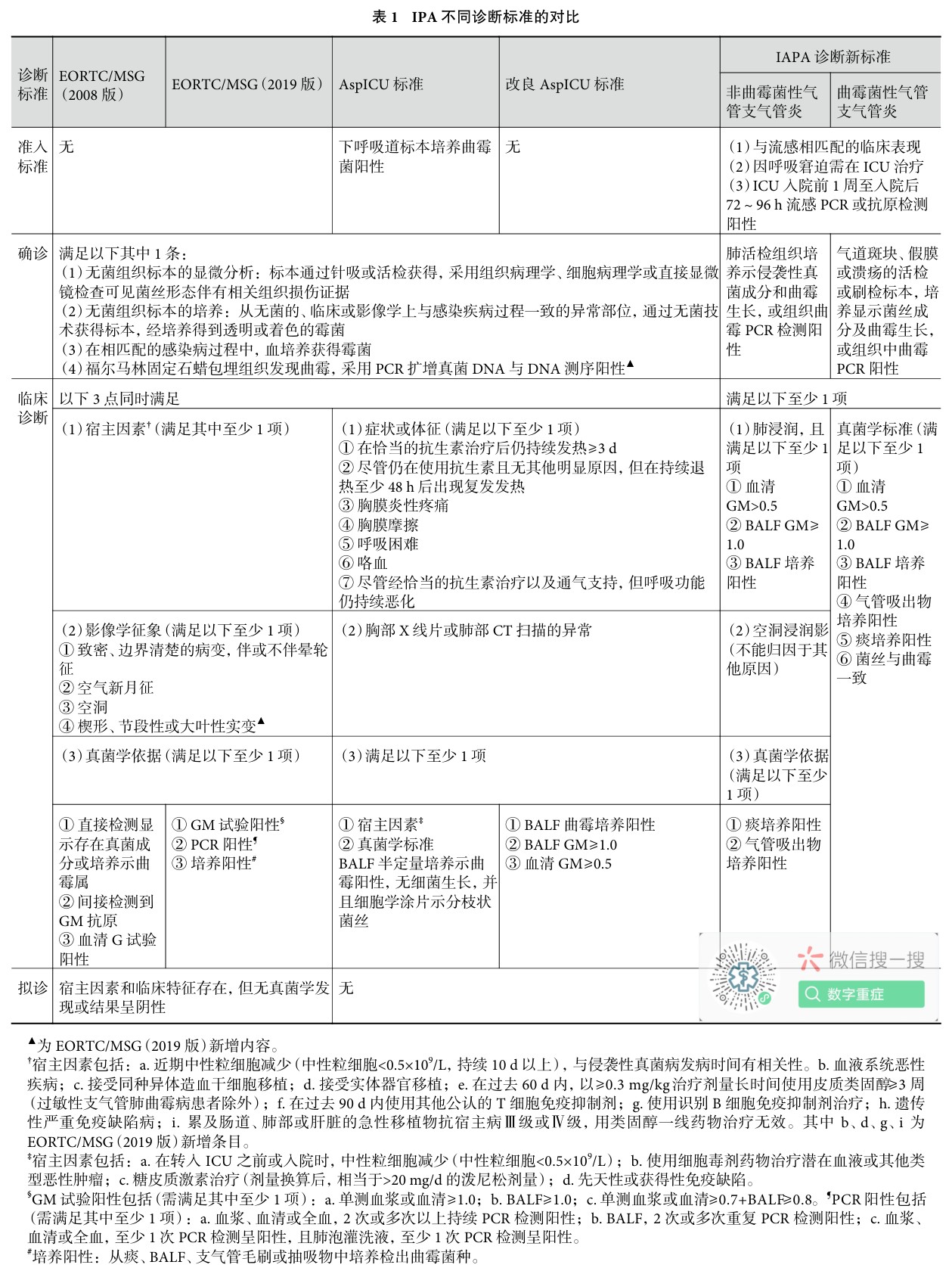
▲为 EORTC/MSG(2019 版)新增内容。
#培养阳性:从痰、BALF、支气管毛刷或抽吸物中培养检出曲霉菌种。
1 ICU 中 IPA 的不同诊断标准对比
1.1 EORTC/MSG 指南诊断标准
2019 年欧洲癌症研究和治疗组织/侵袭性真菌感染协作组和美国国立变态反应和感染病研究院真菌病研究组(EORTC/MSG)对于侵袭性真菌病的定义与诊断进行了更新,但宿主因仍为拟诊与临床诊断的必备要素之一[16]。对于 ICU 危重症患者,确诊侵袭性真菌病所要求的组织病理学证据显然是难以获得的,大多数病例只能做出拟诊或临床诊断,而 IAPA 患者很大一部分缺乏经典的免疫抑制因素[17],如果严格根据 EORTC/MSG 的定义和标准,误诊漏诊风险很高[18-19]。EORTC/MSG 在最新指南更新中也特别指出 ICU 患者应在指南更新之外单独发文进行表述。
1.2 AspICU 诊断标准
Blot 等[20]制定了一种针对 ICU 患者中区分曲霉定植和 IPA 的临床诊断策略(简称 AspICU 诊断标准)。AspICU 诊断标准要求在进行 IPA 诊断前必须首先满足患者的下呼吸道标本曲霉培养阳性这一前提,但高达 50% 的 IPA 感染下呼吸道标本培养为阴性[21],以此作为唯一的“准入标准”会导致漏诊大大增加。Schroeder 等[19]的研究结果显示,当将支气管肺泡灌洗液(BALF)的半乳甘露聚糖(GM)试验结果作为 AspICU 诊断的“准入标准”之一时,可提高 ICU 患者诊断 IPA 的敏感性。
与 EORTC/MSG 标准相比,两者的确诊标准一致,但在临床诊断和拟诊 IPA 标准上各有千秋。在真菌学诊断标准方面,相较于前者采用多种检测手段,AspICU 诊断标准中仅以 BALF 的半定量培养或细胞学涂片作为唯一真菌学诊断依据,这极大限制了其临床推广应用的价值。在宿主因素方面,相较于前者将宿主因素作为三项必备诊断要求之一,AspICU 将其与真菌学诊断证据合并为可选择项,满足二者其中一条即可。在影像学定义方面,考虑到 ICU 患者通常表现不典型,AspICU 诊断标准仅要求胸部 X 线或 CT 显示异常影像即可,而 EORTC/MSG 标准则要求具备空气新月征、空洞、致密且边界清楚的病变(伴或不伴晕轮征)或实变影(呈楔形、节段性或大叶性)征象。
1.3 改良 AspICU 诊断标准
针对 AspICU 标准及 EORTC/MSG 标准(2008 版)的不足之处,Schauwvlieghe 等[8]进行了改良(简称改良 AspICU 诊断标准),并将其应用于 ICU 重症流感患者。相较于 EORTC/MSG 标准及 AspICU 诊断标准,改良 AspICU 诊断标准不再强调宿主因素的必要性,并将 AspICU 诊断标准中的“准入标准”剔除。在真菌学诊断标准方面,改良 AspICU 诊断标准将 BALF 的曲霉培养阳性、血清 GM>0.5 或 BALF GM>1.0 结果作为证据之一。Schauwvlieghe 等[8]研究了 432 例重症流感患者,共有 83 例符合改良 AspICU 诊断标准的 IPA 定义;当采用 AspICU 诊断标准时,仅 48 例可确诊或临床诊断为 IPA,此外有 5 例被诊断为曲霉定植;当采用 EORTC/MSG 标准(2008 版)时,仅 36 例可确诊或临床诊断为 IPA。Nyga 等[15]的回顾性研究同样证实三种不同诊断标准之间存在较大的诊断差异率。如果将改良 AspICU 诊断标准的 GM 试验阈值调整为 EORTC/MSG 标准(2019 版),将有 4 例(11%)患者不再符合原有的 IPA 诊断。
1.4 对上述三项诊断标准的评价
2真菌学检测手段
2.1 血清 GM 试验
血清 GM 试验在非粒细胞缺乏患者中的敏感性较低[15],此外还受到合并抗菌药物[23]、静脉注射免疫球蛋白[24]以及基础疾病(如合并多发性骨髓瘤[25])等因素的影响。多项研究结果显示 ICU 患者的血清 GM 试验敏感性仅为 30%~50%[26-27]。在 IAPA 患者中,当以 0.5 作为 GM 试验阳性阈值时,诊断率不足 50%,这将延误患者的治疗[28]。目前 EORTC/MSG 标准(2019 版)已将单份血浆或血清 GM 试验阳性阈值上修至 1.0,但对于 IAPA 患者的最佳阈值尚不明晰,需要进一步的研究。
尽管如此,血清 GM 试验作为非侵袭性检查之一,仍推荐应用于 IAPA 患者中。但需要特别强调的是,在 ICU 临床实践中不应仅仅依赖于该检测手段,血清 GM 阴性不能排除曲霉感染。当怀疑 ICU 重症流感患者合并 IPA 感染时,相较于间隔 3~4 d 检测 1 次,早期连续 3 d 的血清 GM 试验检测更为推荐[18]。对于连续多次血清 GM 试验阴性但仍不能除外 IPA 患者,应尽早行支气管镜检查。
2.2 支气管镜及肺泡灌洗液 GM 试验
研究显示高达 25% 的 IAPA 可同时合并曲霉性支气管炎表现[29]。Nyga 等[15]的研究结果还发现,相比非 ITBA 组,ITBA 组第 30 天和第 90 天病死率均显著升高(分别为 32% 比 90%,P=0.003;44% 比 90%,P=0.02)。对于 ITBA 的诊断标准,观察到气管或支气管壁存在散在溃疡/斑块状病变或广泛的膜覆盖于黏膜表面是重要依据,而支气管镜的优势之一就在于可直视气管和支气管,并能对可疑病变部位进行活检取得组织病理学依据。
此外,支气管镜还可同时取得 BALF 行 GM 试验及核酸检测。多项研究结果显示 BALF GM 试验具有更佳的诊断效能[15, 20, 30-31],BALF GM 试验阳性高度提示 IPA,而阴性结果可基本排除 IPA 可能[32]。对于非粒细胞缺乏患者,无论以 0.5 还是 1.0 作为 BALF 标本阈值,其敏感性均显著优于血清 GM 试验(分别为 75.68% 比 37.84%,P
考虑到支气管镜检查与呼吸衰竭患者住院病死率升高密切相关[34],在进行检查前必须个体化评估患者的临床获益与风险。支气管镜虽然常作为辅助 IPA 诊断的手段之一,但在急性呼吸衰竭的 ICU 患者,该介入性操作可能造成其状况进一步恶化。但相较于手术活检等更具风险的手段而言,支气管镜检查仍然是寻求诊断证据的最佳手段之一。当非侵入性检查均未能取得证据时,早期行支气管镜是具有价值的,当疾病进展至中后期时则可能无益于诊断且易造成不良预后。此外,倘若第一次支气管检查结果呈阴性,那么除非有其他新的证据提示,否则不应重复进行该项检查[35]。
对于低氧血症患者,可预先使用高流量氧疗纠正后再进行支气管镜检查[36]。对于尚未行气管插管患者,可在接受高流量鼻导管氧疗的同时,由经验丰富的支气管镜医生进行“迷你支气管镜”(全称微型支气管肺泡灌洗,是一种不同于普通支气管镜的盲法操作,通常用于机械通气患者的下呼吸道标本获取)以快速取得标本[37]。
2.3 血与 BALF 的曲霉 PCR 核酸检测
最新的美国胸科学会临床实践指南(2019 版)首次推荐 PCR 作为免疫缺陷患者诊断 IPA 的方法之一,并指出 PCR 的便捷、快速以及高敏感性等特点具有重要的临床应用价值[38]。PCR 的突出优势在于不仅能检测出曲霉属与种,还可通过识别 CYP51A 基因突变来判断是否存在三唑类耐药可能[16, 39]。此外,Imbert 等[40]的研究还发现,PCR 拷贝数可预测患者第 90 天的病死率,当初始真菌载量150 拷贝/mL 时患者病死率可高达 73.2%(P
对于曲霉 PCR 核酸检测而言,选择合适的标本是重要的[41]。在血标本的选择上,Loeffler 等[42]的研究结果显示,相较于血清标本,血浆标本不仅能依旧保持操作简便性与低污染风险,还具有更高的敏感性以及更短的检测周期[43]。在 BALF 与血标本选择上,目前研究显示前者的检验效能更佳[44];不仅如此,Springer 等[45]的一项前瞻性研究结果显示,与未接受抗真菌预防患者相比,已行抗真菌治疗患者的血样本 PCR 阳性预测值可从 62% 直接降至 5%。但在 BALF 标本中,研究显示未观察到诊断性能的显著下降[46]。
综上,PCR(尤其是 RT-PCR)可能更适合用于可疑 IAPA 患者在拟行抗真菌治疗前的筛查以及治疗过程中的实时监测。单份 PCR 阴性结果可极大程度排除 IPA 可能[47]。此外,多项研究显示同时联合 GM 试验的检验性能更佳,采用 BALF 标本同时行 PCR 与 GM 试验的效能优于血清样本[40]。
2.4 IAPA 诊断新技术的展望
PCR 虽然具备快速、灵敏等优势,但在区分污染、定植和感染方面的能力有限[4],此外还受到检测目标范围窄、靶标较为固定、预先抗生素使用等因素的影响。宏基因二代测序技术(mNGS)具有无偏性的病原体覆盖能力,也可提供病原鉴定分型、耐药基因及毒力因子分析。此外,相较于 PCR,mNGS 可通过物种读数丰度将曲霉定植与感染区分开[4, 48]。Miao 等[49]的研究结果显示 mNGS 可在 32~36 h 内报告结果且不易受到先前抗生素使用的影响,这一点有利于 ICU 复杂感染合并多种抗生素治疗患者的诊断。当然,同样存在一些限制 mNGS 临床推广的因素,如检测成本仍偏高,人源背景 DNA 干扰结果解读,不同样本结果之间的比较分析困难等[48, 50],需要进一步改进。对于 mNGS 而言,最佳标本仍为 BALF,此外血清或气道分泌物也可用于检测。一篇关于 mNGS 在 IPA 诊断应用的病例报道显示,mNGS 可作为一种替代或补充的检测手段,帮助临床决策[51]。mNGS 在 IAPA 患者中的应用价值需要进一步的研究证实。
3 IAPA 诊断新标准
2020 年发表的 IAPA 诊断标准,由 29 名国际专家组成的团队从四个方面(包括共识定义的入选标准、宿主因素、临床特征和真菌学证据)对 IAPA 进行阐释(简称 IAPA 诊断新标准)[22],删除了 EORTC/MSG 和 AspICU 诊断标准中的宿主因素,以流感 PCR 或抗原检测呈阳性且伴有呼吸窘迫症状需入住 ICU 作为“准入标准”,将 IAPA 诊断分类为曲霉性气管支气管炎(定义:支气管镜直视下见气管和/或支气管溃疡或斑块或结节、假膜)与非曲霉性气管支气管炎两类。在确诊 IAPA 标准上,除认可组织病理学之外,病变组织的曲霉 PCR 检测阳性也可视为确诊依据之一,这一点与 EORCT/MSG(2019 版)标准的新增部分一致。在临床诊断 IAPA 标准上,非气管支气管炎患者需同时满足影像学及真菌学诊断标准,而气管支气管炎患者不需要影像学方面的证据。但 IAPA 诊断新标准尚未将血或 BALF 标本的曲霉 PCR 核酸检测纳入真菌学诊断标准之中,此外,仍以 0.5 作为单份血清 GM 试验的阳性阈值。
4 总结与展望
诊断标准的准确性直接影响治疗策略。对于 IAPA 而言,适合的诊断标准对未来的流感大环境下快速地识别出合并侵袭性肺曲霉感染患者具有重要的意义。在 2019 年新型冠状病毒肺炎(简称新冠肺炎)爆发后,已陆续有新冠肺炎合并侵袭性肺曲霉病(CAPA)的报道出现。同 IAPA 一样,CAPA 的误诊漏诊将导致病死率增加。因此,其诊断标准也成为探讨的热点话题。在新冠肺炎全球持续大流行的背景下,合理的 IAPA 诊断标准的建立将为 CAPA 的早期诊断提供重要参考。
- 1. Patterson TF, Thompson GR 3rd, Denning DW, et al. Practice Guidelines for the Diagnosis and Management of Aspergillosis: 2016 Update by the Infectious Diseases Society of America. Clin Infect Dis, 2016, 63(4): e1-e60.
- 2. Martin-Loeches I, Valles J. Overtreating or underdiagnosing invasive pulmonary aspergillosis (IPA) in critically ill H1N1 patients: who is right?. Intensive Care Med, 2012, 38(11): 1733-1735.
- 3. Bassetti M, Garnacho-Montero J, Calandra T, et al. Intensive care medicine research agenda on invasive fungal infection in critically ill patients. Intensive Care Med, 2017, 43(9): 1225-1238.
- 4. Decker SO, Sigl A, Grumaz C, et al. Immune-response patterns and next generation sequencing diagnostics for the detection of mycoses in patients with septic shock – Results of a Combined Clinical and Experimental Investigation. Int J Mol Sci, 2017, 18(8): 1796.
- 5. He Q, Li H, Rui Y, et al. Pentraxin 3 gene polymorphisms and pulmonary aspergillosis in chronic obstructive pulmonary disease patients. Clin Infect Dis, 2018, 66(2): 261-267.
- 6. Rodriguez-Goncer I, Thomas S, Foden P, et al. Invasive pulmonary aspergillosis is associated with adverse clinical outcomes in critically ill patients receiving veno-venous extracorporeal membrane oxygenation. Eur J Clin Microbiol Infect Dis, 2018, 37(7): 1251-1257.
- 7. Cavayas YA, Yusuff H, Porter R. Fungal infections in adult patients on extracorporeal life support. Crit Care, 2018, 22(1): 98.
- 8. Schauwvlieghe A, Rijnders BJA, Philips N, et al. Invasive aspergillosis in patients admitted to the intensive care unit with severe influenza: a retrospective cohort study. Lancet Respir Med, 2018, 6(10): 782-792.
- 9. Van De Veerdonk FL, Kolwijck E, Lestrade PP, et al. Influenza-associated aspergillosis in critically ill patients. Am J Respir Crit Care Med, 2017, 196(4): 524-527.
- 10. Wauters J, Baar I, Meersseman P, et al. Invasive pulmonary aspergillosis is a frequent complication of critically ill H1N1 patients: a retrospective study. Intensive Care Med, 2012, 38(11): 1761-1768.
- 11. Crum-Cianflone NF. Invasive aspergillosis associated with severe influenza infections. Open Forum Infect Dis, 2016, 3(3): ofw171.
- 12. De Pauw B, Walsh TJ, Donnelly JP, et al. Revised definitions of invasive fungal disease from the European Organization for Research and Treatment of Cancer/Invasive Fungal Infections Cooperative Group and the National Institute of Allergy and Infectious Diseases Mycoses Study Group (EORTC/MSG) Consensus Group. Clin Infect Dis, 2008, 46(12): 1813-1821.
- 13. Alshabani K, Haq A, Miyakawa R, et al. Invasive pulmonary aspergillosis in patients with influenza infection: report of two cases and systematic review of the literature. Expert Rev Respir Med, 2015, 9(1): 89-96.
- 14. Cornillet A, Camus C, Nimubona S, et al. Comparison of epidemiological, clinical, and biological features of invasive aspergillosis in neutropenic and nonneutropenic patients: a 6-year survey. Clin Infect Dis, 2006, 43(5): 577-584.
- 15. Nyga R, Maizel J, Nseir S, et al. Invasive tracheobronchial aspergillosis in critically ill patients with severe influenza. A clinical trial. Am J Respir Crit Care Med, 2020, 202(5): 708-716.
- 16. Donnelly JP, Chen SC, Kauffman CA, et al. Revision and Update of the Consensus Definitions of Invasive Fungal Disease From the European Organization for Research and Treatment of Cancer and the Mycoses Study Group Education and Research Consortium. Clin Infect Dis, 2020, 71(6): 1367-1376.
- 17. Ku YH, Chan KS, Yang CC, et al. Higher mortality of severe influenza patients with probable aspergillosis than those with and without other coinfections. J Formosan Med Assoc, 2017, 116(9): 660-670.
- 18. Koehler P, Bassetti M, Kochanek M, et al. Intensive care management of influenza-associated pulmonary aspergillosis. Clin Microbiol Infect, 2019, 25(12): 1501-1509.
- 19. Schroeder M, Simon M, Katchanov J, et al. Does galactomannan testing increase diagnostic accuracy for IPA in the ICU? A prospective observational study. Crit Care, 2016, 20(1): 139.
- 20. Blot SI, Taccone FS, Van Den Abeele AM, et al. A clinical algorithm to diagnose invasive pulmonary aspergillosis in critically ill patients. Am J Respir Crit Care Med, 2012, 186(1): 56-64.
- 21. Kaziani K, Mitrakou E, Dimopoulos G. Improving diagnostic accuracy for invasive pulmonary aspergillosis in the intensive care unit. Ann Transl Med, 2016, 4(18): 352.
- 22. Verweij PE, Rijnders BJA, Brüggemann RJM, et al. Review of influenza-associated pulmonary aspergillosis in ICU patients and proposal for a case definition: an expert opinion. Intensive Care Medicine, 2020, 46(8): 1524-1535.
- 23. Sulahian A, Touratier S, Ribaud P. False positive test for Aspergillus antigenemia related to concomitant administration of piperacillin and tazobactam. New Engl J Med, 2003, 349(24): 2366-2367.
- 24. Liu WD, Lin SW, Shih MC, et al. False-positive Aspergillus galactomannan immunoassays associated with intravenous human immunoglobulin administration. Clin Microbiol Infect, 2020, 26(11): 1555. e9-1555. e14.
- 25. Ko JH, Peck KR, Lee JY, et al. Multiple myeloma as a major cause of false-positive galactomannan tests in adult patients with cancer. J Infect, 2016, 72(2): 233-239.
- 26. Meersseman W, Lagrou K, Maertens J, et al. Galactomannan in bronchoalveolar lavage fluid: a tool for diagnosing aspergillosis in intensive care unit patients. Am J Respir Crit Care Med, 2008, 177(1): 27-34.
- 27. Lahmer T, Neuenhahn M, Held J, et al. Comparison of 1,3-β-d-glucan with galactomannan in serum and bronchoalveolar fluid for the detection of Aspergillus species in immunosuppressed mechanical ventilated critically ill patients. J Crit Care, 2016, 36: 259-264.
- 28. Van De Groep K, Verboom DM, Van De Veerdonk FL, et al. Detection of invasive aspergillosis in critically ill patients with influenza: the role of plasma galactomannan. Am J Respir Crit Care Med, 2019, 200(5): 636-638.
- 29. Verweij PE, Brüggemann RJM, Wauters J, et al. Influenza coinfection: be(a)ware of invasive aspergillosis. Clin Infect Dis, 2020, 70(2): 349-350.
- 30. Zhou W, Li H, Zhang Y, et al. Diagnostic value of galactomannan antigen test in serum and bronchoalveolar lavage fluid samples from patients with nonneutropenic invasive pulmonary aspergillosis. J Clin Microbiol, 2017, 55(7): 2153-2161.
- 31. Sehgal IS, Dhooria S, Choudhary H, et al. Utility of serum and bronchoalveolar lavage fluid galactomannan in diagnosis of chronic pulmonary aspergillosis. J Clin Microbiol, 2019, 57(3): e01821-18.
- 32. D’haese J, Theunissen K, Vermeulen E, et al. Detection of galactomannan in bronchoalveolar lavage fluid samples of patients at risk for invasive pulmonary aspergillosis: analytical and clinical validity. J Clin Microbiol, 2012, 50(4): 1258-1263.
- 33. Yu Y, Zhu C, Gao Y. Bronchoalveolar lavage fluid galactomannan as a diagnostic biomarker for IPA: still a long way to go. Crit Care, 2016, 20: 280.
- 34. Bauer PR, Chevret S, Yadav H, et al. Diagnosis and outcome of acute respiratory failure in immunocompromised patients after bronchoscopy. Eur Respir J, 2019, 54(1): 1802442.
- 35. Bauer PR, Chevret S, Azoulay E; Nine-I Investigators. Acute hypoxaemic respiratory failure in immunocompromised patients: abandon bronchoscopy or make it better?. Eur Respir J, 2019, 54(6): 1902177.
- 36. 中华医学会呼吸病学分会呼吸危重症医学学组, 中国医师协会呼吸医师分会危重症医学工作委员会. ICU 患者支气管肺泡灌洗液采集, 送检, 检测及结果解读规范. 中华结核和呼吸杂志, 2020, 43(9): 744-756.
- 37. Rijnders BJA, Schauwvlieghe AFAD, Wauters J. Influenza-associated pulmonary aspergillosis: a local or global lethal combination?. Clin Infect Dis, 2020, 71(7): 1764-1767.
- 38. Hage CA, Carmona EM, Epelbaum O, et al. Microbiological laboratory testing in the diagnosis of fungal infections in pulmonary and critical care practice. An Official American Thoracic Society Clinical Practice Guideline. Am J Respir Crit Care Med, 2019, 200(5): 535-550.
- 39. Guegan H, Robert-Gangneux F, Camus C, et al. Improving the diagnosis of invasive aspergillosis by the detection of Aspergillus in broncho-alveolar lavage fluid: comparison of non-culture-based assays. J Infect, 2018, 76(2): 196-205.
- 40. Imbert S, Gauthier L, Joly I, et al. Aspergillus PCR in serum for the diagnosis, follow-up and prognosis of invasive aspergillosis in neutropenic and non-neutropenic patients. Clin Microbiol Infect, 2016, 22(6): 562. e1-8.
- 41. Buchheidt D, Reinwald M, Hofmann WK, et al. Evaluating the use of PCR for diagnosing invasive aspergillosis. Expert Rev Mol Diagn, 2017, 17(6): 603-610.
- 42. Loeffler J, Mengoli C, Springer J, et al. Analytical Comparison ofIn Vitro-Spiked Human Serum and Plasma for PCR-Based Detection of Aspergillus fumigatus DNA: a Study by the European Aspergillus PCR Initiative. J Clin Microbiol, 2015, 53(9): 2838-2845.
- 43. Springer J, White PL, Hamilton S, et al. Comparison of performance characteristics of Aspergillus PCR in testing a range of blood-based samples in accordance with international methodological recommendations. J Clin Microbiol, 2016, 54(3): 705-711.
- 44. Eigl S, Hoenigl M, Spiess B, et al. Galactomannan testing and Aspergillus PCR in same-day bronchoalveolar lavage and blood samples for diagnosis of invasive aspergillosis. Med Mycol, 2017, 55(5): 528-534.
- 45. Springer J, Lackner M, Nachbaur D, et al. Prospective multicentre PCR-based Aspergillus DNA screening in high-risk patients with and without primary antifungal mould prophylaxis. Clin Microbiol Infect, 2016, 22(1): 80-86.
- 46. Reinwald M, Hummel M, Kovalevskaya E, et al. Therapy with antifungals decreases the diagnostic performance of PCR for diagnosing invasive aspergillosis in bronchoalveolar lavage samples of patients with haematological malignancies. J Antimicrob Chemother, 2012, 67(9): 2260-2267.
- 47. Mengoli C, Cruciani M, Barnes RA, et al. Use of PCR for diagnosis of invasive aspergillosis: systematic review and meta-analysis. Lancet Infect Dis, 2009, 9(2): 89-96.
- 48. Gabaldón T. Recent trends in molecular diagnostics of yeast infections: from PCR to NGS. FEMS Microbiol Rev, 2019, 43(5): 517-547.
- 49. Miao Q, Ma Y, Wang Q, et al. Microbiological diagnostic performance of metagenomic next-generation sequencing when applied to clinical practice. Clin Infect Dis, 2018, 67(Suppl_2): S231-S240.
- 50. Li H, Gao H, Meng H, et al. Detection of pulmonary infectious pathogens from lung biopsy tissues by metagenomic next-generation sequencing. Front Cell Infect Microbiol, 2018, 8: 205.
- 51. He BC, Liu LL, Chen BL, et al. The application of next-generation sequencing in diagnosing invasive pulmonary aspergillosis: three case reports. Am J Transl Res, 2019, 11(4): 2532-2539.
- 52. 施毅, 赵江南. 侵袭性真菌病病原学非培养实验室诊断方法. 中华结核和呼吸杂志, 2019, 42(7): 500-505.
- 53. Eigl S, Prattes J, Lackner M, et al. Multicenter evaluation of a lateral-flow device test for diagnosing invasive pulmonary aspergillosis in ICU patients. Crit Care, 2015, 19(1): 178.
- 54. Jenks JD, Mehta SR, Taplitz R, et al. Point-of-care diagnosis of invasive aspergillosis in non-neutropenic patients: aspergillus galactomannan lateral flow assay versus aspergillus-specific lateral flow device test in bronchoalveolar lavage. Mycoses, 2019, 62(3): 230-236.
本文荟萃自沈焜路, 王玉, 顾彧, 刘寅, 施毅, 苏欣. 流感相关侵袭性肺曲霉病的早期诊断. 中国呼吸与危重监护杂志, 2021, 20(7): 516-521. doi: 10.7507/1671-6205.202012058 ,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫