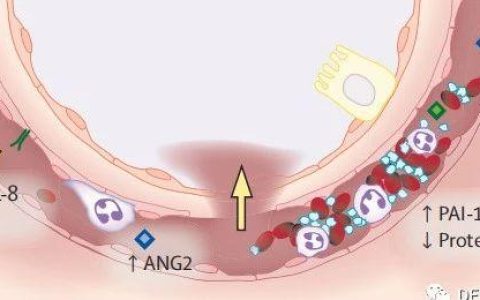
肾脏是血流丰富的人体器官,非常容易受血流灌注不足或过多以及缺氧的打击,导致肾脏功能损伤。重症患者肾功能损伤的因素多种多样,组织灌注改变是其中最重要的因素之一。维持机体合适的肾脏灌注压是肾脏保护治疗的重要环节。对于个体而言,由于基础情况不同,满足肾灌注压的最佳血压值并不一样。为此,如果临床可以实施肾脏血流灌注导向的肾脏灌注压管理,可能有利于患者的肾脏功能保护。本文将从肾脏血流的病理生理学特点,肾脏灌注监测方式,肾脏灌注相关血流动力学指标的临床应用等几个方面进行详细阐述。
1 肾脏血流的病理生理学特点
1.1 肾脏解剖结构相关的血流特点 肾脏是一个低阻力通路,尽管重量仅占体重的0.5%,但接受心输出量比例很大,在安静状态下,健康成人两肾的血流量约1200 ml/min,相当于心输出量的25%,因而肾脏是人体供血最为丰富的器官[1]。肾脏血流在不同部位其供血量并不一致,供应肾皮质的血流量约占肾血流量的94%,肾外髓部血流量约占5%,肾内髓部血流量占不到1%。生理上,肾实质组织,特别是肾髓质是在相对低氧条件下完成工作,当存在持续缺氧、微血管系统受损以及肾皮质和髓质区内炎症时,肾实质特别容易受到灌注不足和缺氧损伤,导致间质纤维化和加速肾病进展的恶性循环[2-4]。
1.2 肾脏血流的自主调节功能 肾血流量的一个重要特征是当肾动脉灌注压在一定范围内发生变化时肾血流量具有保持相对稳定的能力,临床称之为肾脏血流的自主调节能力。肾脏与颅脑、心脏(冠状动脉)都是具有较强血流自主调节能力的器官。在生理状态下,血压改变对血流影响较小。当肾动脉灌注压降低时,肾血管阻力会相应降低,而当肾动脉灌注压升高时,肾血管阻力会相应增加,因而肾血流量能保持相对恒定。早期在离体实验和人体试验中均得到证实,肾脏血流保持自主调节能力的动脉血压范围在80~180 mmHg(1 mmHg=0.133 kPa)内。
临床上肾脏血流保持自主调节功能具有非常重要的意义。如果肾动脉灌注压波动变化超出血流自主调节范围,肾脏血流量就会随着灌注压的变化而相应发生改变,产生低灌注或高灌注改变。同时,肾血流量稳定也可使肾小球滤过率保持相对稳定。如果肾血流量的自身调节功能受损,则动脉血压的较小波动就可能引起肾小球滤过率的明显波动,导致肾脏对水、钠和其他代谢产物的排泄紊乱,机体内稳态失衡。由于潜在疾病(如各种类型休克)或先前存在的基础疾病状态(如高血压),肾脏血流自主调节功能可能受损,对于终末期肾病和缺血后肾脏而言,这些代偿机制受损情况更严重。在血流自主调节功能受损患者中,低血压或高血压水平均可能会导致肾灌注进一步改变,从而导致肾功能损伤加重[5]。
1.3 肾脏灌注压 肾脏需要一定的灌注压才能保证血液进入肾脏微循环。肾脏灌注压通常是指肾动脉压与肾静脉压之差,即保证肾脏血液循环的压力,是预防肾脏缺血、保证肾脏代谢的基础。从血流的角度,肾静脉压越低越好,同时肾动脉压是影响肾脏灌注高低的最重要因素。临床上,肾动脉压不能直接测量,往往用全身动脉血压来代替。但是,从腹主动脉到肾动脉压力是梯度下降过程,肾动脉压力与全身动脉压力之间应该存在较大的差距。1991年Gosling等[6]提出最低灌注压(Pz),即临界关闭压(critical closing pressure)概念,反映肾动脉实际血流灌注情况。其计算公式:Pz=MAP-[P(s)-P(d)]/PI。MAP为平均动脉压,P(s)为收缩压,P(d)为舒张压,PI为搏动指数。只有当肾动脉压高于Pz时,才能对肾小球形成血流灌注,因此,不管血压和Pz如何变化,血压和Pz的差值可以反映肾脏实际血流灌注情况。
2 肾脏灌注的监测方法
由于肾脏灌注直接影响肾脏功能,其临床意义重大,因此,对肾灌注血流动力学指标的监测至关重要。目前常用的肾脏灌注监测方法主要包括以下几种:
2.1 肾脏超声与肾灌注评估
2.1.1 彩色多普勒(color Doppler flow imaging,CDFI) 半定量血流分级 CDFI可清晰显示肾脏各级血管血流图像,动静脉血流从肾门至皮质呈树枝状分布,血流由粗逐渐变细。CDFI可对肾脏大体血流分布及血流速度进行初步判断,但无法提供具体量化评估参数。有学者根据CDFI肾血流影像特征按照以下规则进行半定量评估,评分方式为四级法:超声检查不到肾血管评为0分;超声在肾门位置可见少许血管评为1分;超声见大部分肾实质部位显示叶间血管评为2分;整个肾脏超声见肾脏血管可显像至弓状动脉水平评为3分。该评分方法在临床上一定程度上有助于医疗工作者了解肾脏灌注情况并判断其预后。
2.1.2 彩色多普勒速度能量图(power Doppler ultrasound,PDU) PDU在用于评价肾实质的血流灌注情况上,比CDFI更具优越性,尤其是用于低流速以及低能量血流的测定。PDU是利用血液系统中红细胞的能量来显示血流的信号,彩色信号的亮度以及颜色代表着多普勒信号的能量大小,其能量大小与红细胞数量相关。在临床中,可以先应用PDU方法来获取肾脏整体灌注图像,之后再使用半定量评分方式来评估肾脏的灌注情况。陈秀凯等[7]在评估急性肾损伤(AKI)患者肾脏灌注的研究中使用PDU技术,发现PDU评分<3分与长期(>3天)连续性肾脏替代疗法(CRRT)结局密切相关。但是,不管是CDFI还是PDU都无法对较小的血管进行检测,因此对肾脏的微循环灌注情况评估是难以实现的。
2.1.3 肾动脉血流波形与肾脏阻力指数(renal resistive index,RRI) 应用CDFI或者能量多普勒技术来显示肾血管,再采用脉冲多普勒技术获取叶间动脉的血流频谱。正常的肾动脉血流频谱是低阻型,在收缩早期频谱显示为陡直上升,然后呈现缓慢下降,其收缩早期可显示有一切迹,称为收缩早期切迹。该切迹使得收缩期频谱呈现为双峰,前一个为收缩早期峰,后者为收缩晚期峰。经过手工或自动描记可获得该血管的收缩期最高速率(peak-systolic velocity,PSV),舒张期最低速率(end-diastolic velocity,EDV)和加速时间等,应用相应公式可计算得出RRI,RRI=(PSV-EDV)/PSV。在肾血管顺应性为正常的条件下,RRI同肾血管阻力呈现为线性相关性。RRI表现的是单个血管的灌注情况。RRI表达的是肾血管内EDV相较于PSV下降的比例[8],其范围是0~1,正常RRI≤0.7,双肾RRI的差异<5%,并受到年龄因素影响。在年龄<4岁和>60岁的肾功能正常受试者中,RRI 可>0.7。RRI检测方法无创、简单、可重复性好,结果不受血流角度影响。Lerolle等[9]发现如果脓毒症休克患者最初几小时内 RRI>0.74,预示可能随后出现肾功能障碍,即RRI 可用以鉴别脓毒症休克患者发生AKI的情况,可以作为发生 AKI 的预测因子。Iacoviello等[10] 研究表明,RRI>0.74是慢性心力衰竭患者12个月后肾功能指标恶化的独立危险因素。Deruddre等[11]报道应用去甲肾上腺素将脓毒症休克患者 MAP由65 mmHg升到75 mmHg,伴有 RRI 的显著性降低和尿量的显著性增加,将MAP进一步升高至85 mmHg却没发现有上述的显著性差异。这些研究结果表明在临床上可以使用 RRI来滴定式选择适当的灌注压,实现个体化治疗。
2.1.4 肾脏增强超声造影(constrast-enhanced ultrasound,CEUS) CEUS技术近年来在相关领域同样也在快速发展。CEUS是将超声增强剂微气泡注人体血液中,利用超声增强剂的特性以及特有的成像技术,从而清晰显示出含有造影剂的微小血流信号,进而反映出相应微血管的灌注情况,是目前临床上监测器官血流灌注的新技术。不同于增强CT、MRI灌注评估技术,增强超声定量分析技术使用的增强剂所含微泡直径为2~10 μm,其大小保证了其可通过血流分布到全身各组织,且不能透过血管内皮或肾脏基底膜,不会溢出到组织间或随尿液排出,且无肾毒性,该技术发生致命过敏反应概率为0.001%左右,其概率低于增强CT,与增强MRI相似,是一项非常具有临床应用前景的微循环灌注评估技术[12]。Lang等[13]首次报道在动物实验中将微气泡从狗降主动脉注入,利用肾脏超声观察血管活性药物对肾动脉血流速率的影响。Schneider等[14]对脓毒症休克患者进行研究,使用去甲基肾上腺素实现不同血压目标,然后通过CEUS技术观察相应血压下的肾脏微循环灌注情况,结果发现肾脏微循环灌注存在异质性以及在不同患者之间存在显著差异性。以上研究提示,仅仅将血压做为目标导向的肾脏灌注监测以及治疗是不够的,而临床上通过应用CEUS技术,使用肾脏微循环灌注为导向的治疗可能更有意义。
2.2 其他方法
2.2.1 近红外光谱技术(near-infrared spectroscopy,NIRS) NIRS可对局部组织氧合情况进行检测,具有无创、实时、连续、操作简便等特点,临床上得到了较多应用。其原理是应用近红外光对组织良好的穿透性,穿透皮肤后深入到组织,继而测定组织的氧饱和度。组织对近红外光进行吸收使其衰减,但不同组织成分对其吸收的程度不同,而血红蛋白是近红外光在体内吸收衰减的主要色基,因此当组织氧合发生改变时它的吸收光谱也会相应发生变化,通过计算吸收谱的比值进而就能算出组织的氧合情况[15]。在新生儿心脏手术过程中,该技术用于监测肾脏组织饱和度,其低值被发现与术后肌酐浓度增加和AKI风险有关。但是在成人患者中应用由于穿透性等因素影响,具有一定的局限性[16]。
2.2.2 血氧水平依赖性磁共振成像(blood oxygen level-dependent magnetic resonance imaging,BOLD MRI) BOLD MRI是一种无创、多用途、安全可靠的技术,可以在不暴露于辐射或外源性造影剂的情况下评估肾组织的氧合情况[17],因此这种检查可以重复进行,而无需担心不良反应。它还具有很高的空间分辨率,可以检测肾组织病理损伤前发生的功能变化,并定量反映肾氧合[18]。
BOLD MRI原理是基于脱氧血红蛋白的生理和强顺磁特性。通过测量表观松弛率(R2*)反映组织脱氧血红蛋白水平。R2*与脱氧血红蛋白水平呈正相关[19]。对缺氧反应的较高R2*值对应于的高脱氧血红蛋白水平的低氧合组织,反之亦然。通常,皮质R2*较低,从皮质到髓质R2*值呈梯度增加。最高的R2*值可在髓内区识别,与该区已确定的相对缺氧相一致[20]。在过去的20年中,BOLD MRI被广泛用于评估各种肾脏疾病条件下肾氧水平的变化,例如,缺血、高血压、糖尿病和对比性肾病以及肾病综合征、狼疮性肾炎、慢性肾病、AKI和肾移植排斥反应。
3 肾灌注压多少合适
3.1 动脉血压水平与肾灌注 生理上,动脉血压在80~180 mmHg范围内水平波动时,肾血流量具有维持恒定的能力,以确保肾小球滤过率保持恒定。各种因素影响状态下,例如炎症反应、脓毒症、容量不足、梗阻、手术干预、缺血-再灌注损伤、内源和外源性有毒性物质等,自主调节功能可能受损,表现为肾血流自动调节范围下限和上限的改变。虽然经典的生理学研究表明肾血流的自动调节功能下限MAP在50~60 mmHg[21-22],但回顾性数据表明术中MAP<55 mmHg与AKI和心肌损伤有关[23]。在274例脓毒症患者回顾性研究中证实,MAP低于75 mmHg与对肾脏替代治疗(RRT)的需求增加相关[24]。Poukkanen等[25]对423名重症脓毒症患者进行了前瞻性观察试验,观察了血流动力学参数与AKI进展之间的关系,结果证实MAP<73 mmHg是 AKI 进展的独立危险因素。Badin等[26]研究也发现72~82 mmHg的MAP对于预防感染性休克患者的AKI是必要的。针对心脏手术患者的一项小型研究显示,当MAP从60 mmHg恢复到75 mmHg时,肾氧饱和度和肾小球滤过率有所改善[27]。但是,并不是所有研究都支持高的MAP改善肾灌注,减少肾损伤发生。Asfar等[28]将脓毒症休克患者根据MAP分为两组:维持在低目标组(MAP 65~70 mmHg)与高目标组(MAP 80~85 mmHg),两组各388例,对比结果发现,患者血肌酐值成倍增长情况和RRT方面需求差异无统计学意义,90天死亡率差异也无统计学意义。但是对高血压患者进行亚组分析发现,当MAP目标达到 80~85 mmHg时,相对于低目标组,血肌酐水平以及RRT概率更低,表明在慢性高血压患者中,高目标血压组AKI发生率较低[28]。Toth等[29]在MAP为80~100 mmHg的患者中观察到稳定的肌酐水平,在MAP<80 mmHg的患者中肌酐值增加,而在MAP>100 mmHg的患者中肌酐值下降。Campos等[30]也观察到MAP<93 mmHg与移植功能不良相关。此外,Aulakh等[31]在一项关于肾移植患者研究中发现,MAP在95~131 mmHg之间的患者肌酐水平没有观察到差异,但该研究通过补充液体和多巴胺升压的方式,一直将患者的MAP始终持续维持在95 mmHg以上,整个研究中没有出现低血压病例。总而言之,这些关联说明低血压可能会带来肾脏低灌注,但增加压力并不意味着会恢复肾脏功能。目前尚不清楚评估肾微循环的最佳方法,也不清楚在不同的医疗条件下,哪种MAP可以预防AKI。
在一些研究中,通常认为平均灌注压力(mean perfusion pressure,MPP)以及舒张期灌注压力(diastolic perfusion pressure,DPP)是肾脏的有效灌注压力,而中心静脉压(CVP)以及舒张压(diastolic arterial pressure,DAP)是决定性因素。Saito等[32]报道的研究中对心脏术后患者进行分析,患者分为AKI进展组和未进展组,发现两组之间所有压力指标差异均无统计学意义,但将患者血压进行逆差计算分析,血压逆差值=(实际血压-基线血压)/基线血压,发现进展组的DAP、DPP、MPP逆差值更高,两组之间差异有统计学意义,反映其肾灌注情况偏低。
上述研究说明,考虑到潜在疾病和起病前状态,每个患者的最佳血压对于确保足够的肾灌注压和预防AKI至关重要。但是对于单个患者而言,无法定义某个具体压力数值为最佳灌注压力[5],这与严重脓毒症和脓毒性休克的拯救脓毒症运动指南的建议一致,至少维持MAP≥65 mmHg的情况下,根据患者情况个性化调整MAP值[34]。为了实现这一目标值,KDIGO指南建议将持续输注血管加压药物与补充适当的容量相结合[5],同时根据临床情况进行患者血管加压药物的个体化选择。
3.2 静脉压与肾灌注 CVP是肾脏的后向压力。正常情况下,肾小球毛细血管平均压和肾小管旁毛细血管内压分别在50和10mmHg 左右。CVP 增高,肾静脉回流障碍,肾静脉淤血,导致肾小球出球小动脉末端肾小球毛细血管的压力增高,导致净滤过压降低[35],同时,由于肾静脉淤血,肾间质压力增加,导致肾动脉阻力增加,使得肾脏有效灌注压降低[36]。在失代偿性心功能衰竭患者中,CVP增高 (>8 mmHg)是AKI 发生、进展的最重要原因[37]。CVP≥11 mmHg时,肾功能不全风险增加了两倍[30]。Legrand等[33]研究发现与脓毒症 AKI 进展密切相关的血流动力学指标是低舒张血压和高 CVP。为此,临床管理中CVP越低越好的管理策略可能有助于肾脏灌注的维持。
4 未来研究方向和展望
肾血流自主调节的机制分为肌源性学说和管-球反馈学说,而肾血流量还可通过神经和体液调节,有大量的文献研究报道这些调节方式的分子生物学机制。未来进一步的研究,有助于我们进一步了解这些重要的基本调控机制中的分子生物学事件,并且随着临床肾脏灌注监测方法学的不断进步,可以实现肾脏血流调节功能的评价[38]。由此,寻找到理想肾脏血流和氧合的个体化肾脏灌注压成为希望。
[1] Calixto Fernandes MH,Schricker T,Magder S,et al.Perioperative fluid management in kidney transplantation:a black box[J].Crit Care,2018,22(1):14.
[2] Hirakawa Y,Tanaka T,Nangaku M.Renal hypoxia in CKD;pathophysiology and detecting methods[J].Front Physiol,2017,8:99.
[3] Haase VH.Mechanisms of hypoxia responses in renal tissue[J].J Am Soc Nephrol,2013,24(4):537-541.
[4] Heyman SN,Rosen S,Rosenberger C.Renal parenchymal hypoxia,hypoxia adaptation,and the pathogenesis of radiocontrast nephropathy[J].Clin J Am Soc Nephrol,2008,3(1):288-596.
[5] Meersch M,Zarbock A.Renal protection in the 21st century[J].Curr Opin Crit Care,2016,22(6):554-559.
[6] Gosling RG,Lo PT,Taylor MG.Interpretation of pulsatility index in feeder arteries to low-impedance vascular beds[J].Ultrasound Obstet Gynecol,1991,1(3):175.
[7] 陈秀凯,黄立锋,王小亭,等.能量多普勒超声对急性肾损伤的评估价值[J].中华医学杂志,2012,92(47):3354-3357.
[8] 胡振杰,刘丽霞.超声与急性肾损伤肾灌注评价[J].中国实用内科杂志,2017,37(8):690-693.
[9] Lerolle N,Guérot E,Faisy C,et al.Renal failure in septic shock:predictive value of Doppler-based renal arterial resistive index[J].Intensive Care Med,2006,32(10):1553-1559.
[10] Iacoviello M,Monitillo F,Leone M,et al.The renal arterial resistance index predicts worsening renal function in chronic heart failure patients[J].Cardiorenal Med,2016,7(1):42-49.
[11] Deruddre S,Cheisson G,Mazoit JX,et al.Renal arterial resistance in septic shock:effects of increasing mean arterial pressure with norepinephrine on the renal resistive index assessed with Doppler ultrasonography[J].Intensive Care Med,2007,33(9):1557-1562.
[12] Wang L,Mohan C.Contrast-enhanced ultrasound:a promising method for renal microvascular perfusion evaluation[J].J Transl Int Med,2016,4(3):104-108.
[13] Lang RM,Feinstein SB,Powsner SM,et al.Contrast ultrasonography of the kidney:a new method for evaluation of renal perfusion in vivo[J].Circulation,1987,75(1):229-234.
[14] Schneider AG,Goodwin MD,Schelleman A,et al.Contrast-enhanced ultrasonography to evaluate changes in renal cortical microcirculation induced by noradrenaline:a pilot study[J].Crit Care,2014,18(6):653.
[15] Biedrzycka A,Lango R.Tissue oximetry in anaesthesia and intensive care[J].Anaesthesiol Intensive Ther,2016,48(1):41-48.
[16] Owens GE,King K,Gurney JG,et al.Low renal oximetry correlates with acute kidney injury after infant cardiac surgery[J].Pediatr Cardiol,2011,32(2):183-188.
[17] Ebrahimi B,Textor SC,Lerman LO.Renal relevant radiology:renal functional magnetic resonance imaging[J].Clin J Am Soc Nephrol,2014,9(2):395-405.
[18] Chen F,Li S,Sun D.Methods of blood oxygen level-dependent magnetic resonance imaging analysis for evaluating renal oxygenation[J].Kidney Blood Press Res,2018,43(2):378-388.
[19] Niles DJ,Gordon JW,Fain SB.Effect of anesthesia on renal R2* measured by blood oxygen level-dependent MRI[J].NMR Biomed,2015,28(7):811-817.
[20] Zheng Z,Shi H,Ma H,et al.Renal oxygenation characteristics in healthy native kidneys:assessment with blood oxygen level-dependent magnetic resonance imaging[J].Nephron Physiol,2014,128(3-4):47-54.
[21] Bayliss WM.On the local reactions of the arterial wall to changes of internal pressure[J].J Physiol,1902,28(3):220-231.
[22] Harper AM.Autoregulation of cerebral blood flow:influence of the arterial blood pressure on the blood flow through the cerebral cortex[J].J Neurol Neurosurg Psychiatry,1966,29(5):398-403.
[23] Walsh M,Devereaux PJ,Garg AX,et al.Relationship between intraoperative mean arterial pressure and clinical outcomes after noncardiac surgery:toward an empirical definition of hypotension[J].Anesthesiology,2013,119(3):507-515.
[24] Dünser MW,Takala J,Ulmer H,et al.Arterial blood pressure during early sepsis and outcome[J].Intensive Care Med,2009,35(7):1225-1233.
[25] Poukkanen M,Wilkman E,Vaara ST,et al.Hemodynamic variables and progression of acute kidney injury in critically ill patients with severe sepsis:data from the prospective observational FINNAKI study[J].Crit Care,2013,17(6):R295.
[26] Badin J,Boulain T,Ehrmann S,et al.Relation between mean arterial pressure and renal function in the early phase of shock:a prospective,explorative cohort study[J].Crit Care,2011,15(3):R135.
[27] Redfors B,Bragadottir G,Sellgren J,et al.Effects of norepinephrine on renal perfusion,filtration and oxygenation in vasodilatory shock and acute kidney injury[J].Intensive Care Med,2011,37(1):60-67.
[28] Asfar P,Meziani F,Hamel JF,et al.High versus low blood-pressure target in patients with septic shock[J].N Engl J Med,2014,370(17):1583-1593.
[29] T th M,Réti V,Gondos T.Effect of recipients’ peri-operative parameters on the outcome of kidney transplantation[J].Clin Transplant,1998,12(6):511-517.
th M,Réti V,Gondos T.Effect of recipients’ peri-operative parameters on the outcome of kidney transplantation[J].Clin Transplant,1998,12(6):511-517.
[30] Campos L,Parada B,Furriel F,et al.Do intraoperative hemodynamic factors of the recipient influence renal graft function?[J].Transplant Proc,2012,44(6):1800-1803.
[31] Aulakh NK,Garg K,Bose A,et al.Influence of hemodynamics and intra-operative hydration on biochemical outcome of renal transplant recipients[J].J Anaesthesiol Clin Pharmacol,2015,31(2):174-179.
[32] Saito S,Uchino S,Takinami M,et al.Postoperative blood pressure deficit and acute kidney injury progression in vasopressor-dependent cardiovascular surgery patients[J].Crit Care,2016,20(1):74.
[33] Legrand M,Dupuis C,Simon C,et al.Association between systemic hemodynamics and septic acute kidney injury in critically ill patients:a retrospective observational study[J].Crit Care,2013,17(6)):R278.
[34] Dellinger RP,Levy MM,Rhodes A,et al.Surviving sepsis campaign:international guidelines for management of severe sepsis and septic shock,2012[J].Intensive Care Med,2013,39(2):165-228.
[35] Verbrugge FH,Grieten L,Mullens W.Management of the cardiorenal syndrome in decompensated heart failure[J].Cardiorenal Med,2014,4(3-4):176-88.
[36] Braam B,Cupples WA,Joles JA,et al.Systemic arterial and venous determinants of renal hemodynamics in congestive heart failure[J].Heart Fail Rev,2012,17(2):161-175.
[37] Mullens W,Abrahams Z,Francis GS,et al.Importance of venous congestion for worsening of renal function in advanced decompensated heart failure[J].J Am Coll Cardiol,2009,53(7):589-596.
[38] Carlström M,Wilcox CS,Arendshorst WJ.Renal autoregulation in health and disease[J].Physiol Rev,2015,95(2):405-511.
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫