Chestnut Studying
摘要
Sepsis is a complex clinical syndrome marked by dysregulated immune responses, systemic inflammation, and subsequent organ dysfunction. Sepsis involves the interplay of multiple signaling pathways. Traditional sepsis treatment mainly depends on antibiotics and early directed therapy, with limited effectiveness. This article reviews major signaling pathways in sepsis, such as those related to nuclear factor κB (NF-κB), Janus kinase/signal transducer and activator of transcription (JAK/STAT), Toll-like receptors (TLRs), mitogen-activated protein kinase (MAPK), hypoxia-inducible factor 1α (HIF-1α), and nuclear factor-erythroid 2-related factor 2/Kelch-like ECH-associated protein 1 (Nrf2/Keap1). These molecules are pivotal in regulating immune activation, inflammation, and immune cell metabolism. Moreover, mitochondrial dysfunction and metabolic reprogramming substantially contribute to sepsis development, as they greatly affect energy production and immune cell function. Selectively inhibiting these pathways shows potential for effectively reducing hyperinflammation and preventing organ failure. We discussed how future research on these signaling pathways can translate into clinical applications and how personalized treatment strategies can handle the complexity and variability of sepsis. Given the dynamic nature of sepsis, treatment strategies should not solely rely on traditional single-target interventions. Instead, a dynamic and personalized multi-target modulatory approach is needed. While reducing side effects of single-target inhibition, inflammatory responses, immune balance, and metabolic disorders can be more precisely regulated. By precisely monitoring multiple sepsis-related signaling pathways and adjusting treatment regimens in real time, we aim to identify more effective intervention points in the complex dynamics of diseases, thus providing new hope for improving prognosis of septic patients.
脓毒症是一种复杂的临床综合征,以免疫反应失调、全身炎症和随后的器官功能障碍为特征。脓毒症涉及多种信号通路的相互作用。传统的脓毒症治疗主要依赖抗生素和早期指导治疗,效果有限。本文回顾了脓毒症中的主要信号通路,如与核因子κB(NF-κB)、Janus 激酶/信号转导和转录激活因子(JAK/STAT)、Toll 样受体(TLRs)、丝裂原活化蛋白激酶(MAPK)、缺氧诱导因子 1α (HIF-1α)和核因子红细胞 2 相关因子 2/Kelch 样 ECH 相关蛋白 1(Nrf2/Keap1)有关的信号通路。这些分子在调节免疫激活、炎症和免疫细胞代谢方面起着关键作用。此外,线粒体功能障碍和代谢重编程也是脓毒症发生的重要原因,因为它们极大地影响了能量的产生和免疫细胞的功能。选择性地抑制这些通路显示出有效减轻高炎症和预防器官衰竭的潜力。我们讨论了未来对这些信号通路的研究如何转化为临床应用,以及个性化治疗策略如何应对脓毒症的复杂性和多变性。鉴于脓毒症的动态性质,治疗策略不应仅仅依赖于传统的单一目标干预。相反,需要一种动态和个性化的多靶点调节方法。在减少单一靶点抑制副作用的同时,还能更精确地调节炎症反应、免疫平衡和代谢紊乱。通过精确监测多种脓毒症相关信号通路并实时调整治疗方案,我们希望在复杂的疾病动态变化中找出更有效的干预点,从而为改善脓毒症患者的预后带来新的希望。
前言
2016 年脓毒症 3.0 定义将脓毒症描述为因宿主对感染的反应失调而导致的危及生命的器官功能障碍。脓毒症对全身的影响极大地影响了免疫功能。一方面,免疫反应的过度激活会导致过度炎症状态。另一方面,过度的炎症反应可能会引发免疫抑制。这种免疫抑制会使宿主的免疫系统功能失调,容易继发感染。因此,脓毒症的临床治疗变得更加复杂。尽管医学科学在不断进步,但脓毒症的治疗仍然是一个巨大的挑战。作为初步干预措施,标准化治疗方案已经实施,如早期目标导向疗法和广谱抗生素给药。然而,由于脓毒症表现的异质性和患者反应的差异性,这些方法存在局限性。
尽管脓毒症研究领域取得了诸多进展,但仍存在明显不足。一方面,包括核因子κB(NF-κB)和Janus 激酶/信号转导和激活转录因子(JAK/STAT)在内的多种信号通路已被证实与脓毒症密切相关。然而,在不同的个体遗传背景、原有疾病状况以及脓毒症进展的不同阶段下,它们相互作用网络的具体机制仍未完全阐明。另一方面,现有的脓毒症靶向药物在临床试验中表现出不同的疗效和安全性问题。例如,细胞因子抑制剂已证明可降低 1 个月的死亡率和严重不良事件的风险。相反,Toll 样受体 4(TLR4)拮抗剂则与不良事件风险增加有关。目前,还缺乏有效的方法来准确预测脓毒症患者对特定靶向药物的治疗反应。此外,监测脓毒症患者的免疫功能对于脓毒症的治疗也至关重要。然而,白细胞计数和 C 反应蛋白等传统指标缺乏敏感性和特异性。最近的研究突出强调了先进的生物标志物和技术,如程序性死亡 1/ 程序性死亡配体 1(PD-1/PD-L1)、人类白细胞抗原-DR(HLA-DR)、特异性细胞因子谱以及流式细胞术等创新技术,它们能更精确地洞察脓毒症患者的免疫状态。这表明,建立精确、动态的免疫监测指标体系,对于准确评估脓毒症患者的免疫功能、预测疾病预后至关重要。
在脓毒症的诊断和治疗中,一直存在着临床难题和尚未满足的医疗需求。这些都促使学术界将深入探索脓毒症的病理机制及相关信号通路作为制定精准治疗策略的核心方向。本综述重点探讨了脓毒症进展过程中与免疫反应和代谢紊乱相关的关键信号通路。它系统地整合了临床前实验数据和临床研究证据,以及分子和细胞生物学的最新研究成果。
研究主要分析了核心信号通路,包括 NF-κB、JAK/STAT 和 TLR。此外,研究还深入解读了这些通路如何调控脓毒症的各种病理过程。这些过程包括免疫调节失衡、炎症反应失控、线粒体功能障碍和代谢重编程。我们揭示了每种信号通路的分子靶点及其上下游调控关系。然后,结合临床实践中患者的个体差异,探讨基于这些信号通路的潜在治疗策略。这项研究不仅为脓毒症创新靶向疗法的开发提供了理论依据,还致力于推动个性化医疗策略的发展,实现治疗方案的精准定制。随着我们对脓毒症复杂的细胞信号网络和代谢重塑机制认识的不断深入,我们有望开发出新一代的治疗干预方法。这些方法可以降低疾病的复杂性,提高患者的存活率。
本综述对具有治疗潜力的信号通路进行了深入分析,进一步凸显了靶向治疗策略在应对脓毒症这一全球性健康问题中的重要性,为改善脓毒症患者的临床预后奠定了坚实的理论基础。
脓毒症中的免疫调节
脓毒症是一种复杂且危及生命的疾病,涉及免疫反应失调。脓毒症免疫反应的多样性受年龄(尤其是幼儿和老年人)、感染类型和部位、遗传和治疗策略等因素的影响。脓毒症期间,免疫系统的激活是由一系列模式识别受体(PRR)触发的,模式识别受体是位于免疫细胞表面或细胞内部的受体。这些受体可检测到微生物衍生的病原体相关分子模式(PAMPs),如细菌的脂多糖或病毒核酸,或受损宿主细胞释放的内源性损伤相关分子模式(DAMPs),从而启动宿主的免疫反应。这种识别随后会诱导细胞因子和其他炎症介质的释放,或引发细胞死亡。一旦被检测到,这种识别事件就会引发连锁反应,导致细胞因子和其他炎症介质的释放,甚至引发细胞死亡。这种最初的免疫激活是机体抵御病原体入侵的基本防御机制。
然而,脓毒症的特点是免疫系统严重失调。其主要特征是双相免疫功能失调,包括最初的压倒性炎症反应和随后的免疫抑制阶段。这种双相模式是脓毒症病理生理学的基础。早期的高炎症反应阶段是由于白细胞和内皮细胞不受控制的激活,导致促炎症反应。同时,这会引发氧和氮自由基、细胞因子的产生失调,以及补体和凝血系统的激活。因此,尽管这些机制的激活代表了机体对感染的先天免疫反应,但炎症反应和调节反应之间的失衡会导致过度免疫造成组织损伤,加速脓毒症的进展。
在不同的患者中,脓毒症的自然进展表现出不同的不良影响。尽管抗生素治疗和支持性护理提高了存活率,但有效控制疾病进展仍是一项巨大挑战。造成这一挑战的部分原因是患者免疫失衡的异质性尚未得到解决。每位患者的免疫系统对脓毒症的反应不同,了解这些个体差异对于制定个性化治疗策略至关重要。
NF-κB 信号通路
NF-κB 信号传导是免疫反应的基本调节因子,可分为两种不同的途径:经典(标准)途径和非经典(替代)途径。当 PRRs(如 TLRs)识别到 PAMPs 时,就会启动一个复杂的信号级联。这一级联最终导致 NF-κB 的激活和核转位。这种转位启动了促炎细胞因子、趋化因子和粘附分子的转录表达。受到刺激后,IκB 激酶(IKK)复合物将 IκB 磷酸化,导致其泛素化和蛋白酶体降解。这一过程释放出 NF-κB 二聚体,使其能够进行核转位,进而激活基因。NF-κB 二聚体可转位到细胞核中。一旦进入细胞核,它们就会与特定的 DNA 靶点结合。这种结合会促进肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)和 IL-6 等炎症细胞因子的转录。
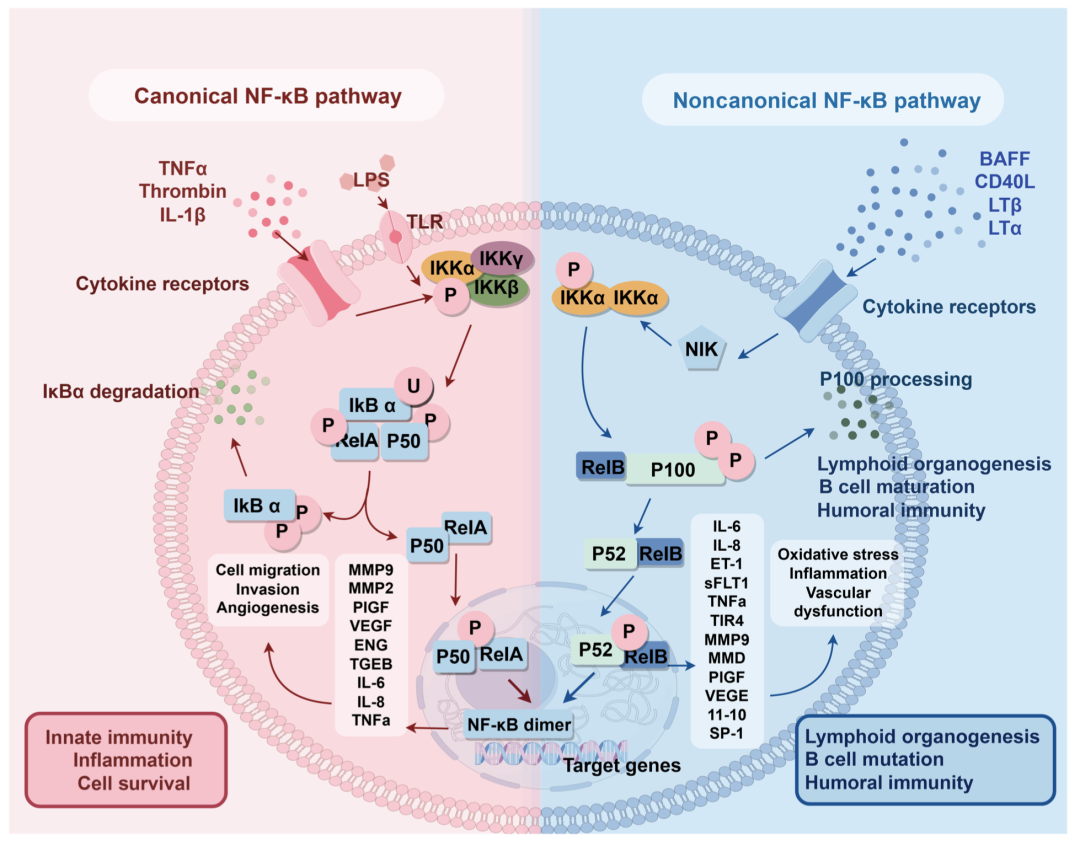
经典的 NF-κB 通路是众所周知的免疫反应启动机制,而非经典的 NF-κB 信号通路也在各种生理过程中发挥着重要作用。它可由 CD40 配体、淋巴毒素 β(LTβ)和细菌脂多糖(LPS,也称内毒素)启动,导致 NF-κB 诱导激酶(NIK)活化。这一途径意味着蛋白质的合成;因此,它的运行动力学与传统途径不同。它在造血发育、次级淋巴器官的形成和免疫平衡的维持中起着至关重要的作用。图1 是经典和非经典 NF-κB 通路的机制示意图。
促炎细胞因子与 NF-κB 信号通路之间的相互作用使其在免疫反应中的作用更加复杂。促炎细胞因子通过自分泌机制维持 NF-κB 信号通路,这种级联反应有利于将免疫细胞招募到感染部位,从而促进病原体的清除。尽管如此,在脓毒症的情况下,NF-κB 的长期激活会导致持续的炎症反应,最终造成广泛的组织损伤和器官衰竭。
值得注意的是,NF-κB 的功能不仅限于促进炎症反应。它还能调节与抗炎途径和组织修复相关的基因的表达,从而突出其在传播和解决炎症方面的双重作用。在脓毒症中,这种微妙的平衡经常被打破。NF-κB 的过度激活会阻碍炎症的消退,造成持续的组织损伤。相反,脓毒症晚期 NF-κB 活性不足会损害组织修复,导致慢性免疫抑制。由于 NF-κB 在脓毒症中起着核心作用,因此它是一个很有前景的治疗靶点。通过调节其活性,我们可以增强其保护作用,同时将其有害影响降至最低。
JAK/STAT 信号通路
有一组细胞因子,如 IL-6、IL-11 和 oncostatin M(OSM),可通过共同受体亚基糖蛋白 130(gp130)发出信号,激活下游的 JAK/STAT 通路。同时,它还会导致 STAT 家族转录因子的招募和磷酸化。这组介质有时被称为 IL-6 型细胞因子。脓毒症期间,1 型和 2 型细胞因子受体也会使用 JAK/STAT 信号途径。该途径介导了 IL-6 和干扰素-γ(IFN-γ)的信号传导。当细胞因子与其特定受体结合时,JAK 被激活。这种活化会导致 STAT 蛋白磷酸化,进而激活 STAT 蛋白。活化的 STAT 蛋白会转运到细胞核并调节基因表达。这种调控控制着免疫细胞的分化、炎症介质的产生以及细胞的存活和凋亡过程。JAK/STAT 信号通路与各种细胞因子和炎症介质的分泌有关,如 IL-6、IL-10、诱导型一氧化氮合酶(iNOS)和高迁移率基团蛋白 B1(HMGB1)。这一途径在调节对脓毒症的免疫反应中起着至关重要的作用。
典型的 JAK/STAT 信号通路通常由细胞外信号分子(包括细胞因子、生长因子和/或激素)启动,这些分子与特定的细胞表面受体结合。这触发了相邻 JAK 激酶的磷酸化和活化。活化的 JAK 激酶使受体上的特定酪氨酸残基磷酸化,这些残基成为 STAT 蛋白招募的对接位点。这种招募促进了 JAK 激酶对 STAT 蛋白的磷酸化。在特定情况下,STAT 蛋白可以不依赖 JAK 而被激活。这种激活可通过两种主要的替代机制进行。一种是通过生长因子受体。另一种是通过非受体酪氨酸激酶,如 Src 家族激酶。这些激酶可直接使 STAT 蛋白磷酸化。在后来的代偿性抗炎反应综合征(CARS)中,STAT3 抑制剂(如舒尼替尼或阿西替尼)可阻止髓源性抑制细胞的招募。研究表明,抑制 JAK3 和 STAT3 可减少内皮粘附分子的过度表达,从而缓解与脓毒症相关的血管麻痹、凝血功能障碍和多器官功能衰竭(MOF)等病理情况。
除了 JAK/STAT 信号通路的主要成分外,还有几种蛋白质有助于 STAT 依赖性转录过程,并促进 JAK/STAT 信号通路与其他信号通路的相互作用。这些蛋白统称为 JAK/STAT 信号转导调节因子。在糖皮质激素与催乳素协同作用的环境中,活化的 STAT5 与 GR 结合形成功能复合物,其中 GR 发挥 STAT5 的转录辅激活剂的作用,从而增强 STAT5 依赖基因的转录活性。与此同时,负调控因子在调节 JAK/STAT 信号通路方面也发挥着至关重要的作用,从而共同促进其稳定性和平衡性。JAK/STAT 信号通路有 3 种主要的负调控机制。它们分别由细胞因子信号转导抑制蛋白(SOCS)、活化 STAT 蛋白抑制蛋白(PIAS)和蛋白酪氨酸磷酸酶(PTPs)介导。其中,SOCS 蛋白通过削弱 JAK/STAT 通路的信号活性,在调节 JAK/STAT 通路方面发挥着重要作用。激活的 STAT 蛋白进入细胞核触发 SOCS 转录。然后,SOCS 蛋白通过利用其 N 端激酶抑制结构域阻止 STAT 与受体结合,或通过促进 JAK 或 STAT 的泛素化和蛋白酶体降解,使 JAK 激酶失活,从而负向调节 JAK/STAT 信号通路。通过调节 JAK/STAT 信号通路,这些抑制剂有可能在维持免疫反应的同时减轻高炎症反应。
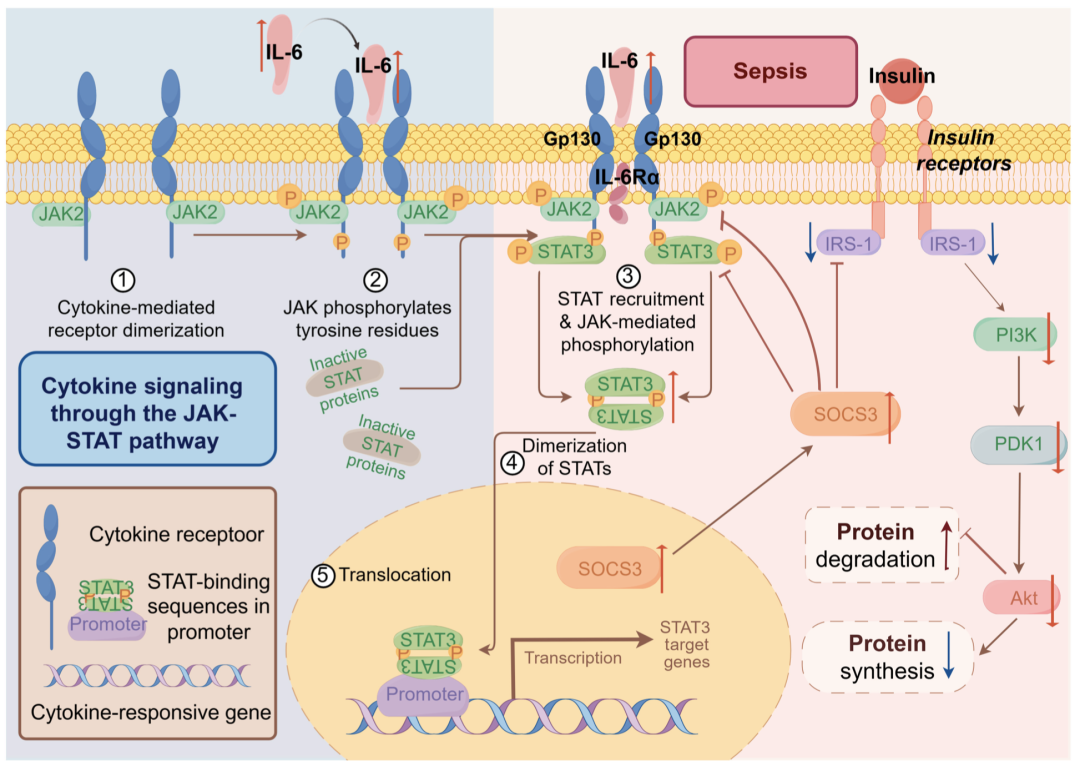
JAK/STAT 通路调节脓毒症期间免疫细胞的命运和功能。例如,IL-6 可激活 STAT3,STAT3 最初可在脓毒症中提供抗炎保护,但其长期激活可能会导致免疫瘫痪。相反,IFN-γ 激活 STAT1,引发对病原体清除至关重要的促炎反应,但如果不加以控制,可能会加剧组织损伤。JAK/STAT 信号传导中这些对立作用之间的平衡对脓毒症的预后至关重要,因此该通路成为一个很有前景的治疗靶点(图2 )。
虽然 JAK/STAT 抑制剂在脓毒症中的临床应用尚未见报道,但其在炎症性疾病和癌症中的治疗用途已得到充分证实。JAK 抑制剂主要抑制下游 STAT 蛋白的活化,并通过靶向 JAK 家族成员阻断炎症因子的信号传导。JAK/STAT 通路抑制剂在疾病治疗领域取得了显著成果,但仍面临诸多挑战。未来,深入探索JAK/STAT通路的调控机制,开发具有高选择性、低副作用的新型抑制剂将是一个重要的研究方向,有望为脓毒症等相关疾病的治疗带来新的突破。
TLR 信号通路
TLRs 是一种 PRRs,在先天性免疫系统中起着主要应答器的作用。它们能识别被称为 PAMPs 的保守微生物结构,从而启动免疫反应。在脓毒症的病理过程中,TLR4 和 TLR2 作为模式识别受体家族的重要成员,凭借其独特的结构特征和配体结合机制,在介导宿主免疫反应方面发挥着重要作用。
TLR4 作为识别革兰氏阴性细菌的主要受体,对细菌细胞壁的一种成分 LPS 具有高度特异性的识别能力。通过与 TLR4 结合,LPS 触发一系列级联反应,诱导宿主免疫细胞释放多种炎症因子,从而推动脓毒症的病理发展。激活后,该受体通过两种信号通路协调调节炎症反应过程,即髓样分化因子 88(MyD88)依赖性通路和 MyD88 非依赖性通路。MyD88依赖途径主要激活NF-κB和丝裂原活化蛋白激酶(MAPK)信号转导途径,促进TNF-α和IL-6等促炎细胞因子的表达。另一方面,不依赖于 MyD88 的途径则通过含 TIR 结构域的适配器诱导干扰素-β(TRIF)介导的信号转导参与免疫调节。这种双途径调控模式赋予了 TLR4 在炎症反应和维持免疫稳态方面复杂而微妙的调控功能。与 TLR4 不同,TLR2 在识别革兰氏阳性细菌方面起着至关重要的作用。它的主要识别配体包括细菌细胞壁成分,如脂肽和脂硫代尿酸。识别 PAMPs 后,TLR2 通过 MyD88 依赖性信号通路招募下游适配蛋白,激活 NF-κB 和 MAPK 信号通路。
TLR 信号通路的激活会迅速产生促炎细胞因子和趋化因子,它们在控制感染方面发挥着至关重要的作用。虽然 TLR 信号通路对病原体识别和免疫激活至关重要,但在脓毒症期间过度或长时间激活会产生有害影响。研究表明,在 TLR4 缺失的小鼠中,LPS 诱导的肝损伤会导致多种后果。肝酶水平降低,肝组织形态发生变化。此外,还会出现氧化应激,并引发细胞凋亡,所有这些都与野生型对照组不同。这表明 TLR4 的持续激活会对肝脏等器官产生有害影响。因此,抑制 TLR 信号转导是一种潜在的治疗策略,可用于控制过度炎症、解决系统性自身免疫性疾病和管理系统性脓毒症反应。研究人员对各种治疗方法进行了研究。这些方法包括使用 TLR 拮抗剂、TLR 特异性单克隆抗体(mAbs)和小分子药物,以防止 TLR 激活或阻断其下游信号通路。值得注意的是,合成脂质 TLR4 拮抗剂 Eritoran 已在临床前研究中证明能够减轻 LPS 诱导的炎症并提高脓毒症模型的存活率。为了实现更平衡的免疫反应,研究人员开发出了更全面、更成熟的方法。这些方法主要集中在两个方面:选择性靶向特定 TLRs 和调节其信号通路,通常与其他治疗策略相结合。总之,脓毒症涉及通过 NF-κB、JAK/STAT 和 TLR 通路进行的复杂免疫调节,强调了靶向疗法的必要性。探索这些机制可以发现新的治疗靶点,以减少脓毒症相关损伤并促进免疫恢复。
微生物组代谢途径
肠道微生物组已被认为是脓毒症发病机制中的一个关键因素,其重要性超过了以往的估计。脓毒症期间,宿主的代谢过程和免疫反应都会发生紊乱,其中肠道微生物组起着至关重要的调节作用。据推测,胃肠道系统是脓毒症诱发的多器官功能障碍综合征(MODS)的 “始作俑者”,在触发和维持全身炎症反应的各种机制中起着重要作用。临床上经常观察到脓毒症患者肠道菌群失调,其特点是肠道微生物群失衡,与不良预后相关。具体而言,醋酸酯、丙酸酯和丁酸酯等 SCFAs 已被证明在细菌群落与免疫系统之间的信号传递过程中发挥作用。除 SCFAs 外,肠道微生物群的多种代谢产物如氨基酸及其代谢衍生物在脓毒症的发生和发展中也起着至关重要的作用。例如,一些微生物代谢产物可上调铁转运蛋白的表达,转运蛋白可通过与 CD14 的相互作用发挥免疫抑制功能,特别是通过抑制 PRR 信号转导,从而诱导宿主免疫耐受。脓毒症患者常表现出氨基酸代谢紊乱,这可能导致免疫功能下降和肠屏障损伤。例如,L-缬氨酸是一种重要的氨基酸,其代谢物水平的降低与脓毒症患者的不良预后密切相关。这表明氨基酸代谢物可作为脓毒症的潜在生物标志物,从而为临床诊断和治疗提供新的见解。吲哚-3-丙酸(IPA)是一种肠道微生物群代谢产物,主要来源于色氨酸,具有显著的抗炎作用。IPA 可上调抗炎因子的表达,抑制促炎因子的分泌,从而在脓毒症等炎症中发挥保护作用。在脓毒症小鼠中,IPA 治疗可降低血清中炎症介质的水平,提高存活率,通过提高双歧杆菌等有益菌的丰度来改变肠道微生物群的组成,并减少肠道中潜在致病菌的数量。这些作用有助于增强肠道屏障的完整性,减轻肠道损伤,从而提高小鼠的存活率。对脓毒症中肠道微生物群代谢物的研究提供了新的见解,凸显了它们在维持肠道屏障功能和免疫反应有效性方面的关键作用。
代谢组学的定义是分析生物系统内的代谢物,它已成为揭示与脓毒症相关的代谢改变的有力方法。例如,肠道微生物群产生的 SCFAs 浓度降低与脓毒症患者肠道屏障功能受损和全身炎症加剧有关。最近的临床前研究表明,粪便微生物群移植可以恢复脓毒症小鼠原有的产生 SCFA 的微生物群落,恢复免疫功能,控制病原体过度增殖。富含纤维的肠内营养等干预措施可以恢复健康的微生物群。这种恢复有可能调节代谢过程并增强脓毒症患者的免疫反应。这些疗法可促进有益代谢物的重新产生,并促进平衡的免疫反应,从而改善患者的预后。
未来的研究方向可能包括多组学整合分析,以解码肠道微生物群代谢物网络。通过多组学整合分析,可以揭示肠道微生物群与宿主之间复杂的相互作用。在进行多组学整合分析时,通过收集不同类型的 omics 数据,包括基因组学、转录组学、代谢组学等,我们可以更全面地了解微生物在宿主代谢中的具体作用。随着研究的深入,更精细的整合分析有望发现新的生物标志物和治疗靶点,从而改善微生物相关疾病的预防和治疗。此外,制定个性化的微生物群代谢物治疗策略也成为近年来微生物组研究领域的一个重要研究方向。这一策略不仅关注微生物群的组成,还强调其代谢物在疾病发生和发展中的作用。在个性化治疗中,分析患者肠道微生物群的组成及其代谢物可以为不同患者制定更精确的治疗策略。多组学整合分析的数据将为制定个性化微生物群代谢物治疗策略提供更有力的支持。此外,还应致力于揭示肠道微生物群与脓毒症之间的因果关系,阐明其作用机制和代谢产物,并制定有效的干预措施。最终,深入了解肠道微生物群代谢产物与宿主之间的相互作用,有望为改善脓毒症患者的预后和存活率提供新的方向。随着研究的不断深入,我们预计肠道微生物群与脓毒症之间的关系将为临床治疗带来革命性的突破,改善患者的生活质量和预期寿命。
其他脓毒症免疫相关信号通路
除了上述在脓毒症患者免疫反应中起关键作用的信号通路外,补体系统通路和 NOD 样受体蛋白 3(NLRP3)炎性体信号通路也有助于脓毒症的免疫调节。在哺乳动物中,补体系统包括 3 个主要激活途径:经典途径、替代途径和凝集素途径。当抗体与病原体表面抗原结合时,经典途径被激活。这种结合会引发级联反应。首先是激活 C1q,然后是 C4、C2 和 C3。最终,这一级联反应导致膜攻击复合物(MAC)的形成。膜攻击复合物负责裂解或摧毁病原体。与此相反,替代途径通过直接识别病原体表面结构激活 C3 而不产生抗体,并遵循类似的过程形成 MAC。与经典途径和替代途径不同,凝集素途径是由病原体的表面糖结构触发的。具体来说,当甘露糖结合凝集素(MBL)或其他凝集素与病原体结合,从而激活补体系统时,凝集素途径就会被激活。这种激活不仅有助于快速清除病原体,还会产生 C3a 和 C5a 等炎症介质。这些介质在吸引免疫细胞和增强整体炎症反应方面起着至关重要的作用。
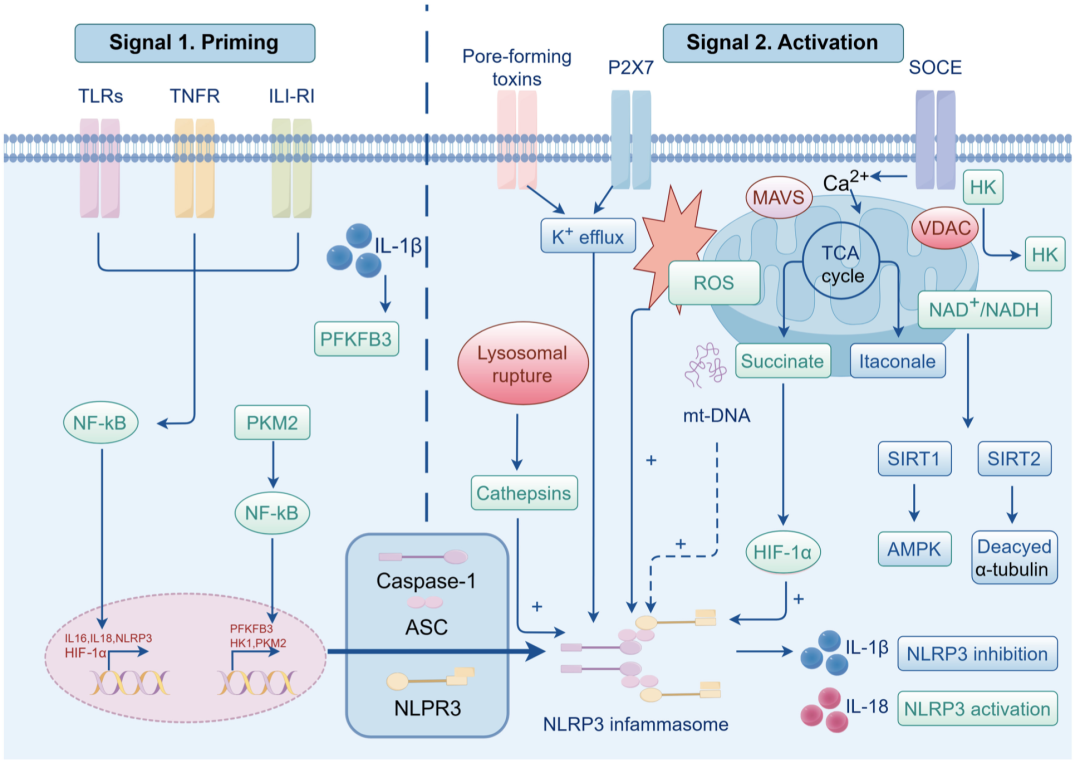
NLRP3 炎性体是一种蛋白质复合物,可调节 Caspase-1 的活化以及 IL-1β 和 IL-18 等促炎细胞因子的释放。此外,人们还发现它能通过非常规途径启动细胞凋亡。就其激活机制而言,当 NLRP3 炎性体被 LPS 激活时,会导致 Caspase-11 的激活。这反过来又触发了一个被称为焦亡的过程,这是一种依赖于炎性体激活的细胞程序性死亡形式。NLRP3 炎性体有助于脓毒症的发展,抑制它可以减轻脓毒症的严重程度。NLRP3 在脓毒症中的双重信号激活机制如图3 所示 。
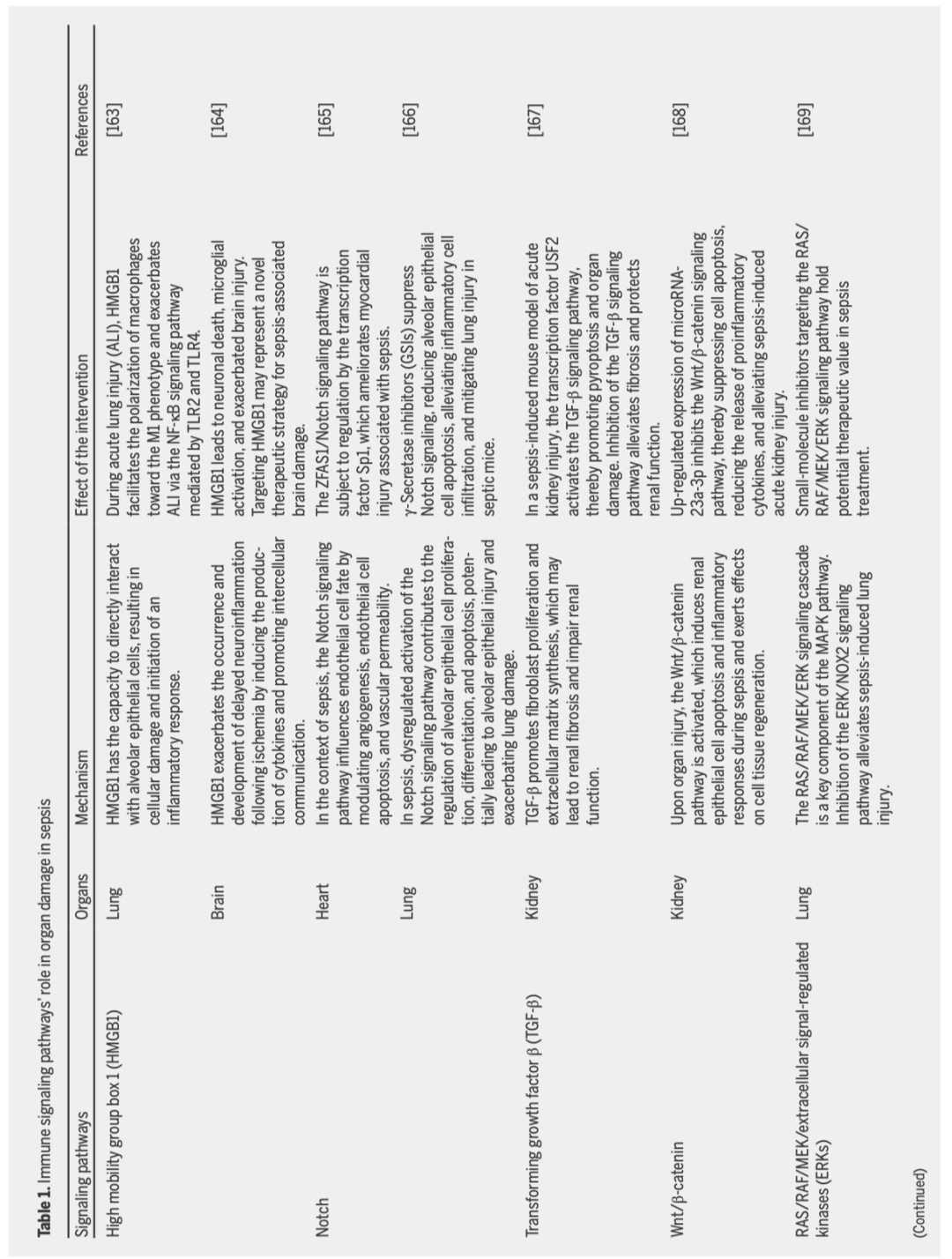
作者在表1中概述了导致脓毒症中观察到的炎症反应和免疫抑制的其他免疫相关信号通路。
上述免疫相关信号通路在脓毒症期间的免疫调节中起着至关重要的作用,它们的异常激活往往会引发炎症反应。脓毒症的炎症反应非常复杂,涉及各种细胞和分子之间的相互作用,与免疫调节密切相关。下面,我们将深入探讨脓毒症中的炎症反应及其相关信号通路。
脓毒症的炎症反应
脓毒症相关炎症反应主要由白细胞介导。这种反应还涉及细胞因子、ROS、内皮细胞、补体系统和凝血系统之间复杂的相互作用。中性粒细胞在识别和清除入侵病原体以及维持免疫平衡方面发挥作用。越来越多的证据表明,以中性粒细胞为靶点有望成为脓毒症治疗的一种治疗方法。例如,从骨髓中释放出来的活化粒细胞会形成 NETs 以捕获病原微生物,这一过程会扩大脓毒症的炎症反应,导致组织损伤。除了中性粒细胞的作用外,脓毒症中观察到的炎症反应的特点是同时发生神经内分泌改变、补体和凝血途径的激活以及脂质介质的改变,所有这些协同作用都有助于炎症状态的放大。这种反应是一个复杂的过程,在抵御感染和防止组织进一步受损方面起着至关重要的作用。在本节中,我们将探讨脓毒症期间炎症反应所涉及的信号通路,尤其关注 MAPK、缺氧诱导因子 1α (HIF-1α)、核因子-红细胞 2 相关因子 2/Kelch-like ECH-associated protein 1 (Nrf2/Keap1)通路。深入了解这些通路对于确定潜在的治疗靶点至关重要,这些靶点可调节炎症过程并改善临床疗效。
MAPK 信号通路
MAPKs 作为在有核细胞和血小板中表达的高度保守的丝氨酸/苏氨酸激酶,其下游的凋亡信号调节激酶 1 (ASK1) 属于丝裂原活化蛋白激酶激酶 (MAP3K) 家族,在应激刺激下可激活下游的丝裂原活化蛋白激酶激酶 (MAP2K)。MAP2K 依次磷酸化下游 MAPK,包括细胞外信号调节激酶(ERK)、c-Jun N 端激酶(JNK)和 p38 MAPK。在脓毒症的情况下,这些信号通路在调节免疫细胞活化、细胞因子产生和细胞凋亡方面各自发挥着不同的作用。当机体检测到 PAMP 和 DAMP 时,这些 MAPK 通路就会被激活。这种激活会引发一系列炎症信号事件。最终导致细胞因子的过度释放,这种现象通常被称为 “细胞因子风暴”。这种风暴在脓毒症患者中经常出现。TLR4/JNK 信号通路可调节 LPS 诱导的促炎细胞因子的产生和心肌功能障碍。在利用脓毒症小鼠模型进行的动物实验中,研究人员应用抑制剂 TAK-242 阻断了 TLR4 的激活。结果,JNK 激活减少,血浆中 TNF-α 蛋白浓度降低,心肌组织学损伤减轻。这些作用有助于维持心脏功能。
考虑到 MAPK 通路在脓毒症期间调节炎症反应的功能,靶向抑制这些通路成为一种很有前景的治疗策略。无论是通过基因敲除、药物干预还是抑制上游因子来抑制 ASK1,都会导致 p38 MAPK 磷酸化和 TLR 介导的细胞因子产生减少。因此,ASK1 是先天性免疫中的一个关键信号元件。ASK1 在调节免疫介导的血小板减少、血栓形成和系统性休克中起着关键作用。因此,抑制 ASK1 可作为治疗免疫复合物(IC)诱导的休克和其他免疫介导的血栓性疾病的治疗靶点。
HIF-1α 信号通路
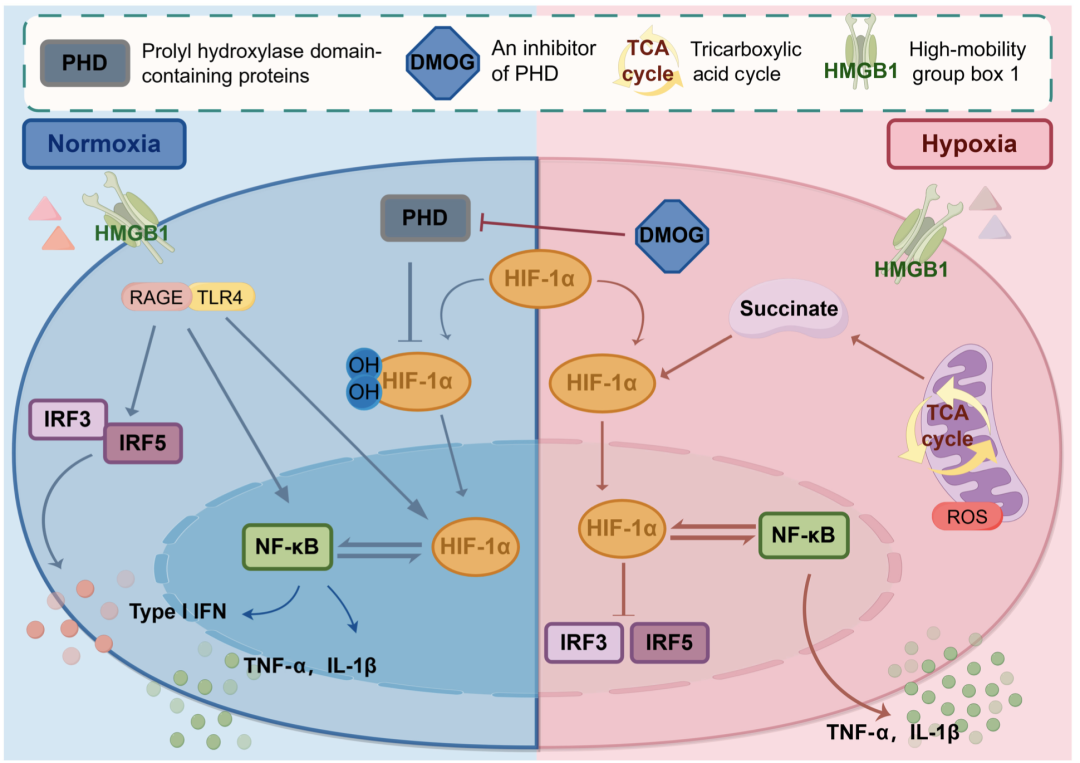
多种病理生理机制导致脓毒症患者出现 MODS。血管内皮损伤、细胞功能障碍和凝血系统活化是罪魁祸首。这些因素以复杂的方式相互作用。最终,它们会导致器官和组织灌注不足、血管内微血栓形成以及大循环和微循环的衰竭。脓毒症造成的组织低灌注会导致组织缺氧,损害细胞对氧的利用。这一过程会产生自由基,其机制与缺血再灌注损伤时的氧化应激类似。HIF-1α 是异源二聚体蛋白复合物 HIF-1 的一个组成部分。它调节细胞对生理性缺氧和感染的反应,通常与急性缺氧条件有关。它的主要作用是激活与糖酵解途径相关的基因,从而降低细胞耗氧量并减少 ROS 的产生。HIF-1α 的激活有助于免疫细胞的新陈代谢适应无氧条件。HIF-1α 在正常和缺氧炎症中的作用示意图见图4。
脓毒症的特点是对感染的炎症反应失调。血液中的单核细胞作为宿主的第一道防线,在这一过程中发挥着至关重要的作用。这些细胞能有效检测入侵的病原体,并迅速引发免疫炎症反应,从而有效对抗感染。在缺氧条件下,虽然单核细胞仍能通过 HMGB1 的作用产生促炎细胞因子,但 IFN1s 的生成受到抑制。这种抑制可归因于缺氧诱导的 HIF-1α,它是 IRF5 和 IRF3 的直接转录抑制因子。因此,HIF-1α 可改变单核细胞的新陈代谢,促进促炎细胞因子的释放,同时保持 IFN 水平的稳定。有证据表明,缺氧和 HIF-1α 会影响细菌的吞噬作用。在 B 组链球菌感染中,当单核细胞中的 HIF-1α 被删除时,细胞内杀死和溶解细菌的能力下降。然而,吞噬吸收率却基本保持不变。HIF-1α 既能促进促炎细胞因子的产生,又能支持细胞存活。这种双重功能使得在脓毒症中调节 HIF-1α 成为一项复杂而具有挑战性的任务,其中包含 2 个不同的方面。HIF-1α 的表达增加会加剧炎症反应,可能导致组织损伤和器官功能障碍,尤其是当缺氧条件超过急性期时。针对 HIF-1α 的靶向疗法是减轻脓毒症中器官损伤的一种有前途的策略。特别是 HIF-1α 抑制剂,有可能减轻过度的炎症反应,同时保留基本的细胞功能。未来的研究应探讨在脓毒症情况下,HIF-1α 的调控对炎症和免疫细胞代谢适应的影响。
Nrf2/Keap1 信号通路
转录因子 Nrf2 属于人类 Cap’n’Collar (CNC) 结构域内的亮氨酸拉链转录因子家族。在生理条件下,Nrf2 被其抑制因子 Keap1 封闭在细胞质中。在应对氧化应激时,Nrf2 被释放并转位到细胞核,在那里它启动了与抗氧化防御和解毒相关的基因转录。由于 Nrf2-Keap1 轴在调节抗氧化、解毒和抗炎反应中的作用,它对疾病预防至关重要。这一途径对于管理脓毒症期间升高的氧化应激至关重要。
目前,针对 Keap1-Nrf2 信号通路的药剂通过两种机制发挥作用。首先,它们能增强 Nrf2 的积累和核转位。它们通过氧化、烷基化修饰或竞争性结合来破坏 Nrf2 和 Keap1 之间的结合。因此,机体的抗氧化应激反应会增强。其次,这些制剂有助于 Keap1 与 Nrf2 分离。它们通过增加 Nrf2 的磷酸化来实现这一目的。磷酸化的增加也会促进 Nrf2 在细胞核中的积累。Nrf2 同时调节抗氧化和炎症途径。体外研究表明,Keap1 缺陷的巨噬细胞对 TLR 激动剂的炎症反应减弱,而 Nrf2 缺陷则会增加对这些激动剂的炎症反应。Nrf2 通路被认为是癌症进展、转移和抗放疗的关键。抑制 Nrf2 有可能减少癌细胞的存活和增殖。同时,它还能提高肿瘤对化疗和放疗的敏感性。这是通过调节免疫反应、增加 DNA 损伤和降低抗氧化防御能力来实现的。我们需要更多的临床数据以及体外和体内实验来加深对 Nrf2 激活的治疗窗口及其与脓毒症所涉及的其他信号通路的相互作用的理解。深入了解 MAPK、HIF-1α 和 Nrf2/Keap1 等与这种反应有关的复杂信号通路,对于推进旨在调节炎症和保护器官功能的靶向治疗策略至关重要。
与脓毒症炎症相关的其他信号通路
除了与脓毒症期间免疫调节有关的信号通路外,还有许多其他通路与这种情况下的炎症反应有关,超出了上述通路的范围。其中包括 cGAS-STING 信号通路、炎症因子/细胞因子通路和 PI3K/Akt 信号通路等。环鸟苷单磷酸(GMP)-腺苷单磷酸(AMP)合成酶(cGAS)和干扰素基因刺激器(STING)通路是近年来发现的一种新型 DNA 传感机制。STING 的激活会引发 IFNs 和各种炎症介质的产生,过度激活可能导致心血管并发症,包括心肌梗死、心力衰竭和心肌炎。
在脓毒症情况下,氧化应激加剧,其产物可抑制 PI3K 活性,降低 Akt 磷酸化水平,损害 PI3K/Akt 信号通路,最终导致炎症反应减弱。此外,PI3K/Akt 信号通路还能调节与细胞凋亡相关的蛋白质的表达,而细胞凋亡是脓毒症中常观察到的一个过程。值得注意的是,以抗炎特性著称的血红素加氧酶-1(HO-1)已被证明可在脓毒症诱导的小鼠肺损伤模型中抑制 PI3K/Akt 信号通路。这种抑制可调节自噬并减轻炎症,从而改善肺功能并提高小鼠的存活率。还有许多信号通路与炎症反应的调控有关,并参与了脓毒症全身器官损伤的发病机制(表2)。
脓毒症中的炎症反应通过各种信号通路对机体产生广泛影响,炎症的持续存在会进一步导致细胞功能障碍。线粒体作为细胞内的关键细胞器,在脓毒症的发病过程中极易受到损伤。接下来,我们将探讨脓毒症中线粒体功能障碍的相关机制。

脓毒症中的线粒体功能障碍
线粒体是细胞内的主要能量发生器,也是细胞凋亡和免疫反应的关键调节器。线粒体功能障碍是脓毒症病理生理学的一个关键组成部分,促使适应性免疫反应转变为病理性炎症和随后的器官衰竭。在脓毒症的情况下,线粒体功能因全身炎症、缺氧和氧化应激而明显受损,导致生物合成活性降低、ATP 生成减少、细胞能量耗竭、ROS 生成增加和细胞凋亡启动。通过细胞呼吸评估线粒体代谢为监测脓毒症等急性病患者的治疗反应和识别有进展至器官衰竭风险的个体提供了宝贵的手段。
线粒体生物能受损
脓毒症引起的线粒体功能障碍通常会导致生物能受损。之所以会出现这种损害,是因为过量产生的 ROS 和炎症介质会损害线粒体 DNA、蛋白质和膜。当线粒体生物能受损时,OXPHOS 过程的效率就会降低。其直接后果是 ATP 生成减少,造成能量不足。这种能量不足对代谢需求高的组织影响更大。此外,从有氧呼吸过渡到无氧糖酵解作为替代能源,会导致乳酸盐的积累。乳酸盐水平升高表明患者患有脓毒症,并提示细胞缺氧和代谢性酸中毒。线粒体生物能的破坏在脓毒症的发生中起着至关重要的作用。它直接导致线粒体功能障碍,减少氧化 ATP 的产生。这些后果最终会导致器官衰竭并增加死亡风险。
线粒体 ROS 在脓毒症中的作用
线粒体代谢是 ROS 的来源之一。最佳水平的 ROS 对细胞信号传递和宿主防御机制至关重要。在脓毒症期间,线粒体 ROS 生成失调导致细胞内抗氧化系统功能紊乱。这种功能障碍会导致细胞成分氧化损伤,并加剧炎症反应。过多的 ROS 生成会诱导炎性体激活,进一步扩大炎症级联反应。因此,利用抗氧化剂或 ROS 清除剂靶向线粒体 ROS 是缓解脓毒症相关氧化应激和炎症的一种很有前景的治疗方法。系统综述和荟萃分析综合了多项研究的证据。这些综合分析的结果表明,抗氧化疗法可有效降低脓毒症患者的短期死亡风险。这些研究结果凸显了以抗氧化剂为基础的治疗方法作为脓毒症治疗方法的潜力。
线粒体诱导的细胞凋亡及其对脓毒症进展的影响
自噬是细胞对营养耗竭或压力的一种反应。它能使细胞成分循环利用,产生氨基酸和脂肪酸。这些物质随后可被代谢并用于 OXPHOS。自噬对于从危重病中恢复至关重要。然而,当线粒体功能失调时,它们可能会产生过多的 ROS。ROS 的增加会刺激自噬。矛盾的是,过于活跃的自噬最终会导致细胞凋亡。脓毒症期间,ROS 和促炎细胞因子水平的增加会导致线粒体膜通透性增强。这种通透性的增强有助于向细胞质释放致凋亡因子,从而激活内在凋亡途径。线粒体功能失调和受损会导致 ROS 生成过多和能量供应不足。线粒体吞噬是一种细胞机制,用于封存和清除这些受损的细胞器,从而减轻这种有害影响。
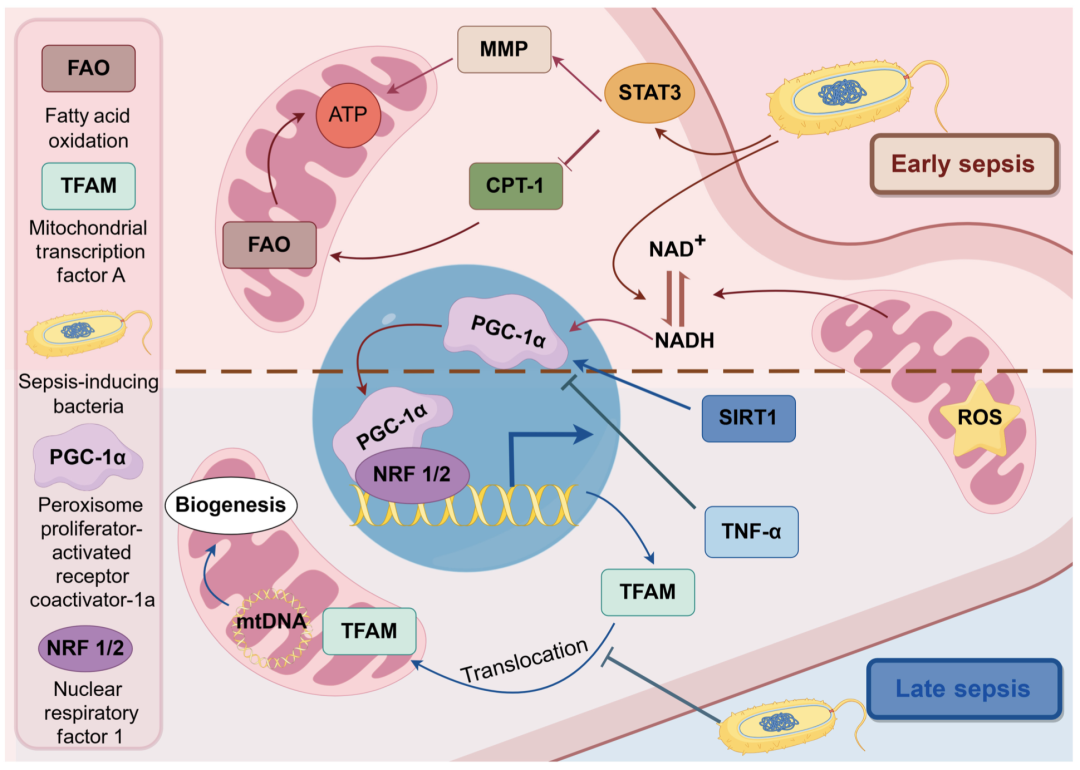
线粒体损伤可诱导淋巴细胞凋亡,这是脓毒症诱导的免疫抑制的一个特征,而 NF-κB 已被证明可通过上调自噬受体 p62 来促进有丝分裂。这是一种自我调节机制,可减轻过度炎症并维持体内平衡。线粒体损伤对脓毒症期间能量供应影响的机理图示(图5 )。
总之,线粒体功能障碍是脓毒症病理生理学的关键,会导致能量衰竭、氧化应激和细胞死亡。掌握这些机制对于创造维持线粒体功能、减轻炎症和提高临床疗效的疗法至关重要。未来的研究应优先确定线粒体内最适合治疗干预的特定分子靶点。此外,还应努力开发可迅速转化为临床实践的策略,以造福脓毒症患者。
线粒体功能障碍在脓毒症的发展过程中起着至关重要的作用,它不仅影响细胞能量供应和细胞凋亡,还与脓毒症的代谢变化密切相关。代谢重编程是脓毒症的一个特征,它与线粒体功能障碍相互作用,共同影响脓毒症的进展。下文将从多方面详细探讨脓毒症中的代谢重编程。
脓毒症中的代谢重编程
代谢重编程是指细胞在特定的生理或病理条件下,调整其代谢途径和代谢产物的利用,以适应环境变化或实现某些功能的过程。这一过程包括多种代谢途径,如糖酵解、氧氧还原、脂肪酸代谢和氨基酸代谢。此外,代谢重编程还涉及代谢中间产物的重新分配和代谢物信号通路的调控。代谢重编程也是脓毒症的一个重要特征。例如,在脓毒症的高炎症阶段,即使在有氧的情况下,细胞也会优先转向糖酵解来产生能量,而不是依赖效率更高的 OXPHOS 过程。其主要驱动因素是线粒体功能障碍导致的 OXPHOS 下调和糖酵解途径激活增强导致的糖酵解上调。在脓毒症的背景下,通过战略性地针对线粒体质量控制机制,特别是调节有丝分裂和线粒体生物生成,可促进代谢重编程,从而积极促进免疫反应的调控。有人提出,脓毒症诱导的 MOF 是一种适应性反应,目的是在感染期间提高细胞存活率。线粒体功能障碍会降低 ATP 生成效率,导致受影响器官能量不足,从而通过下调非必要功能使机体进入 “休眠 ”状态。因此,代谢重编程和能量不足被认为是脓毒症 MOF 发病机制的基本诱因。
了解 PI3K/Akt/ 雷帕霉素机械靶标(mTOR)等关键信号通路和 HIF-1α 在代谢重编程过程中对糖酵解的影响,可为恢复代谢平衡和改善患者预后的治疗策略提供启示。例如,2-脱氧葡萄糖(2-DG)等有氧糖酵解抑制剂已被证明可抑制糖酵解,通过促进乳酸/Sirtuin 3/AMPK 调控的自噬,减少全身炎症和肾损伤。这表明 2-DG 可用于治疗干预。研究数据表明,有效的线粒体干预措施对治疗脓毒症重症患者至关重要,而增强线粒体功能可能提供了一种前景广阔的治疗途径。这可以通过诱导线粒体生物生成和增强抗氧化防御来实现。维持线粒体的平衡将有利于脓毒症患者及早对疾病做出反应,提高患者的存活率。
PI3K/Akt/mTOR 信号通路
PI3K/Akt/mTOR 信号通路参与调节细胞的新陈代谢、生长和存活。在脓毒症中,PI3K/Akt/mTOR 信号通路促使免疫细胞进行新陈代谢重编程。具体来说,该通路介导细胞凋亡和自噬的下调。因此,它可减少与脓毒症相关的心肌损伤。在脓毒症中,PI3K/Akt/mTOR 通路不仅影响炎症和免疫反应,还会改变免疫细胞的新陈代谢。它增强葡萄糖摄取和糖酵解以产生 ATP,而 ATP 对免疫细胞的活化和功能至关重要。这一途径是中性粒细胞正常免疫功能的关键。在脓毒症小鼠模型中抑制 PI3K 与体内中性粒细胞氧化和吞噬活性明显降低有关。尽管向糖酵解的过渡对有效的免疫反应至关重要,但它也可能导致脓毒症中的代谢紊乱,如高血糖和胰岛素抵抗。在脓毒症的情况下,已证明抑制 mTOR 可促进受损细胞器的清除,减轻细胞压力,提高存活率。这一发现表明,在制定针对 PI3K/Akt/mTOR 通路的治疗策略时,有必要谨慎平衡增强免疫细胞功能与保护自噬过程之间的关系。只有这样,才能优化脓毒症患者的治疗效果。
靶向 PI3K/Akt/mTOR 通路成为调节脓毒症患者免疫反应和改善器官保护的一种很有前景的治疗方法。包括雷帕霉素在内的 PI3K 和 mTOR 抑制剂可减轻过度的免疫激活并增强自噬功能。但是,我们必须谨慎考虑这些治疗药物的应用。因为过度抑制可能会损害基本的免疫功能,甚至加剧免疫抑制。例如,在脓毒症小鼠模型中,mTOR 信号通路的过度激活已被证明可诱导 CD4+T 细胞焦亡,加剧与脓毒症相关的免疫抑制。因此,需要开展更多研究,以确定确切的治疗窗口期,并制定选择性调节该通路的策略,从而实现代谢和免疫功能的有利平衡。
HIF-1α 和代谢重编程
在脓毒症组织中经常观察到,HIF-1α 在缺氧条件下会协调从氧合OS 到糖酵解的转变。这种细胞内代谢重编程表明了之前讨论过的沃伯格效应,即免疫细胞即使在缺氧条件下也能快速产生能量,以维持其免疫功能。在脓毒症中,糖酵解途径直接导致乳酸生成增加。乳酸的增加与代谢性酸中毒有关,并最终导致器官功能障碍。
在脓毒症中,由 HIF-1α 介导的糖酵解活性上调不仅能满足免疫细胞的即时能量需求,还能影响整个系统的代谢环境。尽管如此,糖酵解增加可能会导致代谢衰竭,从而降低免疫细胞的反应能力和功效,这也是脓毒症免疫抑制阶段的原因之一。NETosis是中性粒细胞中一种独特的细胞死亡类型,不同于细胞凋亡和坏死。其特点是糖酵解活性增强,有助于形成中性粒细胞胞外捕获物(NETs)。这些 NET 可捕获并消除有害病原体,整个过程就是我们所说的 NETosis。
调节 HIF-1α 的活性是治疗脓毒症的一种很有前景的策略。抑制 HIF-1α 可减轻病理糖酵解转运及其相关的代谢并发症,从而减少组织损伤并增强器官功能。考虑到 HIF-1α 在缺氧条件下维持免疫细胞功能的关键作用,此类干预措施必须经过仔细校准,以防止损害宿主的抗感染能力。将调节 HIF-1α 与其他代谢治疗方法(如改善线粒体功能)相结合,可为脓毒症提供更有效的治疗方法。
总之,代谢重编程是脓毒症的重要组成部分,对疾病进展和患者预后产生深远影响。通过针对 PI3K/Akt/mTOR 和 HIF-1α 等关键通路,并结合微生物组的作用,可以制定更有效的个性化治疗策略,以应对脓毒症带来的复杂代谢挑战。未来,可以深入分析免疫细胞代谢重编程的分子机制,系统阐明脓毒症期间不同免疫细胞亚群代谢表型的变化,为创新治疗策略提供理论依据。研究人员还可以致力于开展大规模、多中心的临床试验,以验证基础研究的结果,探索新的生物标志物。同时,利用机器学习等先进技术分析患者的临床数据,可帮助识别脓毒症的异质性表型,促进精准医疗的发展。此外,通过加强基础研究与临床实践的合作,可以促进新药和治疗策略的研发和临床应用,提高脓毒症的治疗效果。随着对脓毒症发病机制的深入了解,未来有望实现更有效的预防和治疗策略,从根本上改善脓毒症患者的预后。
靶向治疗的前景
目前脓毒症治疗的局限性凸显了研究其病理生理学所涉及的潜在信号通路的迫切需要,这为开发更有效的干预措施提供了潜在的途径。脓毒症的特点是全身免疫失调,包括抗炎和促炎反应。靶向信号通路(包括 JAK/STAT 和 PI3K/Akt)有可能调节免疫细胞功能、恢复免疫平衡并抑制过度炎症反应。此外,脓毒症可导致 MODS。通过调节 HIF-1α 和 AMPK 等特定信号通路,有可能增强器官灌注并减少器官损伤。
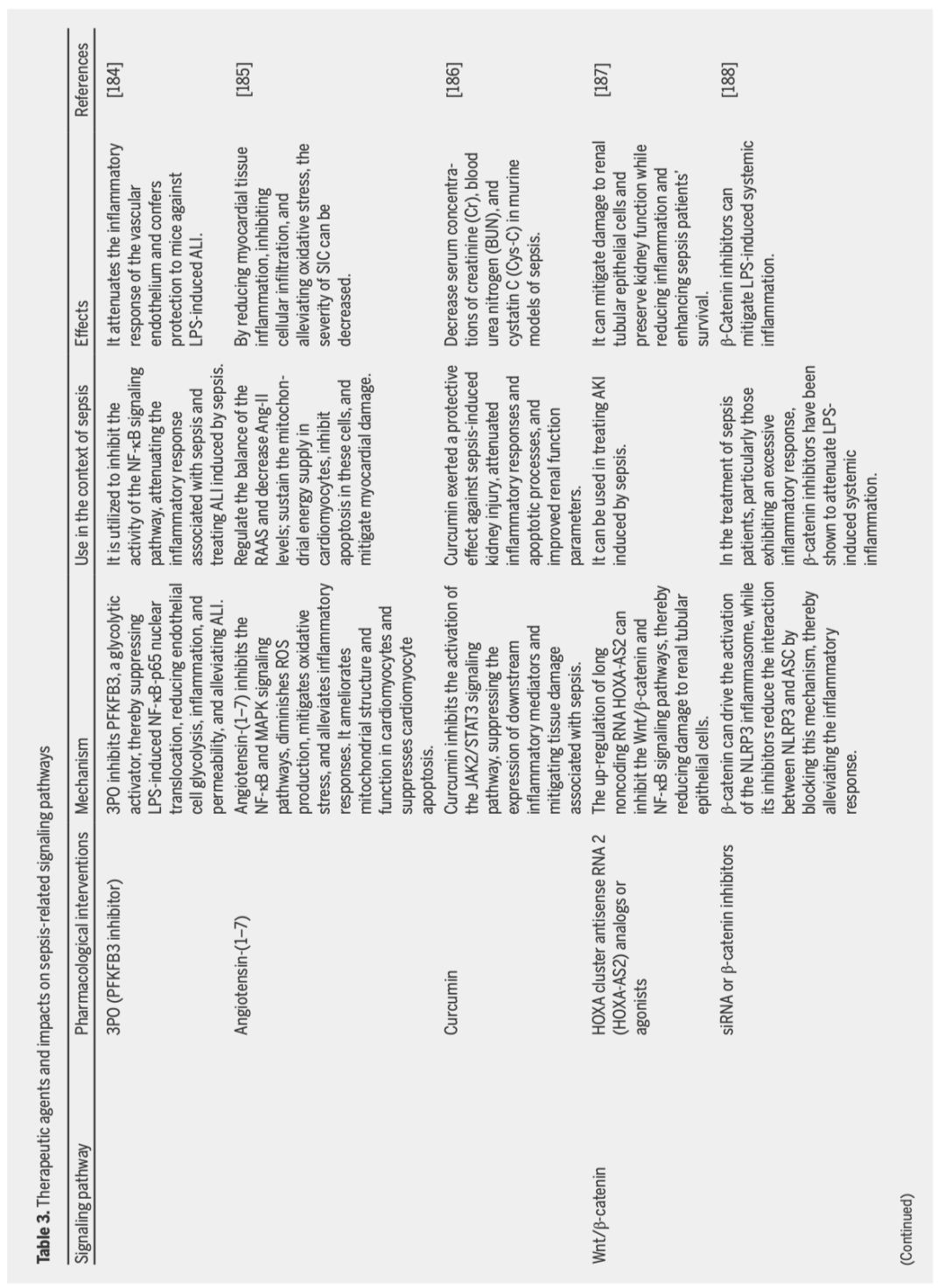
在将脓毒症研究成果有效转化为临床可行的治疗方案之前,仍存在诸多挑战。从发病机制的角度来看,脓毒症包含多种信号通路,它们相互作用建立了一个复杂的调控网络。因此,确定适当的关键信号通路和干预节点是一项重大挑战。从患者治疗的角度来看,靶向治疗必须考虑个体差异性,因为脓毒症患者的病因、临床状况和免疫状态存在明显差异。这些差异会导致不同程度的信号通路激活。尽管已发现越来越多的药物具有治疗脓毒症的潜在疗效,但开发临床治疗药物供人类应用仍然充满挑战。针对信号通路的药物开发过程必须解决药物选择性、生物利用度和毒副作用等问题。此外,该过程本身也十分复杂且成本高昂。就脓毒症的临床试验而言,病情的发展变化很大。为确保试验结果的可靠性,需要仔细考虑试验设计中的诸多因素,包括样本量、干预时机和疗效评估方法。针对脓毒症治疗信号通路的药物研究取得了进展(表3)。
脓毒症是一种涉及多种生物通路的复杂疾病,靶向治疗已成为优化脓毒症治疗的关键策略。生物信息学技术在探索脓毒症靶向疗法方面已显示出巨大的应用价值。例如,一项利用网络药理学分析的研究发现,肝素可能作用于与免疫调节和凝血功能相关的多个靶点,为脓毒症的靶向治疗提供了新的视角。进一步的分子动力学模拟验证了肝素与这些靶点的结合稳定性和亲和力,为开发基于肝素的靶向治疗策略奠定了理论基础。此外,通过干预特定信号通路并结合免疫调节、代谢调节、纳米技术、mAbs 和 microRNAs,可实现个体化治疗,从而提高疗效并减少副作用。在免疫调节疗法领域,细胞因子靶向疗法备受关注。此外,代谢靶向治疗也逐渐成为脓毒症治疗的重要方向。脓毒症患者表现出明显的代谢紊乱,对低氧血症进行靶向治疗可减少 ROS 的积累,改善预后。钙感受体(CaSR)在脓毒症中的双重作用也引起了人们的关注: 它的激活既能缓解器官功能障碍,也可能加剧炎症反应。对 CaSR 信号通路的深入分析将为靶向治疗提供新的见解。针对代谢终点的治疗策略不仅能改善脓毒症的临床疗效,而且有望成为未来的治疗方向。脂质纳米颗粒是一种由脂质分子组成的纳米系统,因其出色的药物包裹性和细胞靶向性,已在脓毒症治疗中显示出优势。纳米药物设计通过调节免疫细胞的功能为脓毒症治疗提供了新的视角。不同的纳米颗粒可诱导免疫细胞向特定方向分化。针对免疫细胞的纳米药物设计在脓毒症的治疗和早期诊断方面都显示出广阔的前景。同时,纳米技术在早期诊断中的应用也可能改变脓毒症的管理模式。 mAb 疗法在脓毒症中也取得了显著疗效。 针对 LPS 及相关炎症信号通路的 mAb 可中和 LPS 的致病作用,抑制炎症。此外,研究表明,调节免疫细胞的活化状态,尤其是通过针对 CD38 高表达单核细胞的靶向治疗,可减轻脓毒症诱发的炎症,提高患者存活率。
脓毒症的靶向治疗在过去几年取得了显著进展,这些新兴方法为改善脓毒症诊断和治疗提供了新的视角和可能性。然而,尽管这些治疗策略具有潜在的益处,但在临床应用中仍需谨慎,特别是要平衡不同研究的观点和发现。未来的工作重点可能是发现新靶点和探索多靶点联合治疗策略。脓毒症并非由单一病因引起,而是涉及多种生物学途径,因此,发现新的治疗靶点和采用多靶点联合疗法将是未来研究的重要方向。通过整合多样化的治疗模式,未来的脓毒症治疗将更加精准,符合患者的个体需求,提高疗效,降低死亡率。这不仅需要基础研究的不断进步,还需要临床试验验证这些新策略的有效性和安全性,最终为改善患者预后提供新的可能。
未来方向和结论
脓毒症是全球健康面临的一大挑战。败血症的特点是免疫反应失调、代谢紊乱和器官功能障碍,发病率和死亡率都很高。因此,急需开发新的、更有效的治疗干预措施。尽管研究工作一直在进行,但现有文献在了解脓毒症病理生理学和确定治疗策略的有效靶点方面仍存在巨大挑战。
尽管在研究脓毒症信号通路方面取得了重大进展,但我们仍然缺乏对这些通路之间如何相互作用以及它们在不同病理阶段发挥何种特定作用的深入了解。因此,未来的研究应考察各种信号通路的改变,并评估它们在脓毒症进展的每个阶段的具体作用。这种方法将有助于精确确定干预窗口和制定有针对性的治疗策略。这包括在脓毒症免疫反应中及时调节这些通路的潜力,理想的情况是在细胞因子风暴开始之前控制和解决全身感染。
脓毒症研究的一大挑战是如何将临床前模型获得的知识转化为临床实践。遗传因素、个体差异和免疫系统背景的差异在很大程度上影响着脓毒症患者的病情发展和预后,从而使统一治疗方案的应用变得复杂。有关脓毒症的人体研究还不够充分。因此,脓毒症的诊断和治疗急需个性化的治疗策略。未来的研究应优先考虑识别和筛选脓毒症相关的生物标志物,并制定个性化的干预策略。这将有助于提高治疗方法的特异性和有效性。目前的治疗模式往往忽视了脓毒症的异质性。它们倾向于使用标准化的治疗方法,但由于个体差异,这种方法可能并不适用于所有患者。未来的工作重点应是识别信号通路中的特定标记物,从而根据患者独特的病理生理学特征对其进行分层。这些生物标志物有可能为个性化治疗策略提供依据,促进早期识别高危脓毒症患者,并促进及时干预。这种方法将使临床医生能够针对信号通路中的特定失调或独特的新陈代谢特征采取有针对性的治疗干预措施。
总之,透彻了解脓毒症的信号通路对于制定有效的治疗策略至关重要。未来的研究可集中在几个关键领域:第一,阐明脓毒症相关信号通路之间复杂的相互作用;第二,开发针对多种信号通路的创新性联合疗法;第三,建立新型免疫监测指标。全面了解脓毒症中错综复杂的信号通路网络对于确定有可能改善患者预后的新靶点至关重要。尽管脓毒症研究取得了进展,但仍存在许多挑战。推进这些研究方向有望为脓毒症的临床治疗带来新的突破,从而提高患者的生存率和生活质量。
本文荟萃自,只做学术交流学习使用,不做为临床指导,本文观点不代表数字重症 ICU.CN立场。

 微信扫一扫
微信扫一扫